Clear Sky Science · pl
Struktury Cryo-EM pośrednich stadiów zespołu portalu-szyi bakteriofaga T4 ujawniają mechanizm zatrzymywania genomu wirusa
Jak wirus utrzymuje DNA pod ciśnieniem
Bakteriofag T4 to wirus atakujący bakterie E. coli i upakowujący swoje DNA w główce tak ciasno, że ciśnienie wewnątrz może być pięć do siedmiu razy wyższe niż w butelce szampana. Mimo to DNA nie wydostaje się, podczas gdy wirus dokańcza budowę reszty swego ciała. To badanie ujawnia na poziomie molekularnym, jak T4 rozwiązuje ten problem, używając malutkich, podwójnych wrót działających jak śluza dla materiału genetycznego.
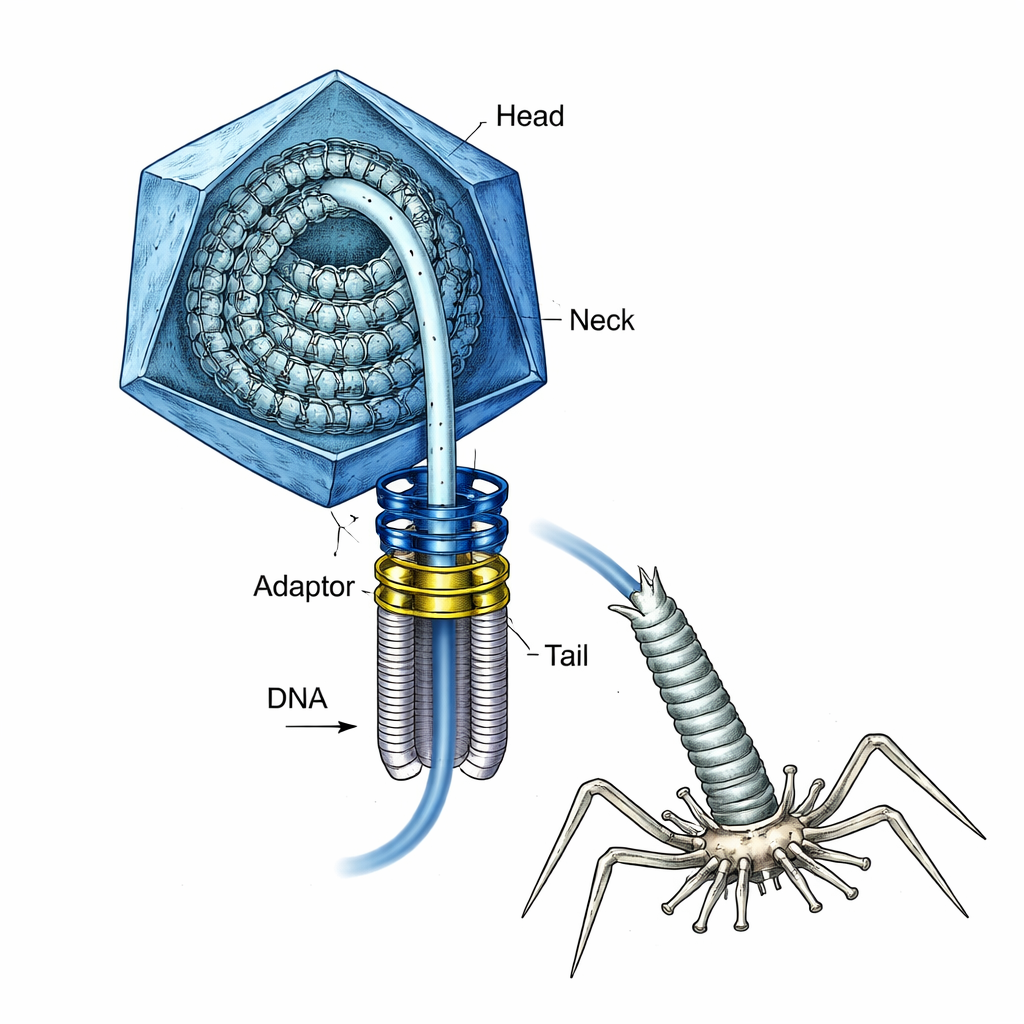
Wirus ze sprężyną w środku
T4 od dawna jest filarem biologii molekularnej i stanowi model przydatny do projektowania przyszłych szczepionek i narzędzi dostarczających geny. Podczas składania wirus najpierw buduje pustą białkową powłokę, czyli główkę, oraz specjalny pierścieniowy „portal” w jednym z wierzchołków. Potężny mechanizm molekularny wtłacza następnie DNA do główki przez ten portal, aż główka stanie się „pełna”. W tym momencie silnik musi odłączyć się, trzeba dołączyć szyję i ogon, a później DNA zostanie wstrzyknięte do bakterii — wszystko to bez pozwolenia, by sprężone DNA wydostało się przedwcześnie. W jaki sposób wirus utrzymywał tak wysoce naprężone DNA bezpiecznie podczas tych przejść, nie było dobrze poznane.
Odbudowa szyi w laboratorium
Naukowcy odtworzyli kluczowe elementy T4 w bakteriach i mieszali je w kontrolowany sposób, aby obserwować, jak składa się szyja — łącznik między główką a ogonem. Dwa białka wirusowe, nazwane gp13 i gp14, wyprodukowano oddzielnie. Każde samo pływało jako jednostka, lecz razem składały się w nawarstwione pierścienie tworzące centralny tunel dla przechodzącego DNA. Ku zaskoczeniu badaczy w tych przygotowaniach pojawiało się trzecie białko: Hfq, dobrze znane bakteryjne białko zwykle pomagające kontrolować RNA i aktywność genów w E. coli. Spektrometria mas potwierdziła, że Hfq wiąże się specyficznie z gp14, sugerując, że wirus zapożycza to białko gospodarza jako część swojej szyi.
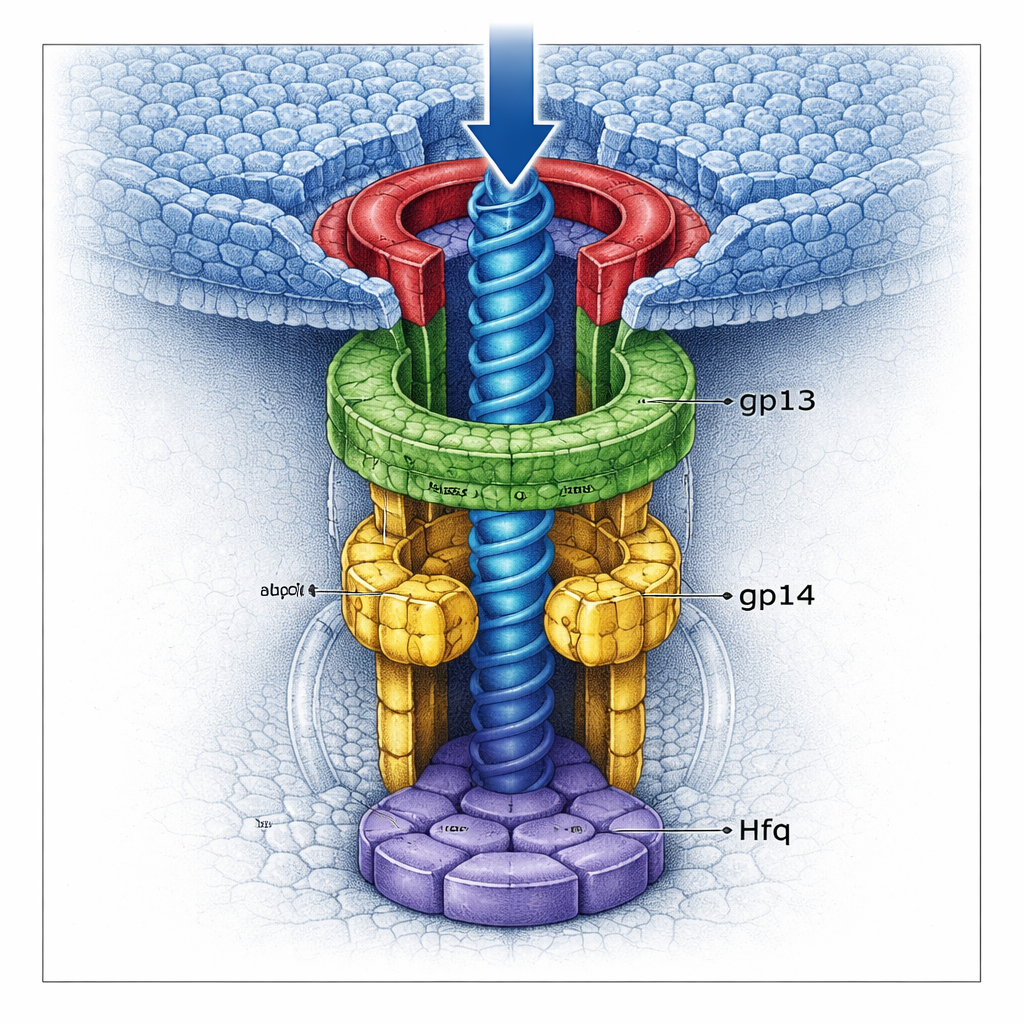
Podwójne wrota blokujące genom
Przy użyciu wysokorozdzielczej kriomikroskopii elektronowej zespół zobrazował kilka wersji kompleksu szyi w niemal atomowych szczegółach. Odkryli, że gp13 tworzy szeroki pierścień dopasowujący się do portalu, podczas gdy gp14 osadza się pod nim jako heksamer, tworząc węższy kanał. Kluczowe jest to, że każdy podjednostka gp14 wnosi długą pętlę, która zamyka się w środkowej części tunelu. Razem sześć takich „pętlowych zatyczek” tworzy szczelną bramę mogącą złapać ostatni odcinek DNA, gdy próbuje opuścić główkę. Pod gp14 zagarnięte białko Hfq układa się w własny heksamer, zatykając dno kanału niczym drugie drzwi. Gdy Hfq jest obecne, struktura gp13–gp14 jest bardziej kompletna i sztywna, a połączone wrota dodatkowo zwężają tunel, znacznie zmniejszając prawdopodobieństwo wycieku DNA.
Czasowanie, zabezpieczenia przed błędami i zapożyczony pomocnik
Badanie pokazuje również, że system ten to nie tylko statyczna zatyczka; to starannie zaaranżowana sekwencja zmian kształtu. Gdy główka jest pełna, wewnętrzne ciśnienie przesuwa portal w nowe konformacje, ujawniając miejsca wiążące dla gp13. Wstępnie zmontowana szyja gp13–gp14–Hfq dokuje wtedy na portalu. Gp13 zgina się, unosi i blokuje zarówno portal, jak i zewnętrzną powłokę, mocno wplatając szyję w główkę. W trakcie tego etapu pętle zatrzaskowe gp14 i korek Hfq utrzymują DNA na miejscu. Hfq pełni drugą rolę jako czynnik kontroli jakości: zajmując kluczowe powierzchnie gp14, zapobiega niewłaściwemu związaniu gp14 z portalem, co mogłoby prowadzić do błędnego złożenia szyi. Dopiero gdy przybywa wstępnie zbudowany ogon, białko końcówki ogona gp15 tworzy jeszcze mocniejsze wiązanie z gp14, wypierając Hfq i otwierając drogę do kontrolowanego uwolnienia DNA do ogona.
Dlaczego to ma znaczenie poza jednym wirusem
Mówiąc prosto, T4 używa blokady z dwoma drzwiami, aby przytrzymać potężną „sprężynę” DNA, podczas gdy dokańcza budowę reszty wirusa. Pierwsze drzwi buduje z własnego białka szyi, gp14, a drugie drzwi zapożycza z białka gospodarza Hfq, którego wirus używa tymczasowo, a następnie odrzuca. Ta podwójna brama zapewnia, że niemal żadne DNA nie zostanie utracone i że końcowy wirus jest w pełni zakaźny. Ponieważ wiele dużych wirusów pakuje swoje genomy pod podobnym ekstremalnym ciśnieniem i dzieli zbliżoną architekturę, praca ta sugeruje, że porównywalne systemy blokujące, a nawet tymczasowe hijackowanie białek gospodarza, mogą być powszechne. Zrozumienie tych mechanizmów może pomóc w projektowaniu bezpieczniejszych wektorów wirusowych do medycyny oraz wskazać nowe sposoby blokowania szkodliwych wirusów poprzez celowanie w ich „zamki” genomowe.
Cytowanie: Han, L., Mao, Q., Zhu, J. et al. Cryo-EM structures of bacteriophage T4 portal-neck assembly intermediates reveal a viral genome retention mechanism. Nat Commun 17, 1964 (2026). https://doi.org/10.1038/s41467-026-69107-7
Słowa kluczowe: bakteriofag T4, składanie wirusa, kriomikroskopia elektronowa, pakowanie genomu, interakcja gospodarza z wirusem