Clear Sky Science · pl
Struktury in situ kompleksu portal-szyjka-ogon bakteriofaga T4 wskazują mechanizm pozycjonowania genomu wirusa
Jak wirus nakręca swoją genetyczną sprężynę
Bakteriofagi — wirusy atakujące bakterie — należą do najbardziej wysublimowanych nanomaszyn w przyrodzie. Jeden z najlepiej poznanych, bakteriofag T4, musi upakować swoje długie DNA do maleńkiej główki, a następnie wystrzelić je do komórki bakteryjnej w ułamku sekundy. Badanie to ukazuje niemal atom po atomie, jak T4 precyzyjnie pozycjonuje swoje DNA jak sprężynę skompresowaną wewnątrz ogona, gotową do wystrzału do nowego gospodarza bez utraty choćby jednego „znaku” genetycznego. 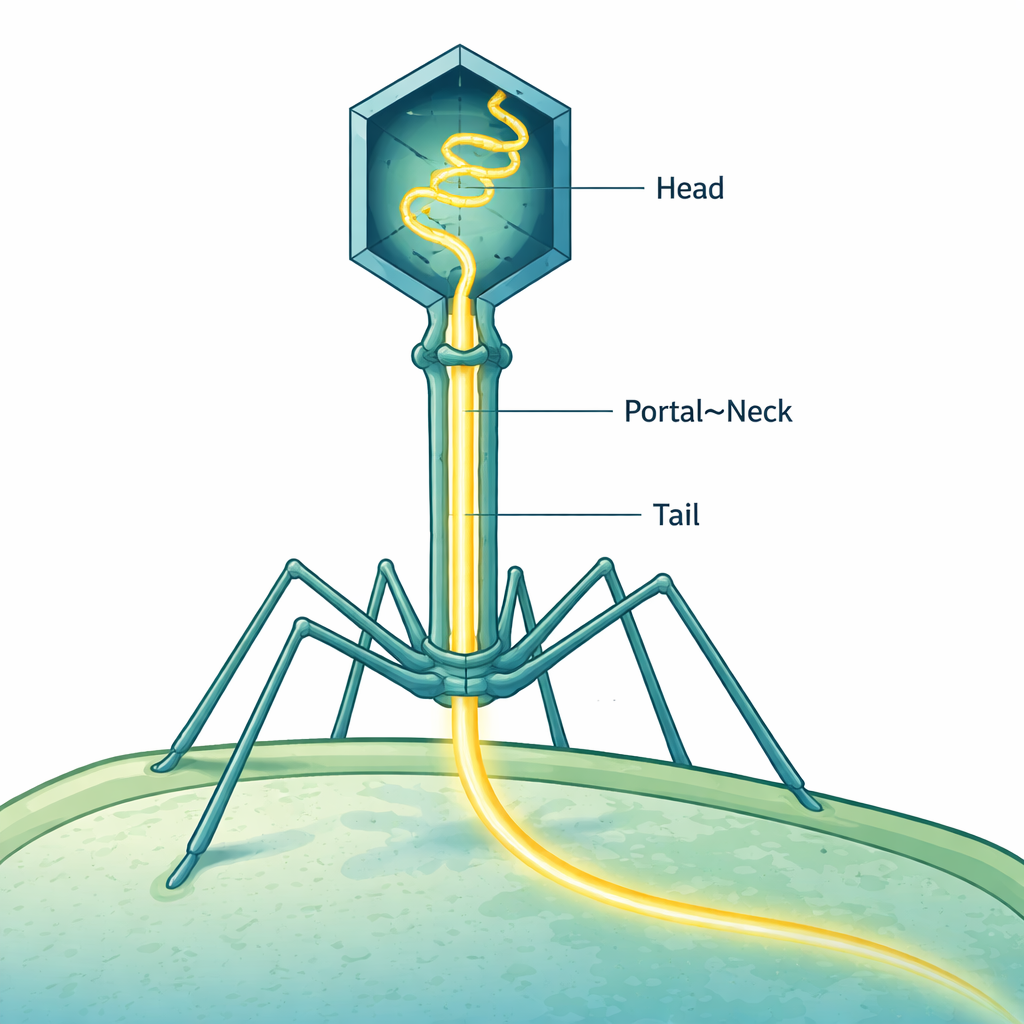
Wirusowa główka pod wysokim ciśnieniem
W białkowej otoczce faga DNA jest upakowane niemal do gęstości krystalicznej, wytwarzając wewnętrzne ciśnienie około 25–35 atmosfer — porównywalne z ciśnieniem w głębinach oceanicznych. Autorzy zastosowali wysoko rozdzielczą kriomikroskopię elektronową, by zobaczyć, co dzieje się przy specjalnym „porcie”, przez który DNA wchodzi i wychodzi z główki. Stwierdzili, że gdy główka się zapełnia, pierścieniowy białkowy portal zmienia kształt z przypominającego „latający spodek” na formę podobną do grzyba i przesuwa się w dół względem osłonki. Ten napędzany ciśnieniem przesuw wydaje się sygnalizować, że zapakowano wystarczającą ilość DNA, uruchamiając odłączanie silnika napędzającego pakowanie oraz odsłaniając nowe miejsca dokujące dla kolejnych elementów wirusowego aparatu.
Budowa blokującej szyjki między główką a ogonem
Gdy główka jest pełna, między główką a ogonem montuje się struktura szyjki, działająca zarazem jako łącznik i zawór. Dwa białka szyjki, nazwane gp13 i gp14, tworzą pierścienie poniżej portalu. Gp13 unosi część swojej struktury, by objąć portal i sięga także do otaczającej osłonki, ściśle wiążąc główkę z szyjką oraz zapewniając punkty przyczepu dla włókien dekoracyjnych. Gp14, znajdujące się niżej, początkowo tworzy z białkiem gospodarza Hfq podwójny „zawór genomowy”, skutecznie zatykając kanał wyjściowy, aby wysokociśnieniowe DNA nie wyciekło przedwcześnie. W tym zamkniętym stanie DNA zatrzymuje się w pobliżu szyjki i jest utrzymywane w miejscu, podczas gdy reszta wirusa kończy montaż.
Dokowanie ogona otwiera zawór
Następnym krokiem jest dołączenie wstępnie zbudowanego ogona, składającego się z wewnętrznej tuby otoczonej kurczliwą pochewką i zakończonego złożoną płytką bazalną rozpoznającą powierzchnię bakterii. Na szczycie tego ogona znajduje się pierścień „terminatora ogona”, gp15, a tuż poniżej inny pierścień, gp3, zamyka wewnętrzną tubę. Gdy ogon dokuje do szyjki, gp14 przechodzi dramatyczną reorganizację: jej pętle tworzące zawór obracają się w dół i zaciskają na gp15, podczas gdy wydłużony „ogon” gp14 owija się wokół gp15, tworząc bardzo dużą, naładowaną powierzchnię interakcji. Ruchy te wyrzucają zatyczkę Hfq i odchylają pętle gp14 z toru, przeobrażając kiedyś zamkniętą szyjkę w całkowicie otwarty kanał, wyrównany teraz z pustą tubą ogona.
DNA schwytane przez molekularną miarę
Z otwartym zaworem DNA — wciąż pod wysokim ciśnieniem — nie wylewa się po prostu na zewnątrz. Zamiast tego przemieszcza się około 17 nanometrów w dół przez nowo uformowany łącznik portal–szyjka–ogon. Na styku z gp3 i szczytem tuby ogona napotyka „białko miarki” (tape-measure protein, TMP), długie zwinięte białko, które pierwotnie działało jak miarka określająca długość ogona. Koniec TMP ma segmenty wiążące DNA, które chwytają czubek genomu. Dalsze ciśnienie z upakowanej główki przesuwa następnie kompleks DNA–TMP głębiej w tubę ogona, ściskając zwinięte segmenty TMP jak sprężynę i przesuwając czubek DNA na dno drugiego pierścienia tuby ogona. 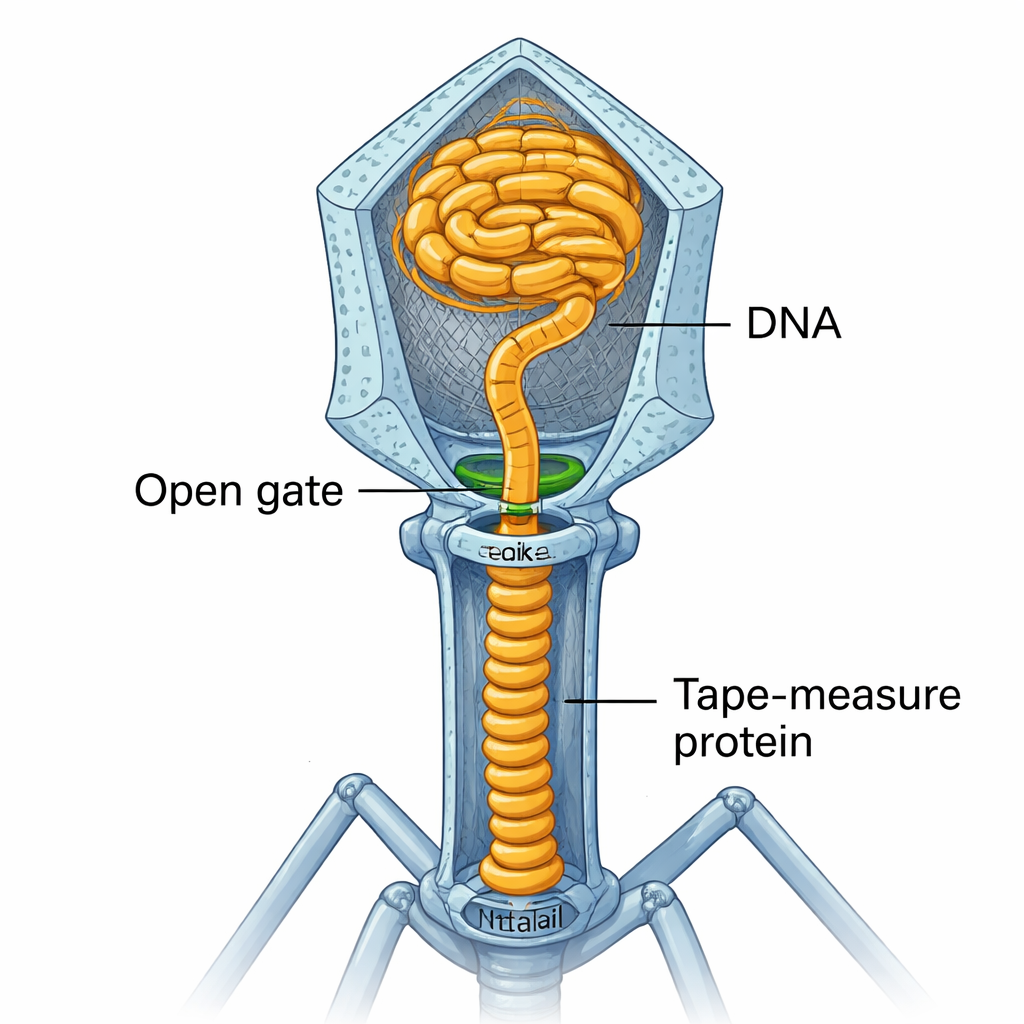
Sprężynujący genom gotowy do wystrzału
Te strukturalne migawki pokazują, że po złożeniu genom faga nie jest po prostu przechowywany w główce; jest celowo pozycjonowany tak, aby jego wiodący koniec był zawieszony głęboko w wewnętrznym tunelu biegnącym od główki, przez szyjkę i do ogona. DNA jest tam utrzymywane przez skompresowane białko miarki oraz „zatyczkę” przy płytce bazalnej, utrzymując metastabilny, naładowany stan sprężynowy. Gdy płytka bazalna wykryje i zablokuje receptor bakteryjny, wywołuje zmiany usuwające tę zatyczkę i pozwalające skompresowanemu kompleksowi DNA–TMP rzucić się naprzód, prowadząc genom gładko do wnętrza komórki gospodarza. W istocie wirus wyewoluował napędzany ciśnieniem system ładowania i celowania, który zapewnia szybkie, kompletne i niezawodne dostarczenie ładunku genetycznego.
Cytowanie: Fokine, A., Zhu, J., Klose, T. et al. In situ structures of the portal-neck-tail complex of bacteriophage T4 inform a viral genome positioning mechanism. Nat Commun 17, 1965 (2026). https://doi.org/10.1038/s41467-026-69106-8
Słowa kluczowe: bakteriofag T4, pakowanie DNA wirusa, kriomikroskopia elektronowa, struktura wirusa, mechanizm infekcji fagowej