Clear Sky Science · pl
Strukturalne podstawy pauzy podczas inicjacji transkrypcji w Mycobacterium tuberculosis
Jak przełączniki genów zarazka mogą się zablokować
Mycobacterium tuberculosis, bakteria wywołująca gruźlicę, musi nieustannie włączać i wyłączać geny, by przetrwać w trudnych warunkach panujących w organizmie. Opisane tu badanie zagląda w jeden z najwcześniejszych etapów tej kontroli genetycznej, uchwytując przelotną „pauzę”, która zachodzi w momencie, gdy komórka zaczyna przepisywać DNA na RNA. Zrozumienie tej pauzy pomaga wyjaśnić, jak mikroorganizm decyduje, czy w pełni włączyć dany gen, czy przerwać próbę — i może w końcu ujawnić nowe słabe punkty dla antybiotyków.
Rozpoczynanie przekazu z DNA
W bakteriach duże białkowe urządzenie zwane polimerazą RNA porusza się po DNA, tworząc RNA — pierwszy krok w kierunku produkcji białek. Na początku współpracuje z pomocniczymi białkami zwanymi czynnikami sigma, które kierują ją do konkretnych miejsc startu na DNA i pomagają rozchylić niewielką „bańkę” w podwójnej helisie. Dla Mycobacterium tuberculosis jednym z takich czynników jest sigma E, szczególnie ważny, gdy bakteria doświadcza stresu poza swoją wewnętrzną błoną komórkową. Inny czynnik, CarD, pomaga stabilizować otwartą bańkę DNA. Razem te elementy tworzą kompleks inicjacyjny, który wytwarza pierwsze kilka nukleotydów RNA, zanim albo zobowiąże się do produkcji długiego RNA, albo zrezygnuje i uwolni krótkie fragmenty RNA.
Ukryta pauza przy długości sześciu lub siedmiu nukleotydów
Wcześniejsze badania biochemiczne i pojedynczych cząstek sugerowały, że polimeraza RNA często pauzuje bardzo wcześnie, gdy nowy łańcuch RNA ma tylko sześć lub siedem nukleotydów długości. Jednak te pauzy są niezwykle krótkotrwałe i trudne do bezpośredniego zaobserwowania, więc brakowało struktur o wysokiej rozdzielczości. W tym badaniu autorzy użyli krioelektronowej mikroskopii (cryo-EM), by «zamrozić» i zobrazować kilka wersji maszyny inicjacyjnej z M. tuberculosis. Przygotowali rusztowania DNA–RNA, które zatrzymują kompleks, gdy RNA ma sześć lub siedem jednostek, i rozwiązali struktury trzech głównych stanów: dwóch „zwykłych” kompleksów inicjacyjnych oraz odrębnego kompleksu w stanie pauzy.
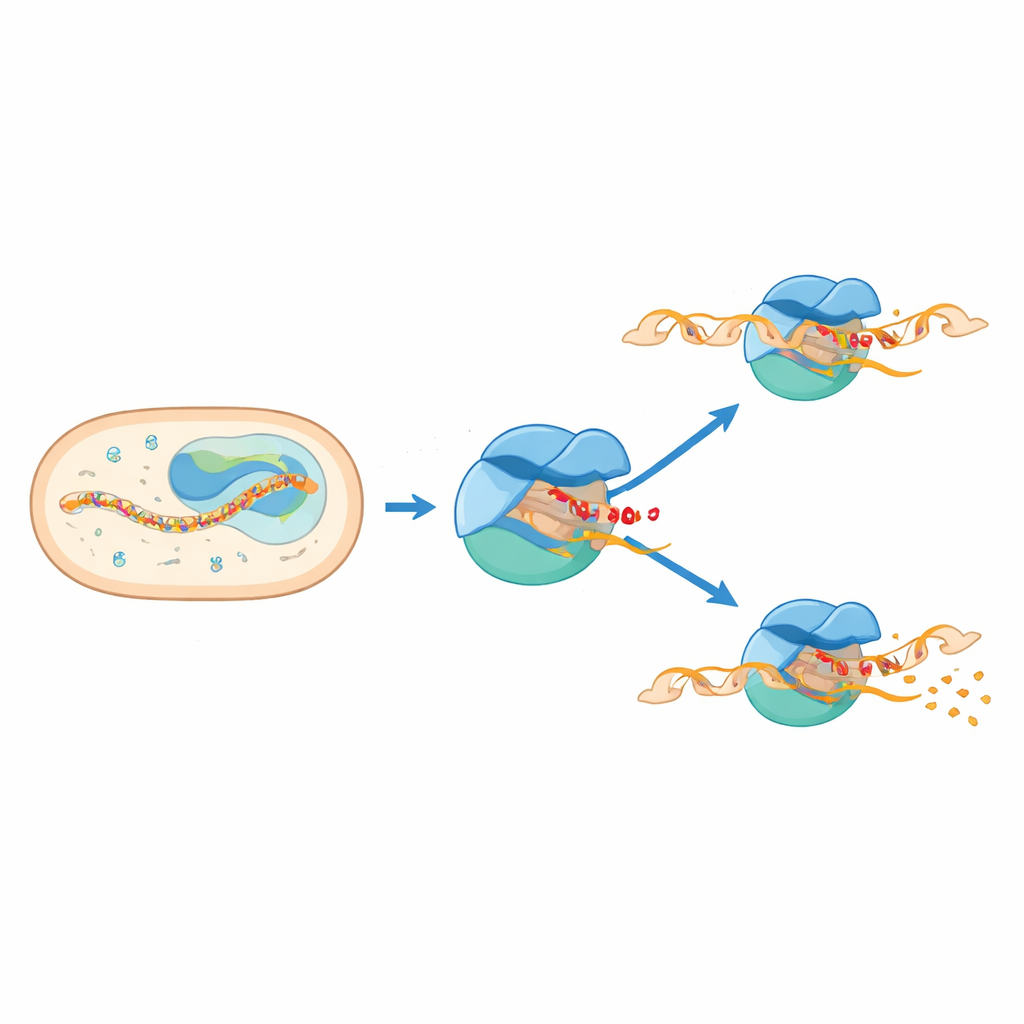
Gdy dwie części maszyny się zderzają
Struktury ujawniają, że pauza powstaje, gdy dwie części aparatu próbują zająć to samo miejsce. Giętki fragment sigma E, znany jako region 3.2, wsuwa się do kanału, którym musi przejść wydłużające się RNA, żeby wydostać się z enzymu. W miarę jak RNA wydłuża się do sześciu lub siedmiu nukleotydów, jego czołowa część zderza się z tym wysuniętym pętlą. To zderzenie wymusza obrócenie dużego modułu wewnątrz polimerazy RNA i deformuje kluczowy element strukturalny zwany helisą mostkową. Równocześnie DNA tuż upstream miejsca aktywnego jest wciągane do środka i częściowo rozwijane, tworząc „ściśniętą” i załamaną bańkę. Te sprzężone ruchy blokują kompleks w pauzowanym, pół-przesuniętym stanie, który magazynuje naprężenia mechaniczne.
Pomocnik zmieniający kształt usztywnia bańkę
Okazuje się, że czynnik pomocniczy CarD odgrywa bardziej wszechstronną rolę, niż sądzono wcześniej. W niepauzowanym kompleksie inicjacyjnym CarD klinuje się w rowek minorowy jednej nici DNA na krawędzi bańki, pomagając utrzymać bańkę otwartą, by polimeraza mogła rozpocząć syntezę. W kompleksie w pauzie CarD przesuwa się, obejmując przeciwległą, niekodującą nić DNA i współpracuje z sigma E, aby szczelniej zacisnąć ściśniętą bańkę. Testy biochemiczne pokazują, że CarD zwiększa transkrypcję zależną od sigma E i wpływa na liczbę cząsteczek RNA gromadzących się na etapie sześciu–siedmiu nukleotydów. Wyniki te sugerują, że CarD zarówno stabilizuje początkowy stan otwarty, jak i pomaga kompleksowi w pauzie uniknąć przedwczesnego zapadnięcia się.
Punkt kontrolny między porażką a zobowiązaniem
Porównując struktury o wysokiej rozdzielczości utworzone na częściowo wstępnie otwartym DNA z strukturami o niższej rozdzielczości zmontowanymi na w pełni sparowanym DNA, autorzy pokazują, że te same zasadnicze kształty pauzy pojawiają się także w bardziej naturalnych warunkach. Proponują, że zderzenie pomiędzy wydłużającym się RNA a pętlą sigma 3.2 tworzy punkt kontrolny naładowany energią przy długości sześciu do siedmiu nukleotydów. Z tego stanu kompleks może pójść dwiema głównymi drogami: może uwolnić krótkie RNA i zresetować się — próba abortywna — albo wykorzystać zgromadzone naprężenie, by wyrwać się z regionu promotora i wejść w stabilną, długotrwałą produkcję RNA. Przemieszczenie się CarD i poluzowanie uchwytu czynnika sigma nad upstream DNA wydają się kierować tą decyzją.
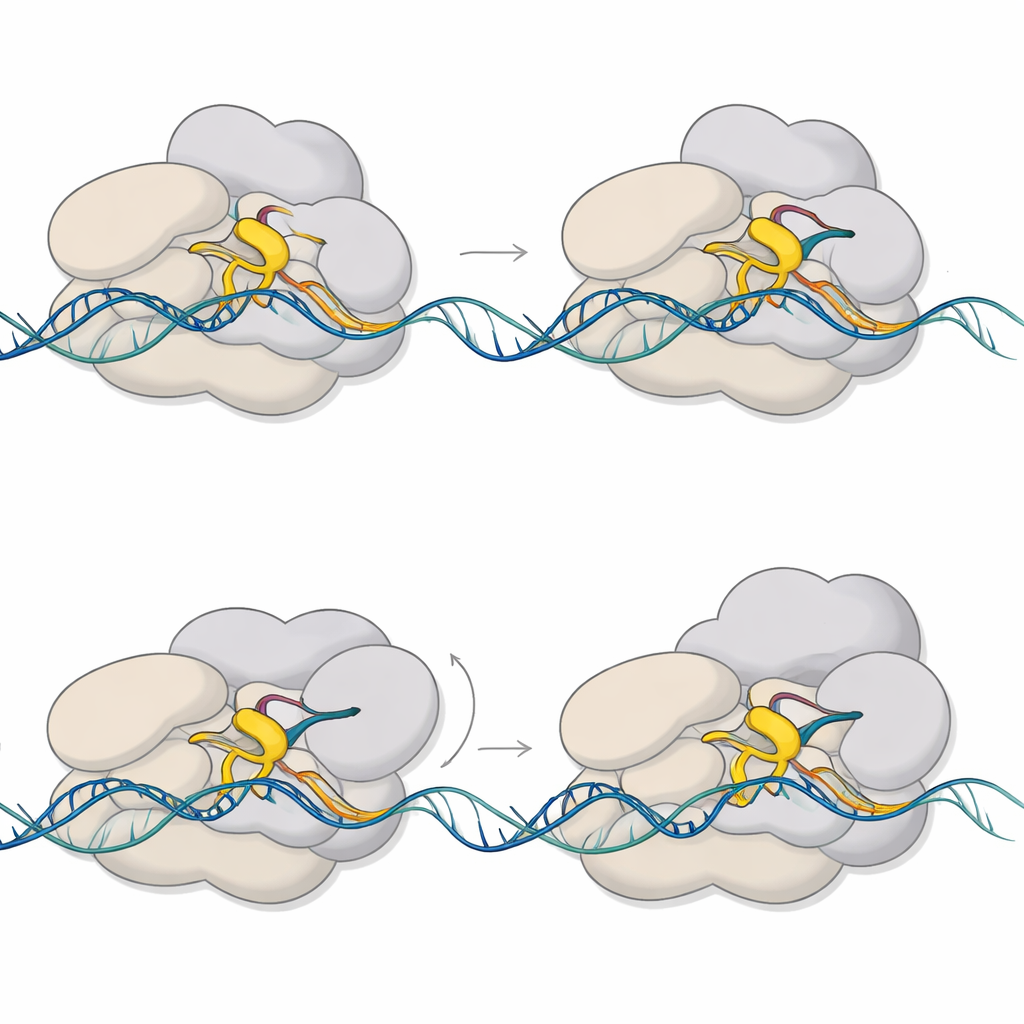
Dlaczego to ma znaczenie dla gruźlicy
Dla czytelnika nietechnicznego najważniejsza konkluzja brzmi: bakteria prątków gruźlicy nie włącza genów po prostu jak światła. Zamiast tego waha się przy bardzo krótkim RNA, używając krótkiej mechanicznej pauzy jako punktu decyzyjnego między przerwaniem a zobowiązaniem do pełnej aktywacji genu. To badanie utrwala tę pauzę w atomowych detalach, pokazując, jak mała ruchoma pętla, obracające się jądro i przekształcona bańka DNA wspólnie tworzą kontrolowany punkt kontrolny. Ponieważ sigma E i CarD są kluczowe dla reakcji M. tuberculosis na stres, te spostrzeżenia mogą w przyszłości pomóc badaczom zaprojektować leki, które zaklinują ten wczesny etap i osłabią zdolność bakterii do adaptacji i przetrwania.
Cytowanie: Zheng, L., Xu, K. Structural basis of pausing during transcription initiation in mycobacterium tuberculosis. Nat Commun 17, 2197 (2026). https://doi.org/10.1038/s41467-026-69104-w
Słowa kluczowe: inicjacja transkrypcji, pauzowanie polimerazy RNA, Mycobacterium tuberculosis, czynniki sigma, cryo-EM