Clear Sky Science · pl
Ostra zapalenie otrzewnej indukuje adipocytarne CD127+ ILC1, które wyrażają PD-L1 i łagodzą zapalenie u myszy
Dlaczego tłuszcz brzuszny może pomóc walczyć ze śmiertelną infekcją
Gdy bakterie przedostaną się z rozdartego jelita do jamy brzusznej, organizm może wpaść w stan zagrażający życiu zwany sepsą. Badanie to ujawnia niespodziewanego sprzymierzeńca w tej walce: specjalną grupę komórek odpornościowych ukrytych w tłuszczu brzusznym, które migrują tam we wczesnej fazie infekcji i działają jak wbudowany hamulec nadmiernego zapalenia. Zrozumienie mechanizmów ich działania może zainspirować nowe terapie, które łagodzą niebezpieczne infekcje bez całkowitego tłumienia układu odpornościowego.
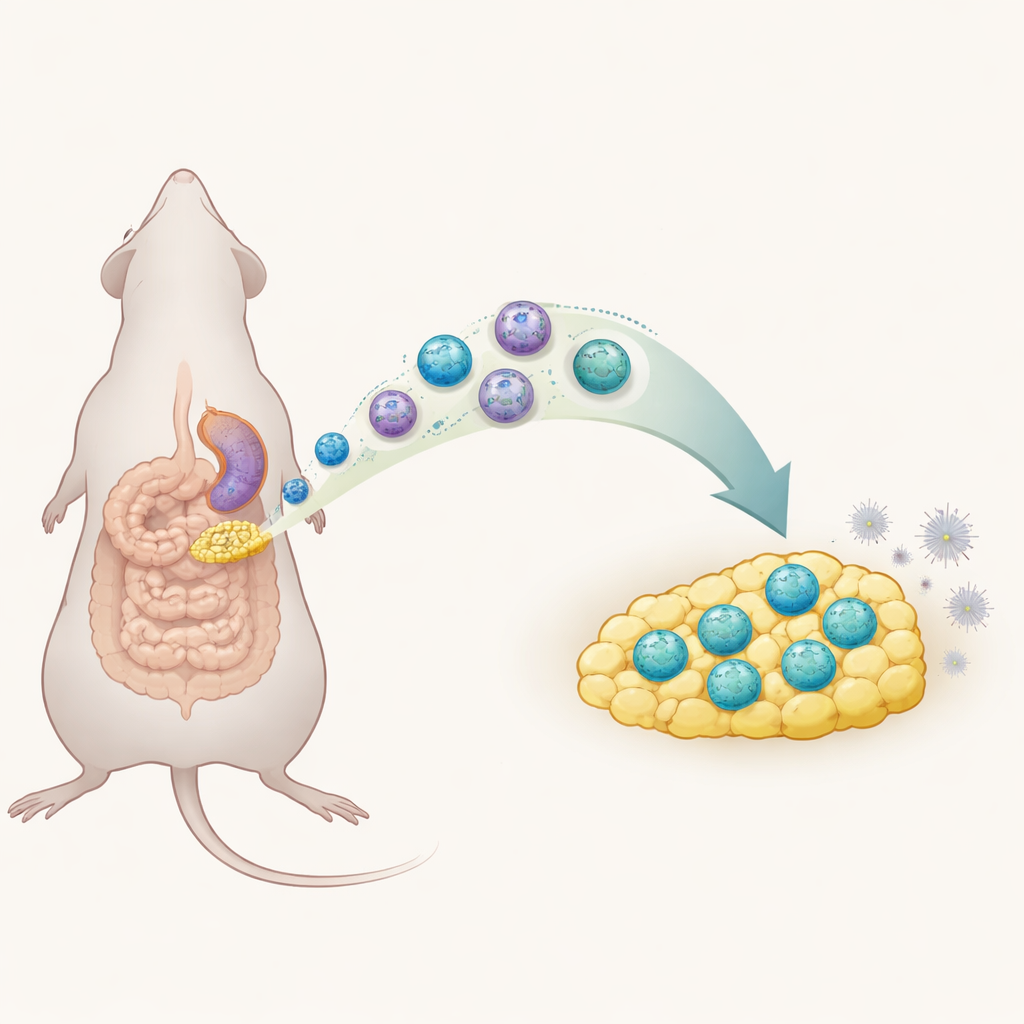
Niebezpieczny przeciek w jamie brzusznej
Zapalenie otrzewnej występuje, gdy wyściółka jamy brzusznej ulega zapaleniu, najczęściej dlatego, że bakterie wydostają się z perforowanego jelita. Jeśli ten wczesny sztorm zapalny nie zostanie opanowany, pacjenci mogą rozwinąć sepsę, która mimo nowoczesnej opieki nadal zabija około jednej na pięć zakażonych osób. Lekarze mogą leczyć zakażenie chirurgicznie i antybiotykami, ale dysponują niewieloma narzędziami, by skierować reakcję odpornościową organizmu z dala od szkodliwego nadmiernego pobudzenia. Tłuszcz okrywający jelita, zwany tkanką tłuszczową krezkową, jest znany z tego, że gromadzi się w miejscach uszkodzeń jelit, co sugeruje, że odgrywa aktywną rolę we wczesnej odpowiedzi immunologicznej.
Ukryci strażnicy w tłuszczu brzusznym
W ostatnich latach naukowcy odkryli „wrodzone komórki limfoidalne”, szybkie strażniki odpornościowe zamieszkujące wiele tkanek. Jeden podtyp, nazywany grupą 1 ILC, zazwyczaj pomaga zapoczątkować silne reakcje zapalne. W badaniu na myszach badacze zastosowali standardowy model chirurgiczny zapalenia otrzewnej, by sprawdzić, jak te komórki zachowują się w tłuszczu krezkowym. Odkryli, że sześć godzin po urazie ta tkanka rozświetliła się sygnałami zapalnymi i napływem komórek ILC1, podczas gdy inne pokrewne typy komórek zmieniły się zaledwie w niewielkim stopniu. Ten czas odpowiadał szczytowi choroby u zwierząt, co sugeruje, że ILC1 są ściśle powiązane z wczesną fazą zapalenia w jamie brzusznej.
Podróżujące komórki, które zmieniają swoją naturę
Głębiej analizując, zespół zastosował zaawansowane profilowanie pojedynczych komórek, aby podzielić populację ILC1 na podgrupy. W normalnych warunkach większość ILC1 w tłuszczu brzusznym nie miała na powierzchni cząsteczki zwanej CD127. W przebiegu ostrego zapalenia otrzewnej pojawiła się jednak nowa grupa ILC1 z pozytywnym oznaczeniem CD127, która się rozrosła. Nowo przybyli wytwarzali mniej silnego sygnału zapalnego interferonu gamma niż ich CD127-ujemni kuzyni, co oznaczało, że są stosunkowo powściągliwi. Naukowcy wykazali, że wiele z tych komórek nie dzieliło się po prostu na miejscu: zamiast tego ILC1 ze śledziony przemieszczały się przez krew do tłuszczu krezkowego, kierowane częściowo przez chemiczny sygnał „homingowy” CXCL10 i jego receptor CXCR3. Po dotarciu do tłuszczu zmieniały markery powierzchniowe, zyskując CD127 i przyjmując spokojniejszą, bardziej regulacyjną tożsamość.
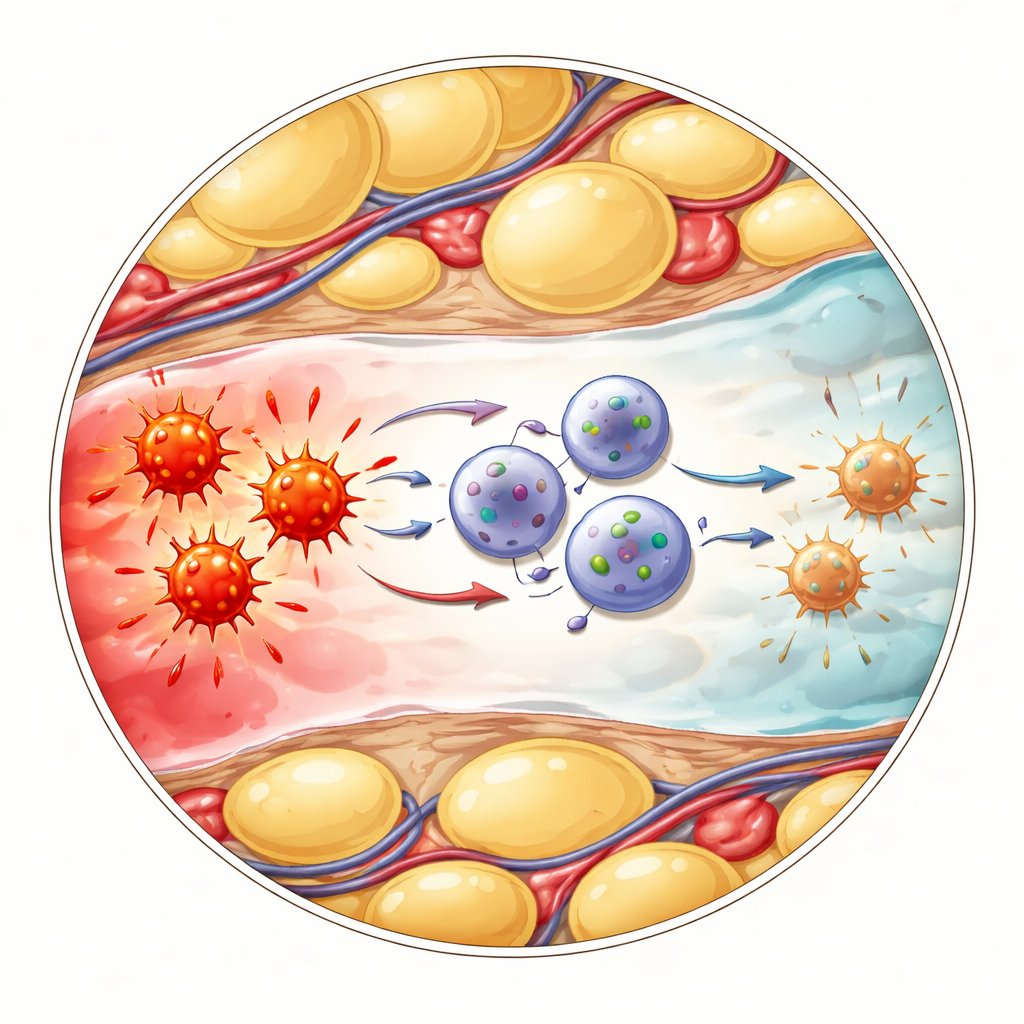
Jak łagodzące komórki rozmawiają z zapalczywymi komórkami
Następne pytanie brzmiało, jak te zmienione ILC1 rzeczywiście tłumią zapalenie. Badacze skupili się na innej grupie odpornościowej, komórkach gamma-delta T, które reagują szybko na zagrożenie i mogą uwalniać duże ilości alarmowej cząsteczki TNF. Analizy pojedynczych komórek sugerowały, że CD127-dodatnie ILC1 i komórki gamma-delta T komunikują się poprzez dobrze znaną ścieżkę „hamującą” obejmującą białka powierzchniowe PD-L1 i PD-1. W zapalonym tłuszczu brzusznym nowo przybyłe ILC1 silnie zwiększały ekspresję PD-L1, podczas gdy pobliskie komórki gamma-delta T wykazywały wysokie poziomy PD-1. Gdy zespół zablokował PD-1 przeciwciałami, komórki gamma-delta T zwiększyły wydzielanie TNF, co potwierdziło, że ten kontakt zwykle hamuje ich produkcję zapalnego sygnału. Podobnie myszy genetycznie pozbawione ILC1 doświadczały cięższego przebiegu choroby, wyższych markerów zapalnych i większego wydzielania TNF przez komórki gamma-delta T — efekty, które można było złagodzić przez bezpośrednie zablokowanie TNF.
Co to oznacza dla przyszłych terapii
Łącząc te obserwacje, autorzy proponują oś „śledziona–tłuszcz brzuszny”: wkrótce po przedostaniu się bakterii do jamy brzusznej ILC1 opuszczają śledzionę, trafiają do tkanki tłuszczowej krezkowej, gdzie przekształcają się w komórki bogate w CD127 i PD-L1, które tłumią produkcję TNF przez komórki gamma-delta T. Zamiast podsycać ogień, te wyspecjalizowane ILC1 działają jako lokalni strażnicy pokoju, zapobiegając nadmiernemu zapaleniu i potencjalnie hamując postęp zapalenia otrzewnej do śmiertelnej sepsy. W dłuższej perspektywie leki, które wzmocnią lub naśladują ten regulacyjny obwód w tłuszczu brzusznym, mogłyby zaoferować nowy sposób leczenia ciężkich infekcji — strojąc odpowiedź immunologiczną tak, aby była wystarczająco silna, by zwalczać zarazki, ale nie na tyle intensywna, by zagrażać pacjentowi.
Cytowanie: Nagata, R., Akama, Y., Goncalves, P. et al. Acute peritonitis-induced adipose CD127+ ILC1s express PD-L1 and ameliorate inflammation in mice. Nat Commun 17, 2391 (2026). https://doi.org/10.1038/s41467-026-69100-0
Słowa kluczowe: zapalenie otrzewnej, wrodzone komórki limfoidalne, tkanka tłuszczowa krezkowa, regulacja odporności, sepsa