Clear Sky Science · pl
Strategia syntetyczna oparta na kombinatoryce do opracowywania nośników białek do edycji genomu ukierunkowanych na siatkówkę myszy
Nowa nadzieja w leczeniu dziedzicznego ślepnięcia
Wiele postaci dziedzicznego ślepnięcia zaczyna się od jednej wadliwej kopi genu w komórkach światłoczułych z tyłu oka. Nowoczesne narzędzia edycji genów, takie jak CRISPR, w zasadzie mogą poprawiać takie błędy, ale bezpieczne dostarczenie aparatu edytującego do właściwych komórek było poważną przeszkodą. W tym badaniu opisano nowy sposób transportu potężnych edytorów genów bezpośrednio do siatkówki myszy przy użyciu specjalnie zaprojektowanych cząstek przypominających tłuszcze, co stwarza perspektywę jednorazowych terapii przywracających wzrok u osób z genetycznymi chorobami oczu.
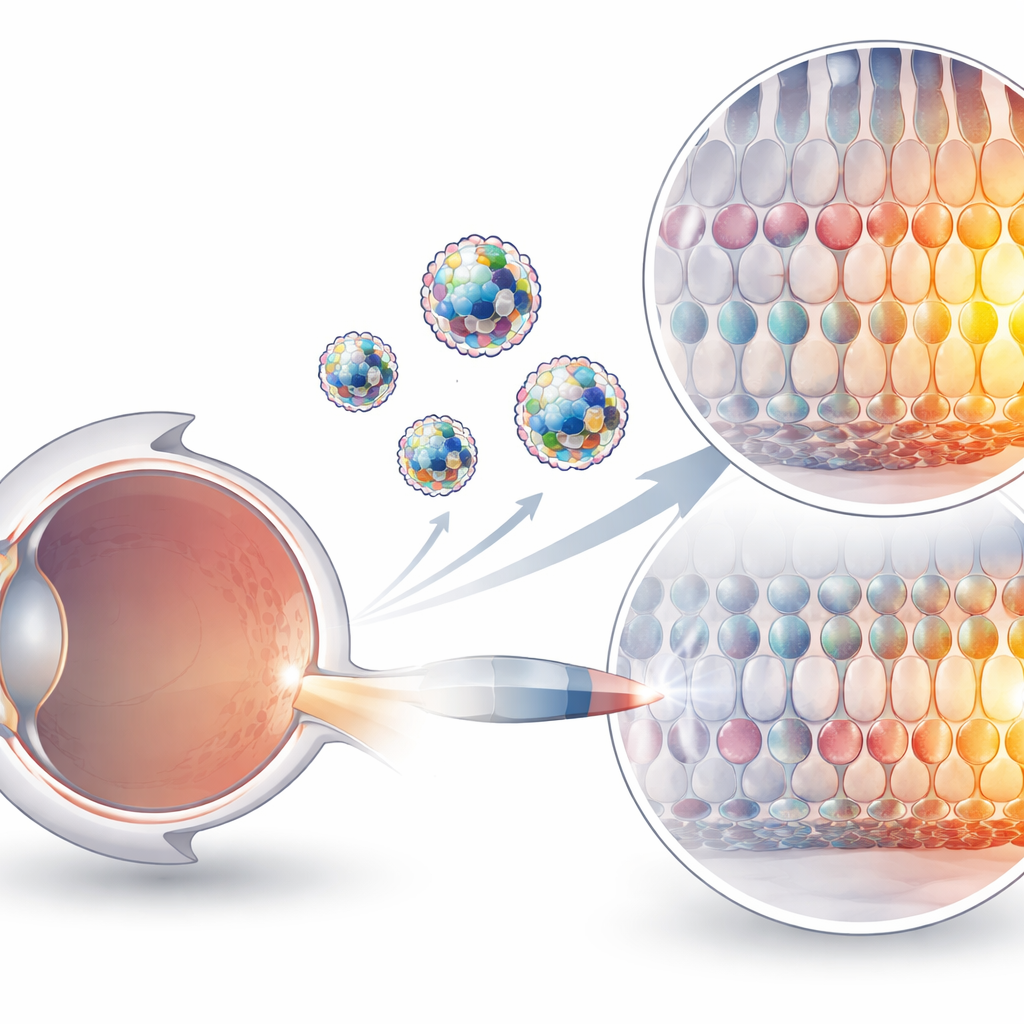
Dlaczego dostarczanie edytorów genów jest tak trudne
Narzędzia oparte na CRISPR potrafią dziś zmieniać pojedyncze znaki DNA bez przecinania obydwu nici, co czyni je atrakcyjnymi do leczenia chorób genetycznych. Jednak są to obszerne kompleksy białko–RNA, naładowane elektrycznie i kruche w organizmie. Obecne metody dostarczania opierają się głównie na zmodyfikowanych wirusach lub na cząstkach przenoszących genetyczne instrukcje dla edytora zamiast samego edytora. Wirusy mogą wywoływać reakcje immunologiczne i mają ścisłe ograniczenia rozmiaru, podczas gdy dostarczanie mRNA działa bardzo dobrze w wątrobie, ale pozostaje nieefektywne w wielu innych tkankach, w tym w oku. Bezpośrednie wstrzyknięcie wstępnie złożonych kompleksów białko–RNA jest koncepcyjnie prostsze i bezpieczniejsze, jednak brakowało dla nich odpowiedniego pojazdu, który pomógłby przekroczyć błony komórkowe i dotrzeć do celów.
Promotor białek zainspirowany barwnikiem
Naukowcy sięgnęli po niespodziewany punkt wyjścia: Coomassie Brilliant Blue, głęboko niebieski barwnik powszechnie używany w laboratoriach biologicznych i już dopuszczony do niektórych zabiegów okulistycznych. Ten barwnik mocno przywiera do wielu różnych białek. Zespół chemicznie połączył „główki” Coomassie z „ogonami” przypominającymi tłuszcze, tworząc rodzinę nowych cząsteczek zwanych lipidoidami. W wodzie lipidoidy mają tendencję do tworzenia skupisk, z oleistymi częściami schowanymi wewnątrz, a grupami Coomassie wystawionymi na zewnątrz, gdzie mogą łapać białka. Poprzez modyfikację długości, rozgałęzienia i ładunku ogonów, naukowcy zbudowali dziesiątki kandydackich związków zaprojektowanych tak, by wiązać białka edytujące geny z jednej strony i wchodzić w interakcje z błonami komórkowymi z drugiej.
Testowanie dostarczania białek do komórek oka
Aby sprawdzić, które projekty faktycznie działają, grupa najpierw użyła prostego białka testowego zwanego rekombinazą Cre, które przestawia genetyczny przełącznik z zielonego na czerwony lub z czerwonego na zielony we wkomponowanych komórkach i myszach. Kilka lipidoidów Coomassie skutecznie przenosiło Cre do hodowanych komórek, przekształcając duże odsetki komórek z zielonych na czerwone. Po wstrzyknięciu pod siatkówkę w myszach reporterowych wybrane związki wywołały uderzające zmiany barwy zarówno w warstwie barwnikowej wspierającej widzenie, jak i w światłoczułych fotoreceptorach, pokazując, że białka dotarły do tych komórek, które są najbardziej dotknięte w wielu chorobach prowadzących do ślepoty. Te wstępne eksperymenty ujawniły także, że subtelne zmiany w strukturze lipidoidu mogą przesunąć, które typy komórek są targetowane, co sugeruje, że przyszłe wersje mogłyby być dostrojone do konkretnych warstw siatkówki.
Wzmacnianie edycji genów i przywracanie wzroku
Następnie zespół załadował swój system adenozynowym edytorem bazowym, udoskonaloną odmianą CRISPR, która potrafi poprawić konkretną pojedynczą literę powodującą utratę wzroku u myszy rd12, modelu ciężkiej ślepoty dziecięcej. Sam kompleks białko–RNA edytora słabo przenikał do komórek. Jeden lipidoid, nazwany CBB11, poprawiał dostarczanie, ale miał tendencję do tworzenia kłaczków w roztworze. Aby go ustabilizować, badacze osadzili CBB11 w małych, dobrze zdefiniowanych liposomach — pustych kulach zbudowanych z kilku typów lipidów, w tym składników klinicznie stosowanych w szczepionkach mRNA. W tych formulacjach CBB11 na powierzchni liposomu chwytał część białkową edytora, podczas gdy inne lipidy pomagały wiązać przewodnik RNA, tworząc współpracującą powłokę, która utrzymywała cały kompleks na zewnętrznej części cząstki.
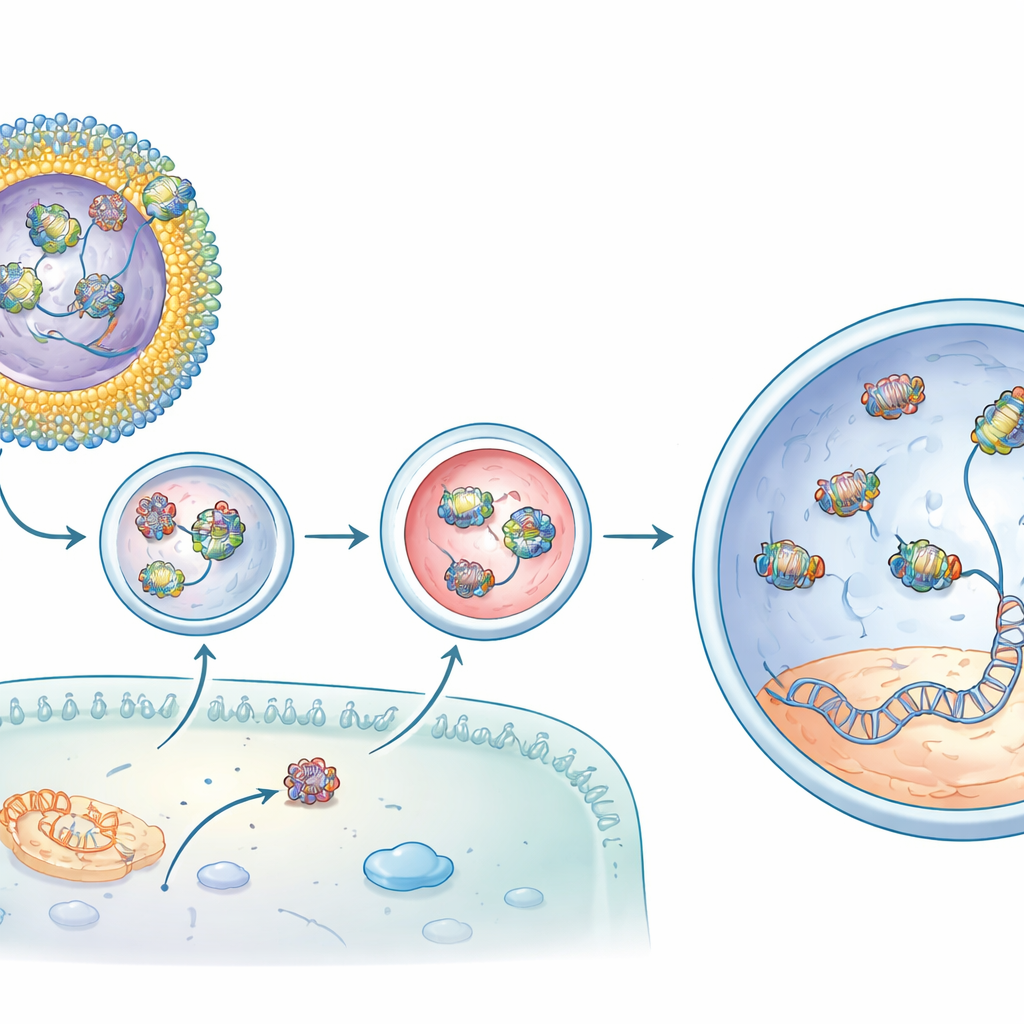
Od naprawy molekularnej do przywróconych reakcji na światło
Gdy te liposomy zawierające CBB11 przenoszące edytor bazowy zostały wstrzyknięte pod siatkówkę myszy rd12, wyniki były uderzające. W porównaniu z wstrzyknięciem samego edytora, zoptymalizowana formulacja zwiększyła pożądaną korekcję DNA w docelowym genie o ponad jeden rząd wielkości i wyprodukowała jeszcze wyższe poziomy skorygowanego mRNA. Analiza chemiczna wykazała odtworzenie światłoczułego barwnika siatkówki, którego brakowało w chorobie. Najbardziej przekonujące były zapisy elektryczne z oczu zwierząt, które pokazały, że ich komórki pręcikowe odzyskały dużą część zdolności reagowania na słabe światło — do około trzech czwartych sygnału normalnej myszy w najlepszych przypadkach. Zmiany poza celem w innych częściach genomu utrzymywały się na poziomie tła, co sugeruje, że edycja była zarówno silna, jak i precyzyjna.
Co to może znaczyć dla przyszłych terapii okulistycznych
Dla osoby niezwiązanej z dziedziną kluczowy wniosek jest taki, że autorzy zbudowali wielokrotnego użytku „autobus” transportowy dla białek edytujących geny, który działa bezpośrednio w żyjącym oku. Dekorując bezpieczne, przypominające szczepionki cząstki tłuszczowe barwnikiem chwytającym białka, stworzyli system, który może pochwycić różne edytory na swojej powierzchni, dostarczyć je do komórek siatkówki, skorygować mutacje wywołujące chorobę i mierzalnie przywrócić wzrok u myszy po jednorazowym zabiegu. Chociaż potrzeba więcej pracy, by w pełni ocenić bezpieczeństwo, poprawić celowanie i dostosować metodę do zastosowania u ludzi, ta platforma wskazuje drogę ku przyszłym jednorazowym precyzyjnym lekom na dziedziczne choroby siatkówki, a być może też inne schorzenia genetyczne, gdzie precyzyjna, miejscowa naprawa DNA może przesądzić o ślepocie lub wzroku.
Cytowanie: Zhang, J., Hołubowicz, R., Smidak, R. et al. A combinatorial synthetic strategy for developing genome-editing protein-delivery agents targeting mouse retina. Nat Commun 17, 2479 (2026). https://doi.org/10.1038/s41467-026-69077-w
Słowa kluczowe: terapia genowa siatkówki, edytowanie bazami CRISPR, liposomy, dostarczanie białek, dziedziczne ślepnięcie