Clear Sky Science · pl
Wgląd w strukturę i modulację ludzkiego TWIK-2
Dlaczego ta maleńka bramka w naszych komórkach ma znaczenie
Głęboko w naszych komórkach mikroskopijne bramki zbudowane z białek kontrolują przepływ naładowanych atomów, kształtując sposób, w jaki nerwy wyładowują się, jak naczynia krwionośne się obkurczają i jak reaguje nasz układ odpornościowy. Jedna z takich bramek, nazwana TWIK-2, została powiązana z nadciśnieniem płucnym i szkodliwym zapaleniem, lecz do tej pory niewiele wiedziano o jej budowie ani o tym, jak kontrolować ją lekami. To badanie odsłania szczegółową strukturę ludzkiego TWIK-2, pokazuje jego właściwości elektryczne i wskazuje, jak można go celować przy opracowywaniu nowych leków przeciwzapalnych.
Cichy kanał o dużych implikacjach zdrowotnych
TWIK-2 należy do dużej rodziny kanałów potasowych typu „leak”, które pomagają ustalić napięcie spoczynkowe komórek, umożliwiając jonów potasu przemieszczanie się przez błonę komórkową. Podczas gdy inne człony tej rodziny, takie jak kanały TREK i TASK, były intensywnie badane i powiązane z bólem i nastrojem, TWIK-2 pozostawał w cieniu, ponieważ trudno go rejestrować i słabo się eksprymuje w standardowych systemach laboratoryjnych. Tym niemniej badania na zwierzętach i komórkach łączyły TWIK-2 z nadciśnieniem płucnym, ostrym uszkodzeniem płuc, utratą słuchu oraz aktywacją kompleksu immunologicznego NLRP3, który napędza szkodliwe zapalenie w sepsie i innych chorobach. Zrozumienie działania TWIK-2 jest zatem kluczowe zarówno dla podstawowej biologii, jak i dla projektowania celowanych terapii.
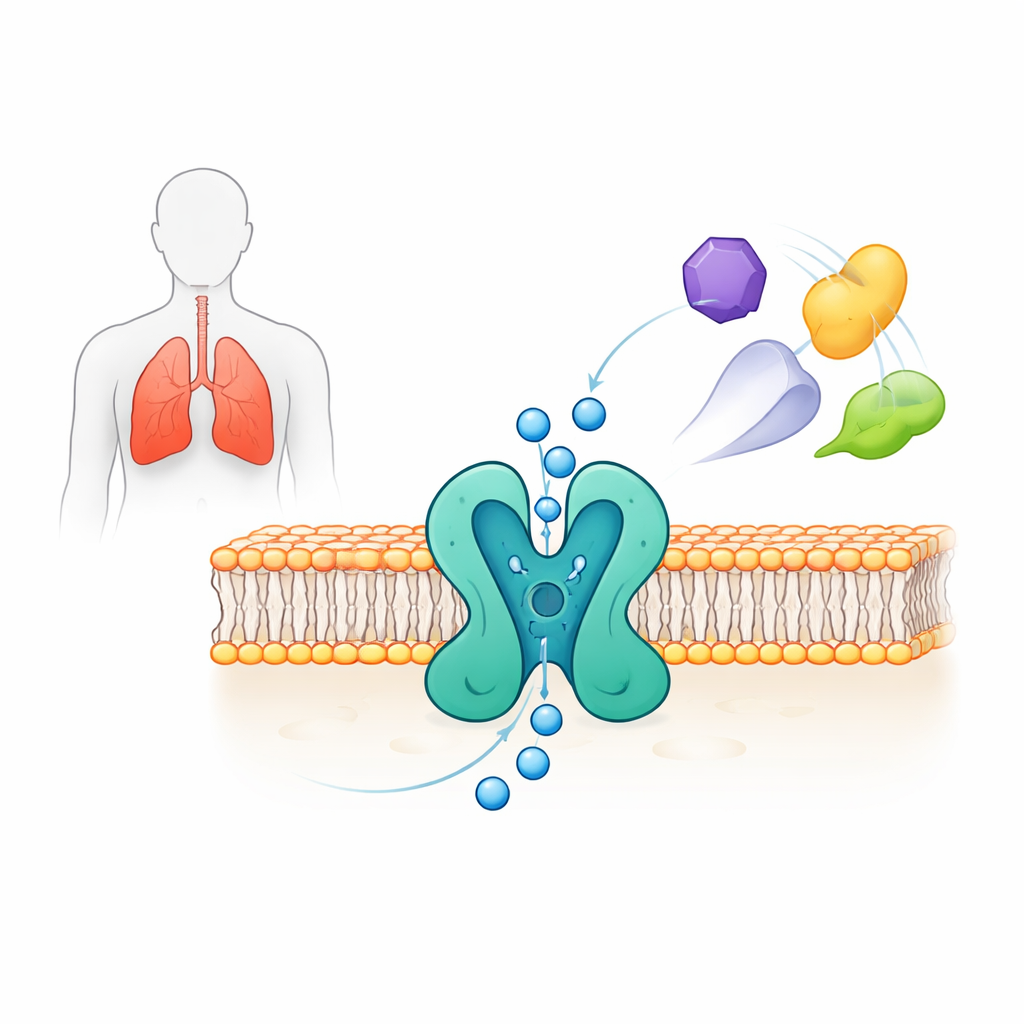
Widzieć bramkę w skali atomowej
Naukowcy wyeksprymowali pełnobiałkowy ludzki TWIK-2 w liniach komórek ludzkich i zastosowali metodę cryo–elektronowej mikroskopii pojedynczych cząstek, aby określić jego trójwymiarową strukturę z rozdzielczością około 3,7 ångströma. Kanał tworzy dwu‑częściowy kompleks, który razem tworzy centralny por, przez który przepływają jony potasu. Każda połowa zawiera cztery segmenty przecinające błonę oraz dwie „helisy porowe”, które formują wąski region zwany filtrem selektywności, gdzie potas jest rozróżniany od innych jonów. Nad porem dwie łukowate struktury „czapki” tworzą dwie odrębne ścieżki wejściowe dla jonów z zewnątrz komórki. Struktura ujawnia także subtelne asymetrie między dwiema stronami poru, dając TWIK-2 pseudo‑czteroczęściowe uporządkowanie — cechę charakterystyczną tej rodziny kanałów.
Ukryte lipidy i precyzyjnie dostrojona ścieżka jonowa
Wzdłuż ścieżki przewodzenia jonów zespół namierzył, jak jony potasu przemieszczają się z wnętrza komórki, przez hydrofobowy „mankiet”, w górę przez filtr selektywności i na zewnątrz pod czapką. Najwęższy punkt wciąż jest wystarczająco szeroki, by potas mógł przechodzić pojedynczym szeregiem. Chociaż białko oczyszczono bez dodatku molekuł tłuszczowych, mapy cryo‑EM wykazały rurkowate gęstości umieszczone w pobliżu dolnej części poru oraz w bocznych kieszeniach między helisami. Prawdopodobnie reprezentują one lipidy lub ogony detergentów, które przylgnęły do TWIK-2 podczas oczyszczania, sugerując, że naturalne tłuszcze błonowe mogą zagnieżdżać się w tych rowkach i subtelnie przesuwać kształt pobliskich helis. Takie przesunięcia, szczególnie w helisie zwanej M4 i w pętlach filtra selektywności, uważa się za element regulujący, czy kanał jest otwarty, zamknięty czy gdzieś pomiędzy.
Badanie bramki za pomocą mutacji i blokerów
Aby powiązać strukturę z funkcją, naukowcy wykorzystali zautomatyzowany system patch‑clamp do pomiaru prądów z komórek eksprymujących zarówno normalny TWIK-2, jak i wersje z konkretnymi zmianami aminokwasowymi. Stwierdzili, że TWIK-2 wykazuje silną zależność od napięcia, ale w przeciwieństwie do swego krewnego TWIK-1 jest w dużej mierze niewrażliwy na zmiany zewnętrznej kwasowości. Mutacje przy dwóch zachowanych resztach treoniny u podstawy filtra selektywności sprawiły, że kanał otwierał się szybciej i przewodził większy prąd, co sugeruje, że te miejsca działają jak kluczowe zawiasy stabilizujące stan zamknięty. Zmiany na wejściu i wyjściu poru zmieniały szybkość, z jaką kanał się włącza i wyłącza, ujawniając, jak precyzyjnie kontrolowana jest ścieżka jonowa. Zespół przetestował też cztery znane małe molekuły modulujące powiązane kanały. Dwie z nich, ML365 i NPBA, silnie blokowały TWIK-2, podczas gdy pozostałe nie miały efektu. Porównując, jak różne mutacje zmieniały czułość na leki, autorzy wnioskują, że te związki prawdopodobnie wiążą się tuż pod filtrem selektywności i w pobliskich kieszeniach, a różne leki korzystają z nakładających się, lecz odrębnych trybów wiązania.
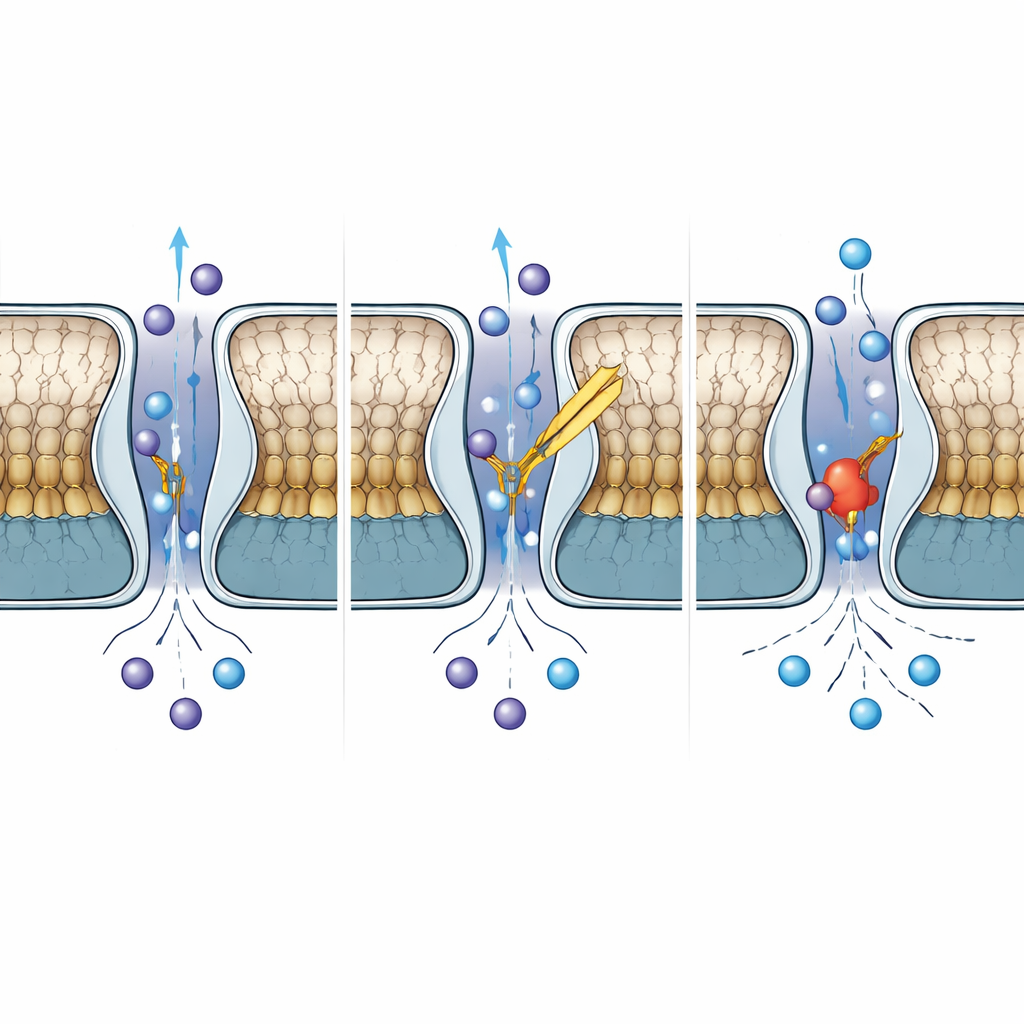
Jak TWIK-2 różni się od bliskich krewnych
Chociaż TWIK-2 dzieli ponad połowę sekwencji z TWIK-1, ich zachowanie różni się w istotny sposób. Porównując TWIK-2 z opublikowanymi strukturami TWIK-1 w pH neutralnym i kwaśnym, autorzy stwierdzili, że region czapki TWIK-2 przypomina formę TWIK-1 zahamowaną przez kwas, podczas gdy jego filtr selektywności pozostaje ułożony jak w formie przewodzącej, otwartej. Pojedyncza histydyna w TWIK-1, znana z wyczuwania protonów i wpadająca do poru, by blokować przepływ jonów przy niskim pH, jest w TWIK-2 zastąpiona tyrozyną. Nawet gdy zespół przywrócił histydynę w tym miejscu w TWIK-2, kanał nie stał się wrażliwy na pH, co pokazuje, że kontrola pH w tych kanałach opiera się na szerszej sieci reszt i ruchów, a nie tylko jednym aminokwasowym „włączniku”.
Od struktury do przyszłych terapii
Podsumowując, praca ta dostarcza pierwszego obrazu ludzkiego TWIK-2 w wysokiej rozdzielczości i mapuje, jak konkretne cechy strukturalne kształtują przepływ jonów, reakcję na napięcie oraz podatność na małe blokerowe molekuły. Odkrycie, że istniejące związki mogą selektywnie hamować TWIK-2, w połączeniu z solidną zautomatyzowaną platformą przesiewową, otwiera drogę do szeroko zakrojonych poszukiwań bezpieczniejszych i bardziej efektywnych leków. Ponieważ aktywność TWIK-2 w komórkach odpornościowych została powiązana z niekontrolowanym zapaleniem, zwłaszcza w płucach, takie leki mogłyby posłużyć jako podstawa nowych terapii przeciwzapalnych działających poprzez delikatne „przyciszanie” tej maleńkiej, ale potężnej bramki w błonie komórkowej.
Cytowanie: Ma, Q., Hernandez, C.C., Navratna, V. et al. Insights into the structure and modulation of human TWIK-2. Nat Commun 17, 2201 (2026). https://doi.org/10.1038/s41467-026-69072-1
Słowa kluczowe: kanał potasowy TWIK-2, kanały K2P z dwoma porami, struktura kanału jonowego metodą cryo-EM, modulatory kanałów potasowych, zapalenie płuc