Clear Sky Science · pl
Przestrzenna proteomika pojedynczych komórek w okrężnicy i modele mysie łączą dysfunkcję mitochondriów z niedoborem plazmatycznych komórek wydzielających dimerowe IgA w chorobie Leśniowskiego–Crohna
Dlaczego przeciwciała jelitowe mają znaczenie w chorobie Crohna
Choroba Crohna jest najbardziej znana z bolesnych zaostrzeń zapalenia jelit, lecz na długo przed pojawieniem się objawów mogą zachodzić subtelne zmiany w sposobie, w jaki układ odpornościowy chroni jelito. Badanie stawia proste, lecz istotne pytanie: czy osoby z chorobą Crohna w remisji wciąż wytwarzają odpowiedni rodzaj przeciwciał, który utrzymuje mikroby jelitowe w spokoju? Łącząc próbki pacjentów, profilowanie tkanki o wysokiej rozdzielczości, analizy metaboliczne i modele mysie, autorzy ujawniają ukrytą słabość w osłonie przeciwciał jelita związaną z produkcją energii w komórkach.
Ochronna powłoka, która okazuje się niewystarczająca
Nasze jelita polegają na specjalnym przeciwciele zwanym wydzielniczym IgA, które jest uwalniane do śluzu wyściełającego jelito. IgA, zwłaszcza w swojej „podwójnej” postaci zwanej dimerowym IgA, pokrywa bakterie i inne mikroby, pomagając utrzymać je przy powierzchni zamiast wnikać głębiej w tkankę. W tej pracy badacze analizowali biopsje okrężnicy, krew i stolec osób z chorobą Crohna w remisji oraz od kontrolnych osób bez stanu zapalnego. W tkance okrężnicy pacjenci z Crohnem mieli faktycznie więcej komórek B i komórek produkujących przeciwciała oraz wyższe poziomy genów i białek związanych z IgA. Jednak gdy zespół zmierzył IgA w kale, uzyskano odwrotny wynik niż można by oczekiwać: wydzielnicze IgA w świetle jelita było istotnie zmniejszone. 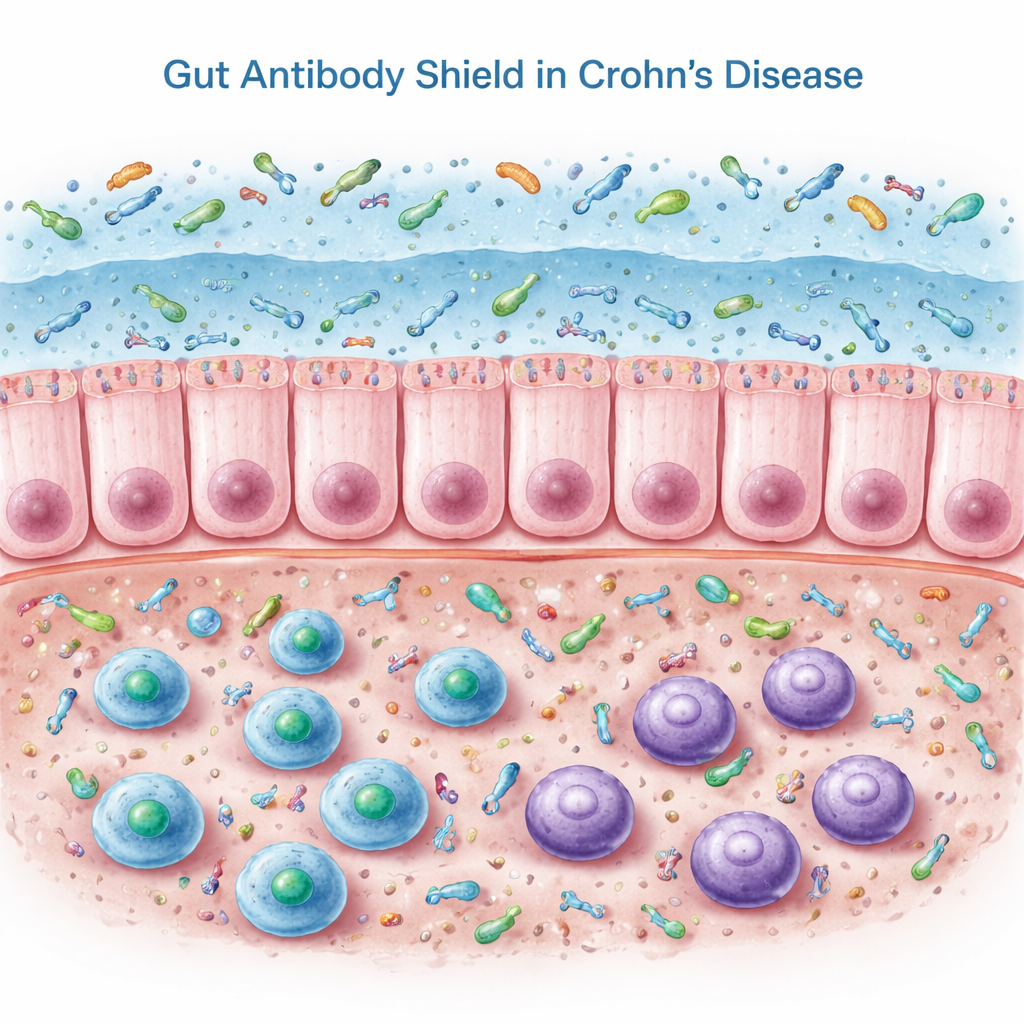
Zatrzymane w połowie: komórki produkujące przeciwciała, które nie dojrzewają w pełni
Komórki wydzielające IgA — komórki plazmatyczne — zwykle dojrzewają przez określone etapy, od aktywnych, krótkotrwałych prekursorów do długowiecznych specjalistów, którzy produkują duże ilości dimerowego IgA. Używając przestrzennej proteomiki pojedynczych komórek, która mapuje wiele białek na poszczególnych komórkach w nieuszkodzonej tkance, autorzy mogli odróżnić podzbiory niedojrzałych i w pełni dojrzałych komórek plazmatycznych w okrężnicy. U pacjentów z Crohnem zaobserwowano rozszerzenie populacji wczesnych plazmablastów i niedojrzałych komórek plazmatycznych, podczas gdy najbardziej dojrzałe komórki plazmatyczne były zmniejszone. Analizy biochemiczne potwierdziły, że stosunek dimerowego do monomerowego IgA był niższy w okrężnicach chorych na Crohna, a każda komórka produkująca przeciwciała wydzielała średnio mniej dimerowego IgA. Gdy zespół wyizolował przełączone pamięciowe komórki B z okrężnicy i pobudził je do przemiany w komórki plazmatyczne w hodowli, komórki pochodzące od pacjentów z Crohnem nie zdołały zwiększyć ekspresji kluczowych markerów dojrzewania i produkowały mniej całkowitego oraz dimerowego IgA, mimo że produkcja IgG pozostawała w dużej mierze prawidłowa. To sugeruje wewnętrzną blokadę programu dojrzewania specyficznie dla komórek plazmatycznych wydzielających IgA.
Fabryki energii pod obciążeniem
Aby zrozumieć, co stoi za tą blokadą, badacze zwrócili się ku metabolizmowi komórek. Stwierdzili, że komórki plazmatyczne w tkance Crohna wykazywały wyższy poziom CD38 — enzymu na powierzchni komórki, który zużywa NAD+, centralny nośnik paliwa dla produkcji energii mitochondrialnej. Geny zaangażowane w mitochondrialną fosforylację oksydacyjną — główny sposób, w jaki komórki generują ATP z substancji odżywczych — były szeroko zredukowane w tkance okrężnicy pacjentów z Crohnem, a wzory metabolitów w osoczu wskazywały na przesunięcie z dala od wydajnego oddychania mitochondrialnego. W eksperymentach ex vivo komórki plazmatyczne pochodzące od chorych na Crohna zużywały mało glukozy, uwalniały mniej mleczanu i wykazywały zmniejszoną ekspresję genów mitochondrialnych, co wskazuje na metabolicznie „quiescencyjny” lub osłabiony stan. 
Wskazówki z modeli mysich i diety
Modele mysie dostarczyły dalszych dowodów. Myszy niosące określoną mutację mitochondrialną, która upośledza enzymatyczny kompleks V produkujący ATP, miały mniej dojrzałych komórek plazmatycznych w związanych z jelitem tkankach limfatycznych, zmniejszoną ekspresję markerów komórek plazmatycznych w okrężnicy oraz niższe poziomy zarówno monomerowego, jak i dimerowego IgA w tkance okrężnicy. Natomiast zdrowe myszy karmione dietą bezglukozową o wysokiej zawartości białka, która zwiększa aktywność mitochondrialną w okrężnicy, rozwinęły więcej komórek produkujących IgA i wyższe stężenia IgA w kale. Te komplementarne eksperymenty wiążą wydajność mitochondriów bezpośrednio ze zdolnością komórek plazmatycznych do dojrzewania i utrzymania silnej bariery IgA w jelicie.
Co to oznacza dla osób z chorobą Crohna
Razem badanie kreśli obraz, w którym choroba Crohna, nawet podczas remisji klinicznej, wiąże się z nadmiarem niedojrzałych komórek linii B w okrężnicy i niedoborem w pełni dojrzałych, energochłonnych komórek plazmatycznych wydzielających dimerowe IgA do śluzu. Jelito może wyglądać na spokojne, ale jego osłona przeciwciałowa jest cieńsza i mniej skuteczna. Łącząc ten defekt z dysfunkcją mitochondrialną — częściowo napędzaną prawdopodobnie przez nasilone działanie CD38 — praca sugeruje, że terapie mające na celu przywrócenie metabolizmu energetycznego komórek lub subtelną modulację sygnalizacji CD38 mogłyby pomóc odbudować śluzówkową barierę IgA. Dla pacjentów otwiera to perspektywę, że przyszłe leczenie mogłoby nie tylko tłumić zapalenie, gdy się pojawi, lecz także wzmacniać pierwszorzędową obronę przeciwciałową jelita, aby zapobiegać występowaniu zaostrzeń.
Cytowanie: Raschdorf, A., de Almeida, L.N., Solbach, P. et al. Colonic spatial single-cell proteomics and murine models link mitochondrial dysfunction to dimeric IgA-secreting plasma cell deficiency in Crohn’s disease. Nat Commun 17, 1590 (2026). https://doi.org/10.1038/s41467-026-69069-w
Słowa kluczowe: Choroba Leśniowskiego–Crohna, przeciwciała jelitowe, IgA, mitochondria, odporność jelitowa