Clear Sky Science · pl
FLASH-MM: szybka i skalowalna analiza różnicowej ekspresji w pojedynczych komórkach z użyciem liniowych modeli efektów mieszanych
Dlaczego maleńkie komórki potrzebują dużej mocy obliczeniowej
Współczesna biologia potrafi już odczytywać aktywność tysięcy genów w setkach tysięcy pojedynczych komórek jednocześnie. Ten obraz na poziomie pojedynczych komórek obiecuje głębsze zrozumienie, jak organizm walczy z infekcjami, różnice między płciami czy rozwój chorób. Przekształcanie jednak tych olbrzymich, hałaśliwych zbiorów danych w wiarygodne odkrycia jest powolne, a przy prostym podejściu może wprowadzać w błąd. Artykuł przedstawia FLASH-MM — nowy sposób przetwarzania danych pojedynczych komórek, który zachowuje rzetelność statystyczną i jednocześnie przyspiesza obliczenia do skali dzisiejszych największych badań.
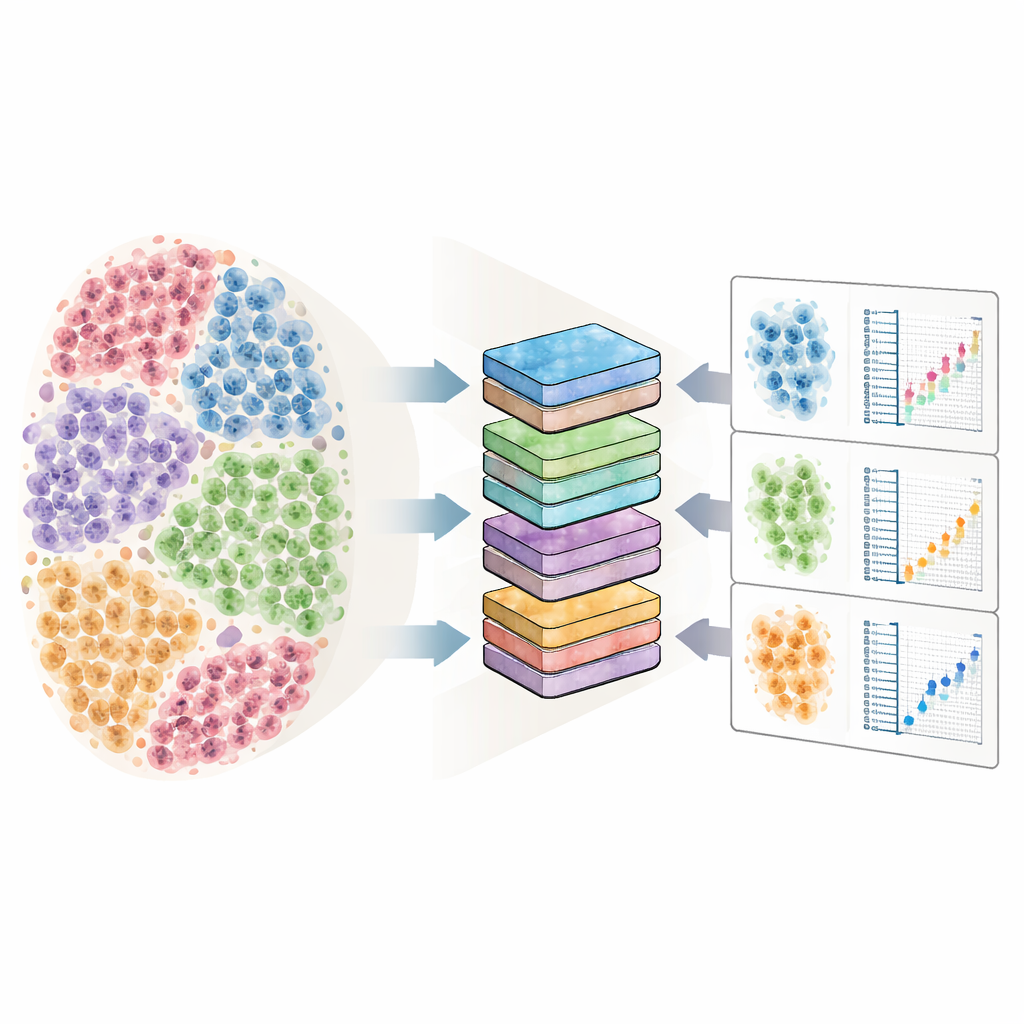
Wyzwanie hałaśliwych, zatłoczonych danych komórkowych
Sequencing RNA pojedynczych komórek mierzy, które geny są „włączone” lub „wyłączone” w każdej komórce, w wielu osobach i warunkach. Komórki od tej samej osoby często wyglądają podobnie, bo dzielą geny i historię życiową, podczas gdy między ludźmi występują duże różnice. To tworzy warstwową strukturę danych: wiele komórek w ramach każdej osoby i wiele osób w ramach danego warunku, np. chory vs. zdrowy. Ignorowanie tych relacji sprawia, że standardowe metody mogą błędnie oznaczać tysiące genów jako zmienione tylko dlatego, że traktują każdą komórkę jako niezależny punkt danych. Równocześnie zbiory danych pojedynczych komórek gwałtownie urósł — obejmują teraz setki osób i do milionów komórek — co przeciąża konwencjonalne narzędzia statystyczne pod względem czasu i pamięci.
Mądrzejszy sposób modelowania osób i komórek
Aby poradzić sobie z tymi złożonościami, statystycy często stosują liniowe modele efektów mieszanych, które wyraźnie rozdzielają stałe różnice między warunkami (np. zakażenie gruźlicą czy płeć) od losowych różnic między osobami. W teorii te modele są idealne dla badań pojedynczych komórek, ponieważ uwzględniają zarówno podobieństwa między komórkami tej samej osoby, jak i zmienność między osobami. W praktyce jednak szeroko używane oprogramowanie do takich modeli znacząco zwalnia lub kończy się brakiem pamięci przy dużych eksperymentach pojedynczych komórek. Badacze często więc uciekają się do uproszczeń, np. uśredniania zliczeń po wszystkich komórkach tego samego typu w obrębie osoby, co traci wiele szczegółowej informacji komórka-po-komórce, która czyni dane pojedynczych komórek wartościowymi.
Jak FLASH-MM przyspiesza ciężkie obliczenia
FLASH-MM zachowuje zalety modeli efektów mieszanych, jednocześnie przebudowując sposób wykonywania obliczeń. Zamiast wielokrotnego przetwarzania gigantycznych tabel pomiarów komórka-na-gen, FLASH-MM najpierw destyluje każdy zbiór danych do zwartego zestawu liczb podsumowujących, które opisują, jak komórki odnoszą się do znanych cech, takich jak wielkość biblioteki, typ komórki, leczenie czy dawca. Główny algorytm pracuje potem wyłącznie na tych mniejszych macierzach, zmniejszając obciążenie obliczeniowe z zależności od liczby komórek do zależności od znacznie mniejszej liczby składników modelu. Autorzy także dopracowują sposób reprezentacji zmienności modelu tak, by standardowe testy statystyczne pozostawały ważne, umożliwiając użycie prostych statystyk t i z do oceny zarówno głównych efektów zainteresowania, jak i dodatkowej wartości uwzględnienia zmienności międzyosobniczej. Badania symulacyjne na realistycznych danych sztucznych pokazują, że wyniki FLASH-MM zgadzają się z oprogramowaniem wzorcowym do kilku miejsc po przecinku, jednocześnie działając od około 50 do 140 razy szybciej i zużywając znacznie mniej pamięci.
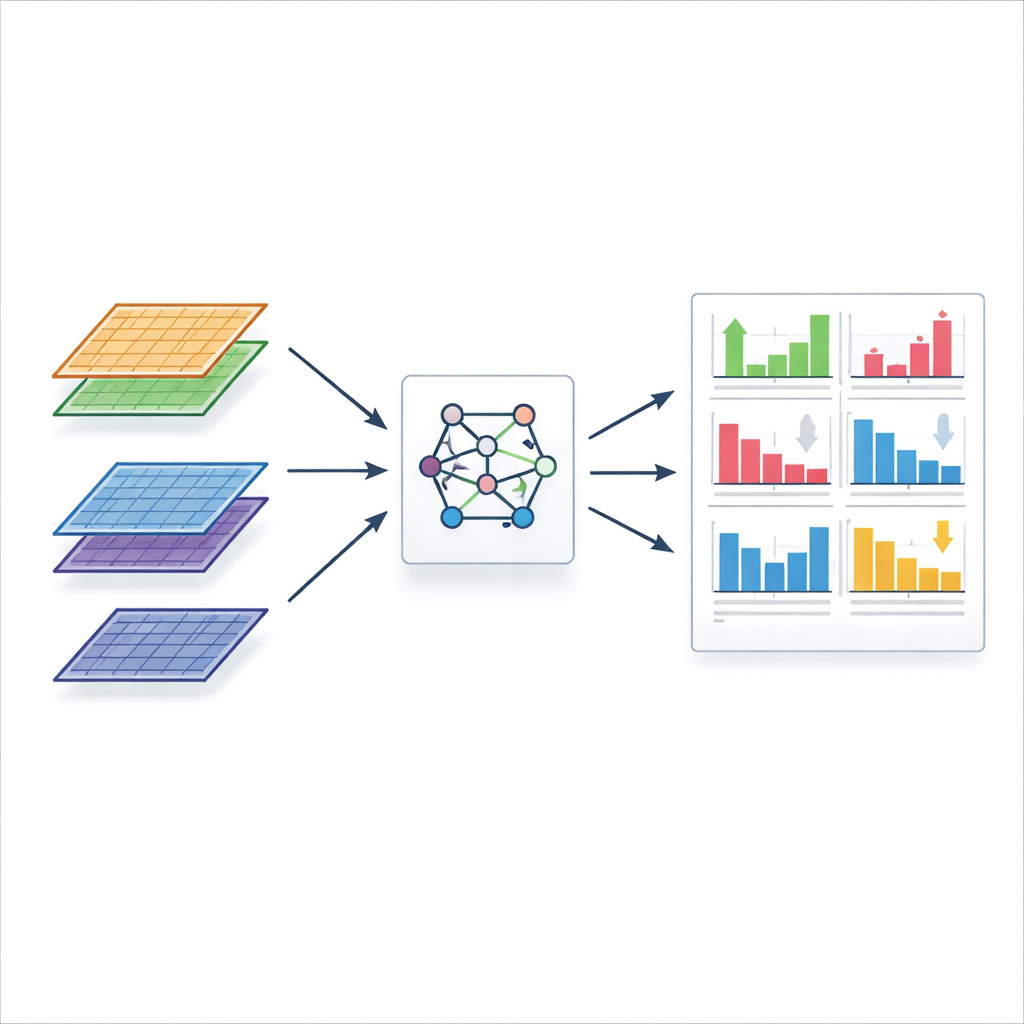
Zastosowanie metody w rzeczywistych tkankach
Aby pokazać praktyczny wpływ, zespół zastosował FLASH-MM do dwóch wymagających zbiorów danych pojedynczych komórek. W mapie ponad 27 000 zdrowych ludzkich komórek nerkowych od 19 dawców FLASH-MM szukał różnic w aktywności genów między dawcami mężczyznami i kobietami w ramach każdego typu komórki, traktując każdą osobę jako czynnik losowy, by uniknąć nadmiernej pewności wyników. Najmocniejsze wzorce związane z płcią znaleziono w konkretnym typie komórek kanalików nerkowych, gdzie komórki męskie preferowały szlaki związane z obsługą kwasów i ciśnieniem krwi, a komórki żeńskie wykazywały wzbogacenie dla procesów sygnalizacji i recyklingu receptorów. FLASH-MM zakończył tę analizę w około minutę, w porównaniu z prawie dwoma godzinami dla standardowego narzędzia. Metoda przeanalizowała także około pół miliona pamięciowych komórek T od 259 osób w kohorcie gruźlicy, identyfikując zbiory genów i szlaków powiązanych ze stanem choroby w różnych aktywowanych stanach komórek T. W tym przypadku FLASH-MM zakończył pracę w mniej niż półtorej godziny, w porównaniu z ponad dwoma dniami dla tradycyjnego podejścia.
Co to oznacza dla przyszłych badań komórka-po-komórce
Z perspektywy laika przekaz jest taki, że możemy teraz lepiej wykorzystać napływ danych pojedynczych komórek bez dystorsji wyników. FLASH-MM śledzi, które komórki pochodzą od których osób i w jakim warunku, dzięki czemu wykryte zmiany w genach mają większe prawdopodobieństwo odzwierciedlania rzeczywistej biologii, a nie artefaktów próbkowania czy partii. Jednocześnie oszczędne obliczenia sprawiają, że możliwe jest analizowanie setek tysięcy komórek na standardowych komputerach, otwierając drogę do ambitniejszych badań subtelnych sygnałów chorobowych, różnic płciowych i rzadkich stanów komórkowych. Ponieważ podejście jest ogólne i dostępne w R i Pythonie, można je rozszerzać na nowe technologie, takie jak przestrzenne mapowanie genów i wielowarstwowe pomiary molekularne, pomagając badaczom przekształcać ogromne zbiory danych na poziomie komórkowym w solidne, klinicznie istotne wnioski.
Cytowanie: Xu, C., Pouyabahar, D., Voisin, V. et al. FLASH-MM: fast and scalable single-cell differential expression analysis using linear mixed-effects models. Nat Commun 17, 2384 (2026). https://doi.org/10.1038/s41467-026-69063-2
Słowa kluczowe: sekwencjonowanie RNA pojedynczych komórek, różnicowa ekspresja, liniowe modele efektów mieszanych, genomika statystyczna, biologia obliczeniowa