Clear Sky Science · pl
Myofibroblasty Tenascin C+ nasilają neointymalne przerosłe przebudowanie naczyń poprzez propagację interakcji nerwów i makrofagów u myszy
Kiedy naczynia krwionośne goją się w niewłaściwy sposób
Zabiegi przywracające przepływ w zatkanych tętnicach, takie jak angioplastyka czy pomostowanie, ratują niezliczone życie. Często jednak pozostawiają ukryty problem: z czasem leczone naczynie może się zbliznowacić do środka, ponownie zwężając światło i narażając pacjentów. Badanie na myszach ujawnia nieoczekiwaną trójstronną rozmowę między komórkami podporowymi, nerwami i komórkami odpornościowymi w ścianie naczynia, która napędza to szkodliwe „nadgojenie”, oraz wskazuje cząsteczkę o nazwie tenascyna C jako obiecujący cel przerwania tego cyklu.
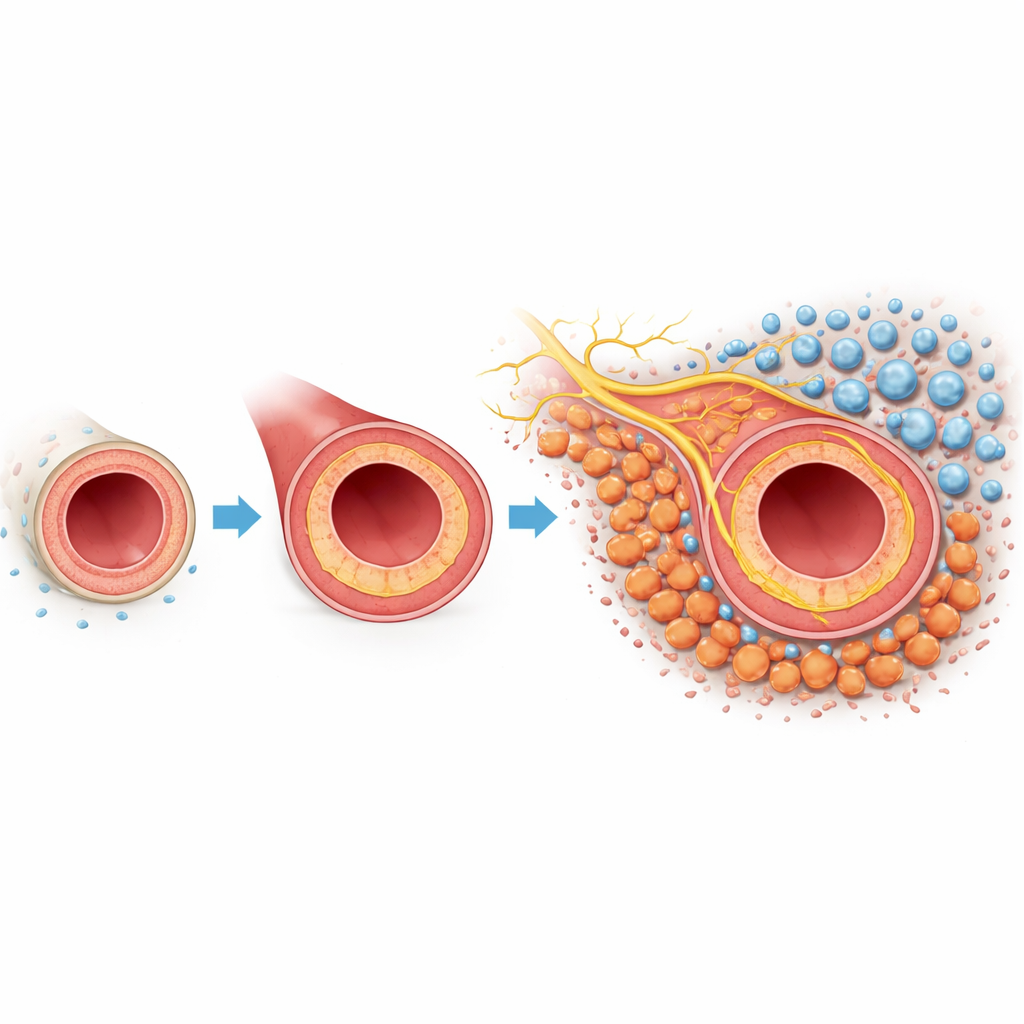
Bliższe spojrzenie na problem bliznowacenia w tętnicach
Kiedy tętnica ulega urazowi lub jest manipulowana podczas operacji, wewnętrzna wyściółka może odrastać zbyt agresywnie. Ten wzrost do wewnątrz, zwany neointymalnym przerostem, pogrubia ścianę naczynia i zmniejsza światło, którym płynie krew. Najbardziej zewnętrzna warstwa naczynia, przydanka, zawiera fibroblasty — komórki podporowe, które zwykle utrzymują strukturę naczynia. W tym modelu myszy, gdzie tętnica szyjna była częściowo związana, aby naśladować uraz, badacze zastosowali profilowanie genetyczne pojedynczych komórek i mapowanie przestrzenne, aby skatalogować wszystkie główne typy komórek zaangażowane w proces. Stwierdzili, że fibroblasty były szczególnie liczne i znacznie zmieniały swoje zachowanie po urazie, co sugeruje, że te komórki mogą być kluczowymi uczestnikami odpowiedzi bliznowatej.
Pojawienie się komórek bliznowotwórczych z tenascyną C
Zagłębiając się w populację fibroblastów, zespół odkrył wyraźną podgrupę, która pojawiła się dopiero po urazie. Komórki te nosiły cechy miofibroblastów — wysokie poziomy kurczliwego białka α-aktyny mięśni gładkich oraz inny marker zwany periostyną — co wskazywało, że przeszły w tryb tworzenia blizn. Co istotne, ta podgrupa produkowała duże ilości tenascyny C, białka macierzy zwykle rzadkiego w zdrowych tkankach dorosłych, ale obfitego w chorobach i podczas naprawy tkanek. Eksperymenty laboratoryjne wykazały, że wystawienie normalnych fibroblastów przydanki na transformujący czynnik wzrostu beta lub dodatkową tenascynę C skłaniało je do przejścia w te tenascyna C–pozytywne miofibroblasty. Komórki te następnie wydzielały jeszcze więcej tenascyny C, tworząc samonapędzającą się pętlę przez specyficzną parę receptorów powierzchniowych, integrynę αvβ1, co stopniowo powiększało populację komórek tworzących blizny.
Nerwy i komórki odpornościowe wkraczają do sąsiedztwa
Historia nie zakończyła się na utworzeniu blizny. Dzięki obrazowaniu 3D całych preparatów i transkryptomice przestrzennej badacze zaobserwowali, że miofibroblasty bogate w tenascynę C skupiały się w pobliżu wyrastających włókien nerwowych oraz komórek odpornościowych zwanych makrofagami w zewnętrznej warstwie naczynia. Uszkodzone tętnice wykazywały gęste, splątane nerwy czuciowe i więcej struktur przypominających synapsy niż normalnie, zarówno u myszy, jak i w próbkach ludzkich tętnic z neointymalnym przerostem. Makrofagi w tych regionach nosiły sygnaturę zapalną, produkując cząsteczki takie jak IL-1β i TGF-β1, które mogą dodatkowo napędzać bliznowacenie. Dane wspólnie rysują obraz przeorganizowanego mikrośrodowiska, w którym komórki bliznotwórcze, nerwy i makrofagi fizycznie się przenikają i wzajemnie na siebie oddziałują.
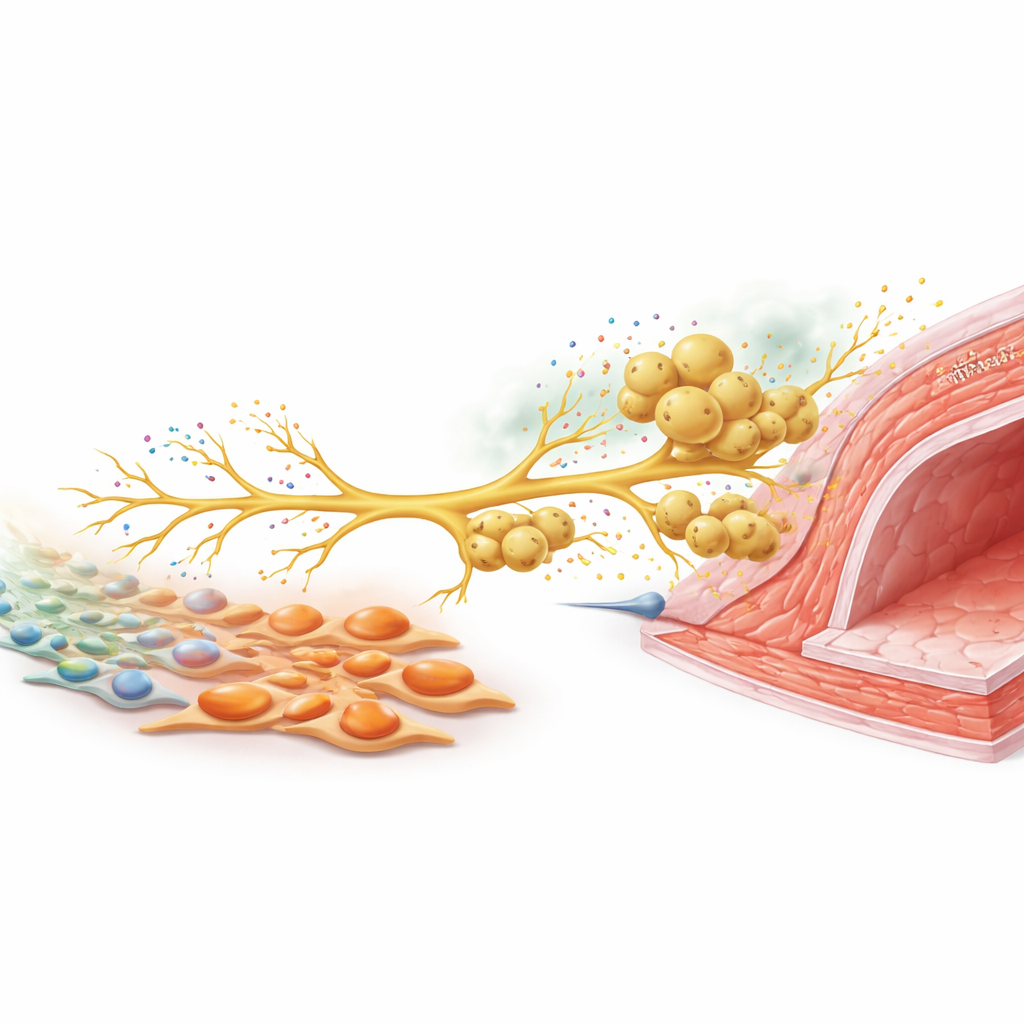
Sygnał nerwowy, który ściąga kolejnych obrońców
Aby zrozumieć, jak te typy komórek komunikują się, zespół skupił się na nerwach czuciowych wyczuwających uszkodzenia. W hodowli miofibroblasty bogate w tenascynę C zwiększały wzrost włókien nerwowych z neuronów zwojów korzeni grzbietowych. U uszkodzonych myszy neurony te zwiększały produkcję CCL2, sygnału chemicznego dobrze znanego z przyciągania makrofagów. Gdy neurony i makrofagi hodowano razem, makrofagi migrowały wzdłuż rosnących włókien nerwowych, podobnie jak obserwowano je wokół tętnic in vivo. Wyciszenie CCL2 w neuronach znacząco zmniejszyło rekrutację makrofagów. U zwierząt zmniejszenie aktywności nerwów czuciowych za pomocą toksyny lub selektywne usunięcie tenascyny C tylko w fibroblastach obniżało gęstość nerwów, poziomy CCL2, gromadzenie makrofagów i ostatecznie pogrubienie ściany naczynia. Połączenie obu interwencji nie dawało dodatkowej korzyści, co sugeruje, że działają wzdłuż tej samej ścieżki.
Dlaczego ta nowa ścieżka ma znaczenie
Podsumowując, wyniki ujawniają błędne koło: uraz skłania fibroblasty do przekształcenia się w miofibroblasty produkujące tenascynę C; komórki te przebudowują macierz i stymulują nerwy czuciowe; aktywowane nerwy uwalniają CCL2, który przyciąga makrofagi; a makrofagi wydzielają czynniki zapalne i włókniste, które pogłębiają bliznowacenie i zwężają tętnicę. Identyfikując tenascynę C i jej osię nerw–makrofag jako centralnych sprawców tej pętli, praca sugeruje, że terapie celujące w tę cząsteczkę lub jej partnerskie szlaki sygnałowe mogłyby pomóc utrzymać udrożnione naczynia przez dłuższy czas, oferując pacjentom trwalszą ochronę po zabiegach kardiologicznych.
Cytowanie: Tong, X., Shi, G., Fang, Z. et al. Tenascin C+ myofibroblasts exacerbate vascular neointimal hyperplasia by propagation of nerve-macrophage interactions in mice. Nat Commun 17, 2199 (2026). https://doi.org/10.1038/s41467-026-69062-3
Słowa kluczowe: neointymalne przerosty, tenascyna C, remodeling naczyń, nerwy czuciowe, zapalenie makrofagów