Clear Sky Science · pl
Paclitaksel napędza ekspansję makrofagów TREM2+, co leży u podstaw jego gorszej skuteczności terapeutycznej w porównaniu z nab‑paklitakselem
Dlaczego to badanie ma znaczenie
Wiele kobiet z rakiem piersi otrzymuje chemioterapię opartą na taksanach, najczęściej paklitaksel lub nowszą wersję związana z drobnymi cząstkami albuminy, znaną jako nab‑paklitaksel. Lekarze od dawna podejrzewali, że nowszy lek bywa skuteczniejszy, ale przyczyny nie były jasne. To badanie analizuje dane pacjentek i eksperymenty na zwierzętach, wykazując, że standardowy paklitaksel może niezamierzenie sprzyjać rozprzestrzenianiu się raka do płuc przez przeobrażenie komórek układu odpornościowego, oraz wskazuje sposób na zablokowanie tego szkodliwego efektu ubocznego.
Dwa podobne leki, dwa różne efekty
Naukowcy najpierw porównali rzeczywistą skuteczność paklitakselu i nab‑paklitakselu u tysięcy kobiet z rakiem piersi. Sumując wyniki z 17 badań klinicznych obejmujących 6 486 pacjentek, stwierdzili, że nab‑paklitaksel powodował wyższe wskaźniki kurczenia się guza oraz częstsze całkowite ustąpienie zmian w piersi i węzłach chłonnych przed zabiegiem chirurgicznym. Przewaga ta była szczególnie wyraźna u pacjentek leczonych po nieskuteczności wcześniejszych terapii. Oba leki podawano w podobnych dawkach i zaprojektowano do atakowania dzielących się komórek nowotworowych w podobny sposób, co sugeruje, że różnice wykraczają poza bezpośrednie działanie cytotoksyczne.
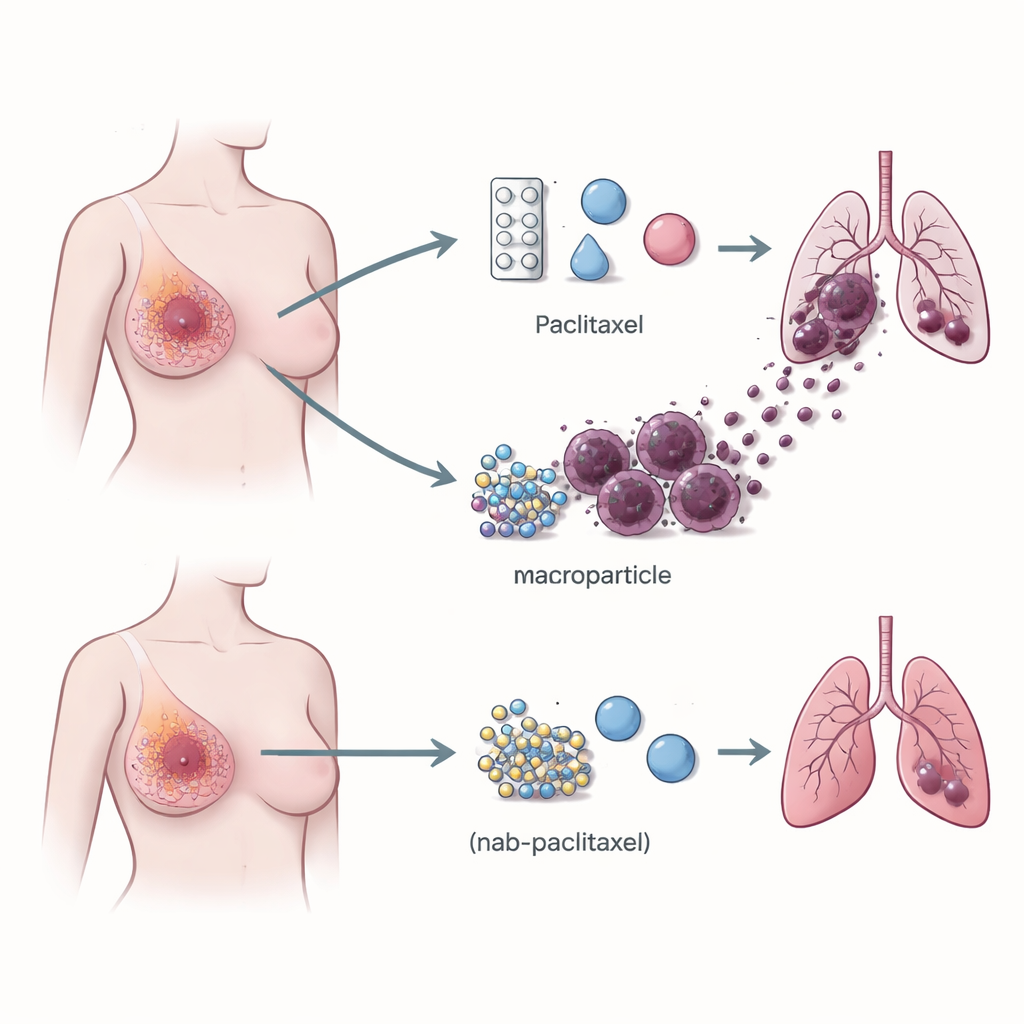
Komórki odpornościowe, które pomagają rakowi się rozprzestrzeniać
Uwaga badaczy zwróciła się ku immunologicznemu mikrośrodowisku guza — mieszaninie białych krwinek, które mogą albo zwalczać nowotwór, albo — co zdarza się zaskakująco często — wspierać jego wzrost. Wykorzystując sekwencjonowanie RNA pojedynczych komórek, które odczytuje aktywność genów w tysiącach pojedynczych komórek, zespół porównał guzy pacjentek leczonych paklitakselem i nab‑paklitakselem. Stwierdzili, że w guzach leczonych paklitakselem było znacznie więcej makrofagów niosących na powierzchni receptor TREM2. Makrofagi TREM2‑pozytywne koncentrowały się na krawędziach guza i występowały znacznie częściej u pacjentek, które później rozwinęły przerzuty do płuc, niż u tych, u których choroba pozostała miejscowa. Wzorzec ten utrzymał się w większych grupach pacjentek i w modelach mysich, co potwierdza silny związek między tym typem makrofagów a ryzykiem rozsiewu raka.
Kiedy leczenie zmniejsza guz, ale sprzyja rozsiewowi
U myszy z guzem piersi paklitaksel zrobił to, czego się oczekuje: hamował lub zmniejszał guzy pierwotne. Jednocześnie jednak zwiększał liczbę zmian nowotworowych w płucach i podnosił odsetek makrofagów TREM2‑pozytywnych w guzach oraz we krwi. Nab‑paklitaksel natomiast zmniejszał rozmiar guza bez wywoływania przerzutów do płuc ani ekspansji tych makrofagów, mimo że równie skutecznie pomniejszał guz pierwotny. Gdy gen TREM2 został usunięty u myszy lub gdy jego poziom obniżono za pomocą antysensownych oligonukleotydów (krótkich odcinków DNA wyciszających konkretne geny), paklitaksel nadal kurczył guzy pierwotne, ale w dużej mierze stracił zdolność do napędzania rozprzestrzeniania się do płuc. To pokazuje, że makrofagi z TREM2 nie są tylko biernymi obserwatorami — są koniecznym partnerem w metastazie indukowanej paklitakselem.
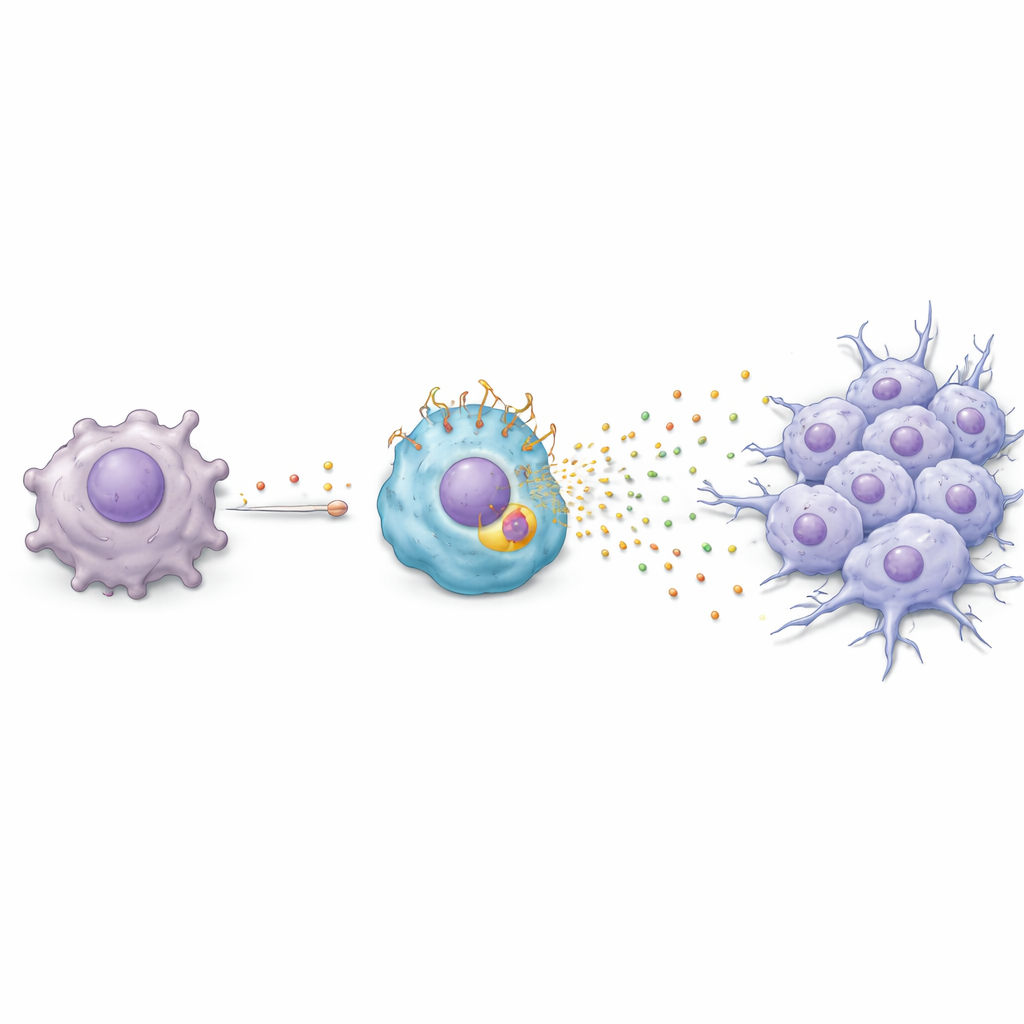
Chemiczny łańcuch reakcji od guza do komórki odpornościowej
Zespół zapytał następnie, w jaki sposób paklitaksel powoduje przejście makrofagów w ten szkodliwy, bogaty w TREM2 stan. Odkryli łańcuch zdarzeń: paklitaksel pobudza komórki nowotworowe do uruchomienia genu odpowiedzi na stres o nazwie ATF3, co z kolei zwiększa produkcję czynnika wzrostu FGF2. Komórki nowotworowe uwalniają FGF2 do otoczenia, gdzie oddziałuje na pobliskie makrofagi. W tych makrofagach FGF2 aktywuje kolejny regulator, EGR1, który podnosi poziomy TREM2. Gdy TREM2 jest wysoki, makrofagi zaczynają wydzielać mieszaninę białek — w tym Serpin E1, HGF, CCL3 i CXCL2 — które skłaniają komórki nowotworowe do przyjęcia bardziej ruchliwego, inwazyjnego fenotypu znanego jako przejście epitelialno‑mezenchymalne. W hodowlach komórkowych i u myszy ta chemiczna wymiana sygnałów zwiększała skłonność komórek guza do migracji i inwazji, kluczowych kroków w drodze do przerzutów.
Jak przemienić miecz obosieczny w bezpieczniejsze narzędzie
Z perspektywy nie‑specjalisty kluczowe przesłanie jest takie, że paklitaksel może zachowywać się jak miecz obosieczny: atakuje guzy, ale jednocześnie instruuje pewne komórki odpornościowe, by pomagały rakowi uciec do odległych narządów. Nab‑paklitaksel wydaje się unikać wywoływania tego konkretnego immunologicznego błędu. Dobrą wiadomością jest to, że blokowanie TREM2 — lub elementów łańcucha sygnałowego FGF2–EGR1–TREM2 — może w modelach zwierzęcych oddzielić korzystne działanie paklitakselu polegające na zmniejszaniu guza od ryzyka promowania przerzutów. Jeśli podobne strategie okażą się bezpieczne i skuteczne u ludzi, lekarze mogliby dalej stosować dobrze znany, szeroko dostępny lek chemioterapeutyczny, ograniczając jednocześnie jego tendencję do wspierania rozsiewu nowotworu, co przełożyłoby się na lepsze wyniki długoterminowe dla pacjentek.
Cytowanie: Xing, Y., Zhong, R., Li, Q. et al. Paclitaxel drives TREM2+ macrophage expansion underlying its inferior therapeutic efficacy compared to Nab-paclitaxel. Nat Commun 17, 2272 (2026). https://doi.org/10.1038/s41467-026-69060-5
Słowa kluczowe: rak piersi, paklitaksel, mikrośrodowisko guza, makrofagi, przerzuty