Clear Sky Science · pl
Niezawodne przekształcanie interaktomu przeciwciał wewnątrz komórki
Przekształcanie przeciwciał w maleńkie narzędzia wewnątrz komórek
Przeciwciała są znane jako precyzyjne „bronze” krążące we krwi, celujące w wirusy i inne zagrożenia. Jednak wiele procesów chorobowych, w tym choroba Alzheimera, Parkinsona i niektóre nowotwory, przebiega głównie wewnątrz komórek, gdzie zwykłe przeciwciała rzadko docierają lub działają skutecznie. W tym badaniu pokazano, jak systematycznie przebudować istniejące przeciwciała w mniejsze „intrabody”, które funkcjonują niezawodnie we wnętrzu żywych komórek ludzkich, otwierając drogę do nowych narzędzi diagnostycznych, badawczych i potencjalnie przyszłych terapii działających bezpośrednio w centrum procesów chorobowych.
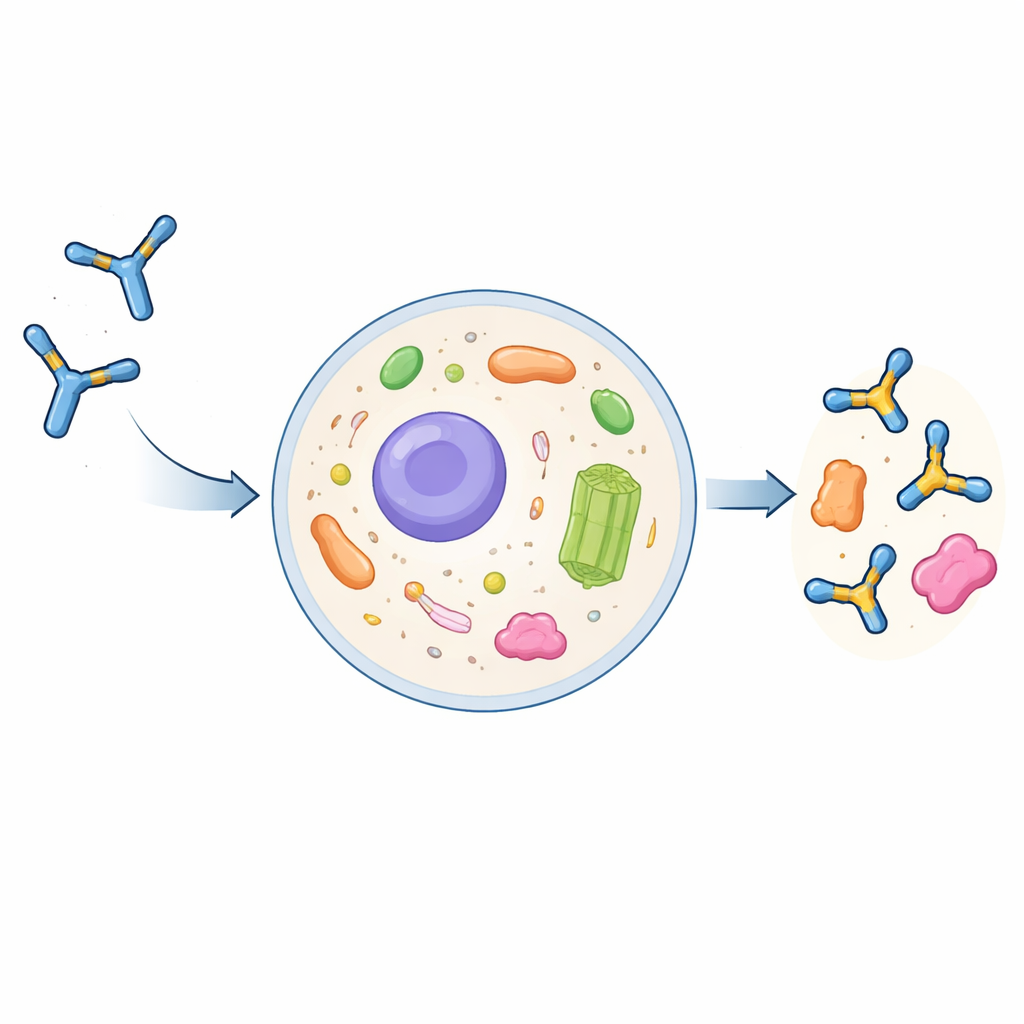
Dlaczego zwykłe przeciwciała słabo działają wewnątrz komórek
Pełnowymiarowe przeciwciała to duże, w kształcie litery Y białka wyewoluowane do działania na zewnątrz komórek. Powstają i są modyfikowane chemicznie w szlaku wydzielniczym komórki, a następnie uwalniane do krwiobiegu. Jeśli zostaną ponownie pobrane przez komórki, zwykle trafiają do kompartamentów degradacyjnych zamiast do płynnego wnętrza komórki, cytoplazmy. Naukowcy mogą skrócić przeciwciała do ich zasadniczych części rozpoznających, zwanych pojedynczymi fragmentami zmienności łańcuchów (scFv), i wyrażać je jako intrabody wewnątrz komórek. Jednak te intrabody często agregują, stają się nierozpuszczalne i tracą zdolność wiązania swoich celów. Do tej pory nie istniał ogólny, wiarygodny przepis na przekształcenie konwencjonalnego przeciwciała w dobrze zachowujące się intrabody.
Odnalezienie zasad projektowania rozpuszczalnych intrabody
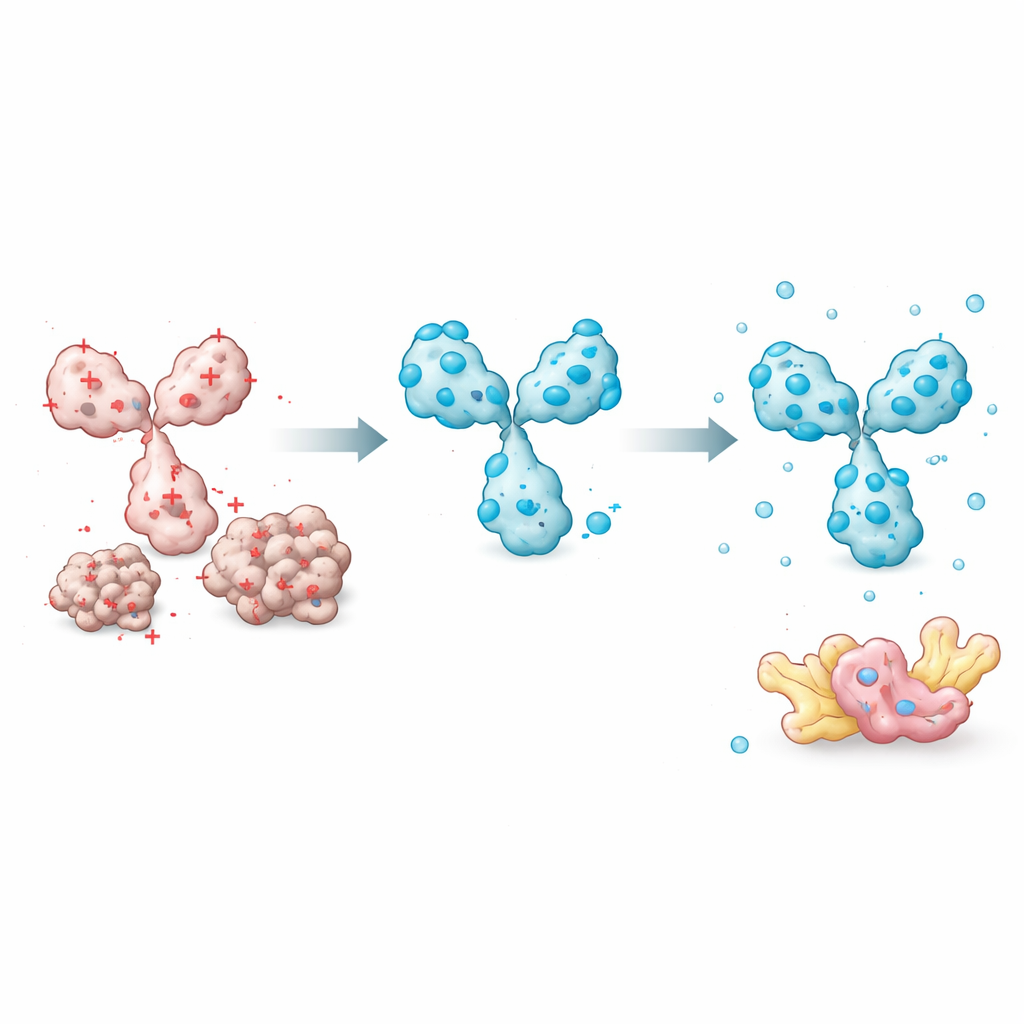
Badacze rozpoczęli od zmierzenia, jak dobrze 45 różnych intrabody pozostawało w stanie rozpuszczonym podczas produkcji w komórkach ludzkich. Systematycznie porównali wiele cech białek — takich jak ogólna hydrofobowość, przewidywana jakość struktury i właściwości pętli wiążących — aby sprawdzić, które z nich najlepiej wyjaśniają, czy intrabody pozostają rozpuszczalne. Jeden prosty czynnik wyróżnił się spośród innych: ładunek elektryczny w zbliżonym do fizjologicznego pH. Intrabody o silnie ujemnym ładunku netto miały znacznie większe szanse pozostania rozpuszczalnymi, podczas gdy te o ładunku obojętnym lub dodatnim miały tendencję do agregacji. Inne zaawansowane predyktory, w tym wskaźniki zaufania struktury z systemu AlphaFold, nie korelowały z rozpuszczalnością. Pozwoliło to zespołowi zbudować praktyczny, oparty na ładunku model, który potrafi oszacować, jaka część intrabody znajdzie się w frakcji rozpuszczalnej ekstraktu komórkowego.
Przeprojektowanie łączników i domen dla lepszego zachowania
Wyposażeni w tę wiedzę, autorzy skupili się na cechach, które można łatwo dostroić, nie zakłócając sposobu, w jaki intrabody rozpoznają swój cel. Kluczowym elementem jest krótki peptydowy „łącznik” łączący dwie domeny zmienne. Większość istniejących projektów używa łączników obojętnych, które nie zmieniają ładunku. Wprowadzając na tych pozycjach aminokwasy o ładunku ujemnym, badacze mogli obniżyć ogólny ładunek intrabody, dramatycznie poprawiając rozpuszczalność przy zachowaniu wiązania docelowego. Odkryli też, że kolejność domen zmiennych (czy część ciężka czy lekka jest pierwsza) oraz konkretne pozycje w ramach szkieletu poza pętlami wiążącymi wpływają na to, jak łatwo białko się fałduje i pozostaje rozpuszczalne. Wybór kolejności domen chroniącej bardziej kruche regiony oraz wprowadzenie starannie umieszczonych mutacji zamieniających ładunek dodatkowo poprawiały właściwości.
Wykorzystanie sztucznej inteligencji do budowy intrabody na dużą skalę
Aby wyjść poza pojedyncze próby metodą prób i błędów, autorzy połączyli swoje proste zasady dotyczące ładunku z zaawansowanym oprogramowaniem do projektowania białek opartym na uczeniu głębokim. Bazując na znanych szkieletem przeciwciał, zastosowali podejście „odwróconego fałdowania”, by zaproponować nowe sekwencje, które nadal przyjmą pożądany kształt, ale będą miały cechy powierzchniowe — zwłaszcza wzory ładunków — sprzyjające stabilności i rozpuszczalności. Ograniczyli zmiany w kluczowych pętlach wiążących, aby zachować rozpoznawanie, jednocześnie pozwalając algorytmowi przeprojektować otaczające powierzchnie. Testy wykazały, że wiele z tych intrabody projektowanych przez SI było nie tylko wysoce rozpuszczalnych, ale również bardziej termicznie stabilnych niż warianty zaprojektowane przez ludzi, przy zachowaniu zdolności wiązania celów istotnych dla chorób, takich jak zmisfoldowany SOD1, p53, α-synukleina i inne białka związane z neurodegeneracją.
Budowanie biblioteki komórkowych „łapaczy” białek
Stosując te zasady i narzędzia na dużą skalę, zespół obliczeniowo przeformatował 672 przeciwciała w intrabody przewidywane jako funkcjonalne wewnątrz komórek. Te zaprojektowane molekuły obejmują ponad 60 różnych wewnątrzkomórkowych celów, w tym białka zaangażowane w chorobę Alzheimera, Parkinsona i Huntingtona, a także czynniki związane z rakiem i modyfikacje potranslacyjne, takie jak fosforylacja i acetylacja. W eksperymentach wybrane intrabody skutecznie wyłapywały specyficzne formy białek związane z chorobą, takie jak mutant SOD1 czy określone konformacje α-synukleiny, ignorując wersje normalne. Wszystkie sekwencje zostały udostępnione otwarcie, a autorzy udostępniają narzędzie internetowe, które pozwala innym oszacować rozpuszczalność intrabody na podstawie sekwencji przy użyciu tego samego modelu opartego na ładunku.
Co to oznacza dla przyszłych leków i badań
W praktyce ta praca przekształca ogromny istniejący zbiór przeciwciał — wiele już zbadanych w kontekście klinicznym — w zestaw narzędzi, który można niezawodnie dostosować do użycia wewnątrz komórek. Dzięki przestrzeganiu prostego zestawu zasad projektowych, badacze mogą teraz tworzyć intrabody, które z dużym prawdopodobieństwem zadziałają za pierwszym podejściem, oszczędzając czas i koszty. Dla laika kluczowa wiadomość jest taka, że naukowcy znaleźli prosty sposób na „przeprogramowanie” naszych najlepszych detektorów białkowych, aby działały w zatłoczonym wnętrzu żywych komórek, gdzie zaczyna się wiele chorób. Może to przyspieszyć rozwój nowych metod śledzenia, badania, a w końcu leczenia schorzeń wywoływanych przez zmisfoldowane lub źle funkcjonujące białka.
Cytowanie: O’Shea, C.M., Shahzad, R., Aghasoleimani, K. et al. Reliable repurposing of the antibody interactome inside the cell. Nat Commun 17, 2222 (2026). https://doi.org/10.1038/s41467-026-69057-0
Słowa kluczowe: intrabody, inżynieria przeciwciał, rozpuszczalność białek, choroby neurodegeneracyjne, sztuczna inteligencja w biologii