Clear Sky Science · pl
Regulacja wody na granicy faz w celu przeniesienia tlenu na benzyliczne wiązania C(sp3)–H przez aktywowaną przez Ni kowalencyjność wolframu i tlenu
Przekształcanie wody i oleju w użyteczne chemikalia
Chemicy od dawna poszukują czystszych sposobów zamiany prostych, pochodzących z olejów cząsteczek w bardziej wartościowe składniki do tworzyw, leków i produktów codziennego użytku. W badaniu pokazano, że staranna „regulacja” cienkiej warstwy wody stykającej się z elektrodą może sprawić, że zwykła woda dostarczy tlen do opornych węglowodorów, zmniejszając odpady i zużycie energii.
Dlaczego tlen z wody ma znaczenie
Wiele przemysłowych chemikaliów powstaje przez przyłączenie tlenu do węglowodorów — cząsteczek zbudowanych głównie z węgla i wodoru. Obecnie często oznacza to użycie silnych utleniaczy i wysokich temperatur, co pochłania dużo energii i generuje emisje wpływające na klimat. Woda jest tanim, bezpiecznym i dostępnym źródłem tlenu, ale przekonanie jej do bezpośredniego oddania tlenu trudnym wiązaniom węgiel–wodór zwykle wymaga bardzo wysokich napięć. W takich warunkach większość energii elektrycznej marnuje się na rozkład wody do gazowego tlenu zamiast na wytwarzanie użytecznych produktów.
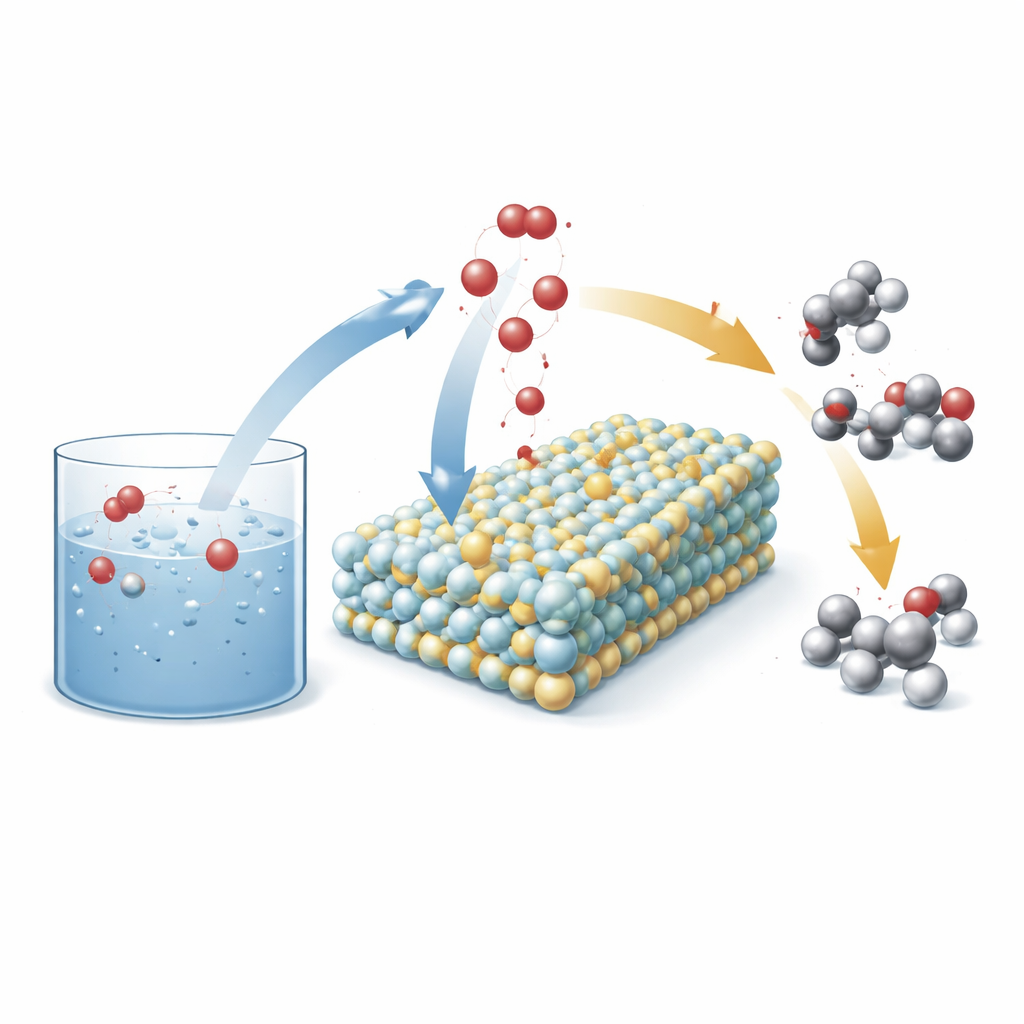
Sprytna elektroda, która przearanżowuje wodę
Badacze zaprojektowali nowy rodzaj anody (elektrody dodatniej w ogniwie elektrolitycznym) zbudowanej z drobnych cząstek węglika wolframu, które podczas pracy przekształcają się w amorficzny materiał wolfram–tlen. Do tej struktury wprowadzili pojedyncze atomy niklu. W warunkach reakcji tlen z wody migruje do ciała stałego, przekształcając je w powierzchnię tlenku wolframu aktywowaną przez nikiel z wieloma odsłoniętymi miejscami reaktywnymi. Odtworzona powierzchnia staje się platformą, na której woda i cząsteczki węglowodorów spotykają się i wymieniają tlen w kontrolowany sposób, sprzyjając powstawaniu wartościowych produktów, takich jak alkohole i ketony, zamiast nadutlenionych kwasów i innych produktów ubocznych.
Poluzowanie „klatki” wody na powierzchni
Kluczowym odkryciem jest to, że atomy niklu subtelnie zaburzają sposób, w jaki cząsteczki wody układają się przy elektrodzie. Zwykle woda przy naładowanej powierzchni tworzy gęstą sieć wiązań wodorowych, jak ciasna siatka spowalniająca ruch. Symulacje komputerowe i czułe pomiary w podczerwieni pokazują, że w pobliżu obszarów domieszkowanych niklem ta sieć staje się luźniejsza, z mniejszą liczbą wiązań wodorowych i większą liczbą „wolnych” cząsteczek wody. Tworzy to kanały, przez które woda może łatwiej dyfundować do reaktywnych miejsc wolfram–tlen. W rezultacie fragmenty zawierające tlen z wody mogą szybciej i częściej docierać do powierzchni, zasilając reakcję zamiast uciekać jako gazowy tlen.
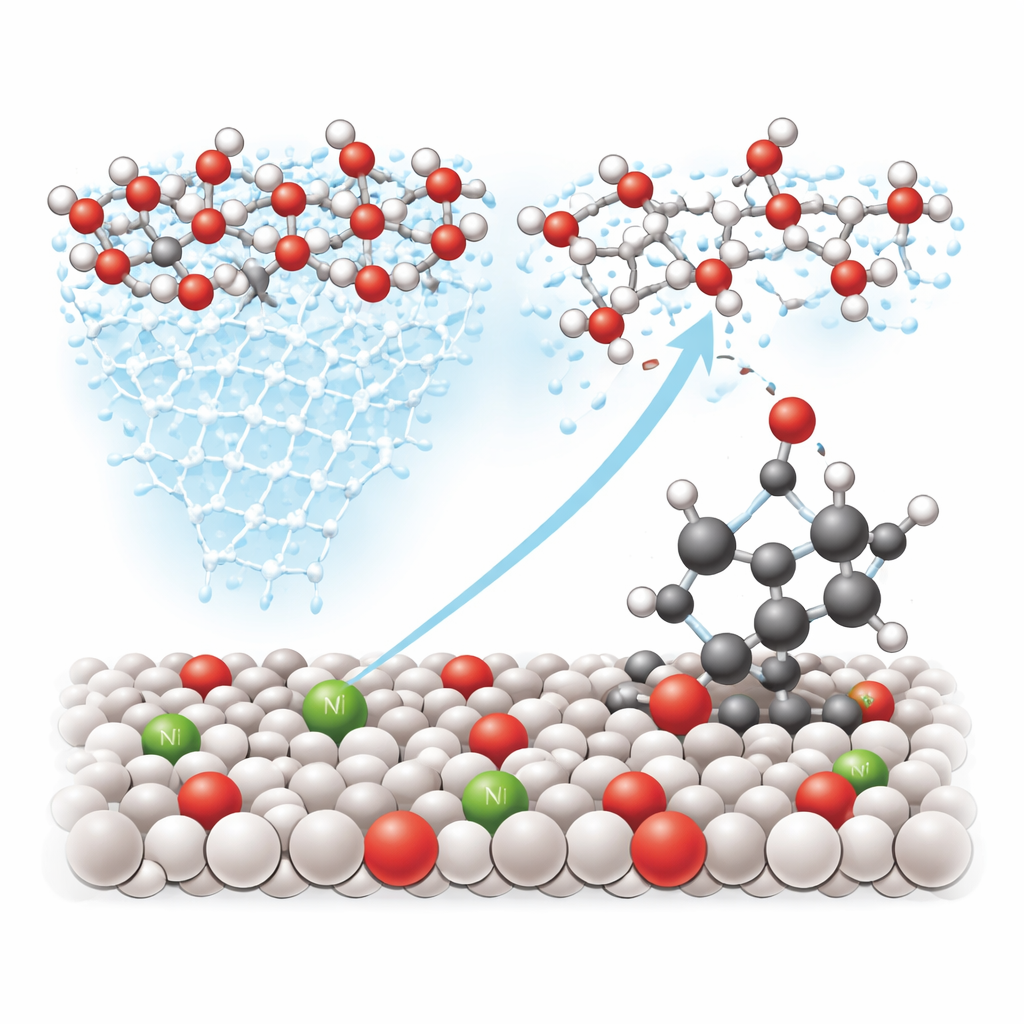
Skierowanie tlenu do właściwych wiązań
Poza poprawą „ruchu” przy powierzchni, nikiel także dostraja strukturę elektroniczną sąsiednich atomów wolframu, czyniąc niektóre miejsca szczególnie skutecznymi w chwytaniu i aktywowaniu wody. Eksperymenty z izotopami — specjalnymi odmianami tlenu i wodoru, które da się śledzić — pokazują, że aktywny tlen pochodzi ze świeżo rozszczepionej wody, a nie z wnętrza samego tlenku. Spektroskopowe „migawek” uchwyciły krótkotrwały mostek między wolframem, tlenem i benzylicznym węglem w cząsteczkach takich jak etylobenzen. Obliczenia teoretyczne potwierdzają, że na powierzchni zmodyfikowanej niklem łatwiej jest atomowi tlenu zaatakować to miejsce C–H niż podążać zwykłą ścieżką rozkładu wody prowadzącą do powstawania tlenu gazowego, skutecznie kierując reakcję w stronę użytecznych produktów tlenowych.
Wydajne, selektywne i trwałe
W testach elektroda aktywowana niklem przekształca szereg benzylicznych wiązań węgiel–wodór w alkohole i ketony z wydajnościami Faradaya — ile ładunku elektrycznego idzie na pożądaną chemię — zwykle powyżej 50%, osiągając ponad 56% w zoptymalizowanych przypadkach. System pracuje przez wiele cykli bez utraty aktywności, utrzymując strukturę nikiel–wolfram. Ponieważ używa wody jako jedynego źródła tlenu i unika dodatkowych utleniaczy chemicznych, oferuje konkurencyjną efektywność energetyczną i niższe koszty materiałowe w porównaniu z innymi zaawansowanymi metodami. Choć obecny zakres dotyczy głównie miejsc benzylicznych, zasadnicza idea — użycie atomowych dodatków do przeformowania wody na granicy faz i przekierowania ścieżek reakcyjnych — wskazuje na szersze możliwości dla bardziej zielonej, napędzanej elektrycznością oksydacji inaczej inertnych wiązań węgiel–wodór.
Co to oznacza dla czystszej chemii
Praca pokazuje, że drobne zmiany na poziomie atomowym mogą mieć ogromny wpływ na zachowanie wody przy elektrodzie i na to, gdzie trafia jej tlen. Poprzez zastosowanie atomów niklu do zarówno poluzowania struktury wody na granicy faz, jak i dopracowania miejsc reaktywnych, autorzy przekształcają wodę w efektywnego dawcy tlenu dla trudnych do aktywacji wiązań węglowodorowych, jednocześnie tłumiąc niepożądane powstawanie tlenu gazowego. W dłuższej perspektywie strategie tego typu mogą pomóc w przeprojektowaniu chemii utleniania w przemyśle chemicznym, czyniąc ją bardziej energooszczędną i przyjazną klimatowi dzięki wykorzystaniu elektryczności i wody zamiast ostrych utleniaczy i reagentów pochodzenia kopalnego.
Cytowanie: Leng, BL., Lin, X., Dong, HY. et al. Regulating interfacial water for oxygen transfer to benzylic C(sp3)–H bonds via Ni-activated tungsten-oxygen covalency. Nat Commun 17, 2355 (2026). https://doi.org/10.1038/s41467-026-69054-3
Słowa kluczowe: elektrokataliza, utlenianie wody, aktywacja wiązań benzylicznych C–H, tlenek wolframu domieszkowany niklem, chemia zielona