Clear Sky Science · pl
Dualne RNA-Seq in vivo ujawnia kluczowe efektory zaburzania bariery nabłonkowej przez patogen zewnątrzkomórkowy
Jak niektóre zarazki prześlizgują się przez nasze komórkowe ogrodzenia
Nasze narządy wyściełają ściśle przylegające komórki, które działają jak mury, utrzymując krew, drobnoustroje i toksyny tam, gdzie powinny być. Mimo to niektóre zarazki potrafią wślizgnąć się między te komórki i rozprzestrzeniać po organizmie. Badanie to ukazuje z dużą szczegółowością, jak bakteria wywołująca leptospirozę — poważną chorobę o zasięgu światowym — po cichu dociera do narządów takich jak wątroba i nerki, a następnie wykorzystuje sprytne działanie związane z wapniem wewnątrz naszych komórek, aby rozchylić te ochronne bariery.
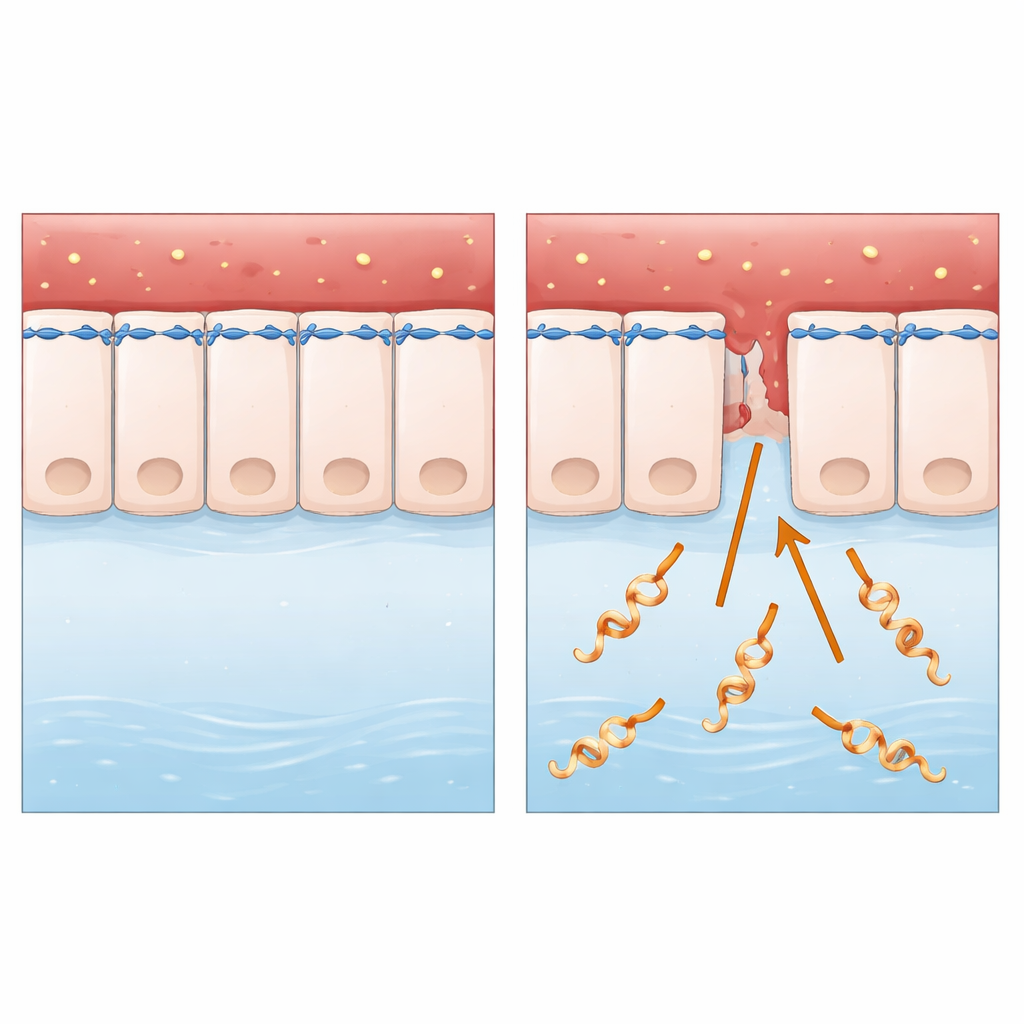
Ucichy najeźdźca tkanek zwierzęcych i ludzkich
Badania koncentrują się na Leptospira interrogans, spiralnej bakterii przenoszonej głównie ze zwierząt na ludzi przez skażoną wodę lub glebę. Po wniknięciu przez drobne uszkodzenia skóry lub błony śluzowe porusza się wraz z krwią i może wywołać ciężką chorobę, w tym niewydolność wątroby i nerek oraz krwotoki wewnętrzne. W przeciwieństwie do wielu dobrze zbadanych mikroorganizmów, Leptospira żyje poza komórkami i nie posiada części klasycznych „broni molekularnych”, na które zwykle zwracają uwagę naukowcy. To czyniło ją idealnym modelem do postawienia podstawowego pytania: jak pozornie prosta, wolno żyjąca bakteria tak skutecznie przekracza nienaruszone warstwy komórek?
Obserwowanie, jak geny gospodarza i zarazka komunikują się jednocześnie
Aby uchwycić proces zakażenia w żywym zwierzęciu, zespół zastosował podwójne sekwencjonowanie RNA u chomików, modelu ostrej leptospirozy. Ta metoda odczytuje, które geny są włączone lub wyłączone zarówno u gospodarza, jak i u patogenu jednocześnie. Naukowcy zakażili chomiki i pobrali tkanki wątroby oraz nerek po jednym i trzech dniach. Na wczesnym etapie, mimo dużej liczby bakterii, aktywność genów komórek zwierząt zmieniała się minimalnie, co sugeruje, że Leptospira początkowo wymyka się uwadze układu odpornościowego. Do trzeciego dnia oba narządy wykazały silną reakcję, zwłaszcza wątroba: geny związane z zapaleniem, połączeniami między komórkami oraz wewnętrznym szkieletem komórek zostały wyraźnie zmienione, co wskazuje na aktywną przebudowę barier tkankowych.
Rozrywanie komórkowego zamka od zewnątrz
Warstwy komórek są uszczelnione przez połączenia zamykające i przylegające, które łączą sąsiednie komórki i kotwiczą je do pierścienia aktyny i miozyny — tej samej pary białek, która pomaga mięśniom się kurczyć. Mikroskopia komórek nabłonkowych człowieka zakażonych Leptospira wykazała zmianę kształtu, pojawienie się szczelin między komórkami oraz osłabienie lub niewłaściwe rozmieszczenie kluczowych białek połączeń. Co istotne, komórki nie ginęły, co oznacza, że bariera była demontowana, a nie niszczona. Naukowcy zaobserwowali także oznaki stresu w zakładach fałdowania białek komórek, ale zablokowanie tego stresu nie przywróciło połączeń, co skierowało ich uwagę na innego podejrzanego.
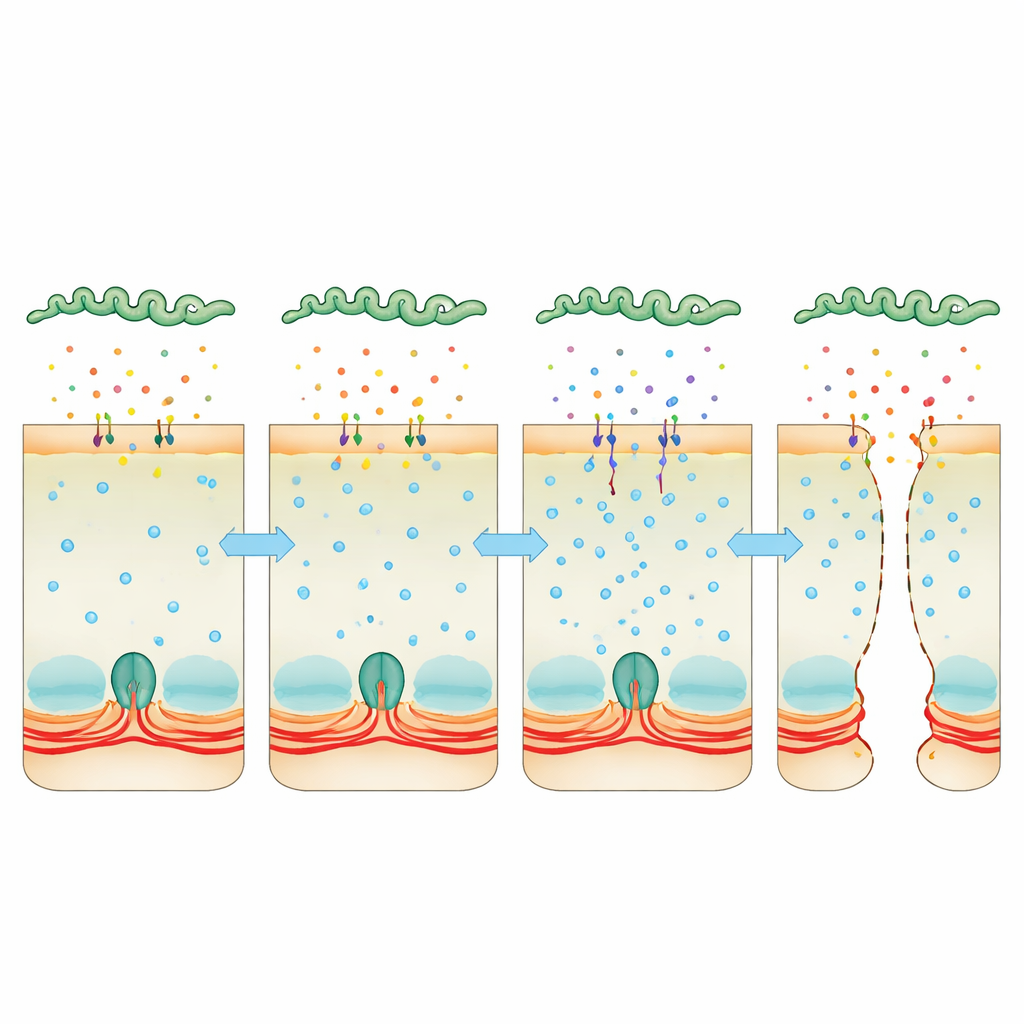
Porwanie wapnia jako ukryte łom
Uwagę zwrócono na wapń, uniwersalny sygnał wewnątrz komórek, który może zaciskać lub rozluźniać pierścień aktyna–miozyna. Zakażone komórki kumulowały więcej wapnia, a to wiązało się ze zwiększoną aktywnością kinazy lekkich łańcuchów miozyny, enzymu, który powoduje, że pierścień kurczliwy napina połączenia. Gdy zespół zastosował związek wychwytujący wapń lub leki hamujące kalmodulinę albo tę kinazę, warstwy komórek pozostawały bardziej szczelne, a bakteriom trudniej było się przecisnąć. Jednocześnie głębokie sekwencjonowanie RNA bakterii wykazało, że wewnątrz gospodarza Leptospira silnie zwiększa produkcję dwóch białek „modyfikujących wirulencję”, które przypominają toksyny. Te białka są wydzielane na zewnątrz, wiążą się z komórkami gospodarza i są wykrywalne wewnątrz nich. Gdy bakterie pozbawione były jednego lub obu tych białek, znacznie gorzej przechodziły przez warstwy komórek i wywoływały śmiertelną chorobę, a ich wydzielina nie podnosiła już poziomu wapnia ani nie rozmontowywała połączeń tak skutecznie.
Co to oznacza dla choroby i przyszłej obrony
Łącznie wyniki przedstawiają klarowną opowieść. Po niemal niezauważalnym wniknięciu do organizmu Leptospira zaczyna wydzielać podobne do toksyn białka modyfikujące wirulencję. Białka te wiążą się z komórkami nabłonkowymi i zaburzają wewnątrzkomórkowy bilans wapnia, co z kolei uruchamia szlak kurczliwy, który rozciąga „zamek” trzymający razem sąsiednie komórki. W miarę rozluźniania się połączeń zamykających i przylegających pojawiają się mikroskopijne szczeliny, pozwalające bakteriom przechodzić między komórkami, kolonizować narządy i wywoływać ciężką chorobę. Identyfikując ten napędzany wapniem mechanizm oraz białka bakteryjne za nim stojące, badanie otwiera drogę do nowych strategii — takich jak blokowanie tych białek lub ich szlaku sygnałowego — by wzmacniać nasze komórkowe ogrodzenia i ograniczać rozprzestrzenianie się leptospirozy, a być może też innych zakażeń wykorzystujących podobne taktyki.
Cytowanie: Giraud-Gatineau, A., Haustant, G., Monot, M. et al. In vivo dual RNA-Seq uncovers key effectors of epithelial barrier disruption by an extracellular pathogen. Nat Commun 17, 2274 (2026). https://doi.org/10.1038/s41467-026-69033-8
Słowa kluczowe: leptospiroza, bariera nabłonkowa, sygnalizacja wapniowa, toksyny bakteryjne, interakcje gospodarz–patogen