Clear Sky Science · pl
Wzmocnione supercharging nDIA-MS umożliwia globalne profilowanie zmian rozpuszczalności proteomu wywołanych lekami
Dlaczego zachowanie białek ma znaczenie wykraczające poza zwykłe liczenie
Leki mogą wpływać nie tylko na ilość białka wytwarzanego przez komórkę, lecz także na jego lokalizację oraz to, czy występuje ono jako forma wolna, czy skłonna do agregacji na strukturach komórkowych. Zmiany w „gdzie” i „jak” białka istnieją w komórce są ściśle powiązane z chorobami, takimi jak rak i schorzenia neurodegeneracyjne, ale trudno je mierzyć masowo. W tym badaniu przedstawiono szybką, wydajną metodę skanowania tysięcy ludzkich białek jednocześnie, aby ocenić, jak ich rozpuszczalność — czyli czy występują w stanie wolnym czy bardziej związanym — zmienia się po ekspozycji komórek na dwa powszechnie stosowane związki eksperymentalne.
Szybszy, ostrzejszy sposób obserwacji białek
Autorzy opierają się na kluczowej technologii współczesnej biologii: spektrometrii mas, technice ważącej i zliczającej fragmenty białek. Standardowe metody doskonale informują nas o ilości poszczególnych białek, ale mają trudności z ujawnianiem zmian stanu białek, takich jak przyłączanie się do DNA czy tworzenie gęstych zespołów. W tej pracy badacze udoskonalają wersję spektrometrii z wąskimi oknami akwizycji niezależnej od danych (nDIA-MS). Dodając do medium przesyłającego peptydy przez instrument małe chemiczne dodatki, zwane reagentami superchargingującymi, zwiększają ładunki elektryczne tych fragmentów i znacznie wzmacniają sygnał.
Po przetestowaniu dwóch powszechnych dodatków superchargingujących, dimetylosulfotlenku (DMSO) i m-nitrobenzylowego alkoholu (mNBA), stwierdzili, że 3% DMSO daje największy całkowity wzrost sygnału i najwyższą liczbę wykrytych białek, natomiast mNBA lepiej zwiększa liczbę i ładunek pojedynczych fragmentów peptydowych. Przy zoptymalizowanym ustawieniu zespół jest w stanie zidentyfikować około 9 600 ludzkich białek z zaledwie jednego mikrograma standardowego trawienia komórkowego w 15-minutowym przebiegu — to wyjątkowe połączenie szybkości i głębokości dla rutynowych eksperymentów. Ta wydajność tworzy podstawę do wykorzystania nDIA-MS nie tylko do zliczania białek, lecz także do badania, jak ich stan fizyczny reaguje na stres.
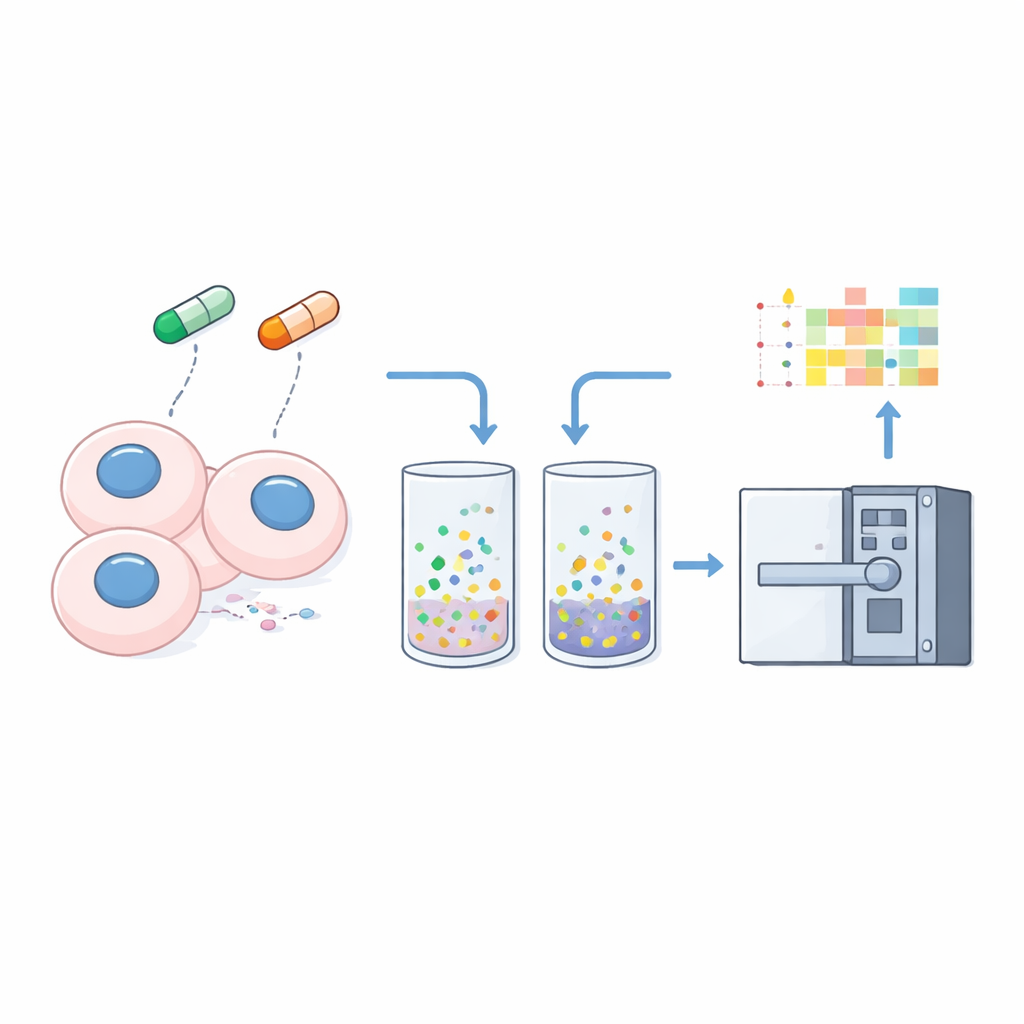
Przekształcenie rozpuszczalności w odczyt zmian komórkowych
Aby przekształcić rozpuszczalność w mierzalny sygnał, badacze delikatnie wstępnie traktują komórki łagodnym detergentem, który ekstraktuje białka swobodnie rozpuszczalne, pozostawiając materiał ściśle związany z DNA, błonami lub innymi strukturami. Analizują zarówno pełny liznat komórkowy, jak i tę „nierozpuszczalną” frakcję z trzech linii komórkowych nowotworowych przy użyciu zoptymalizowanej metody nDIA-MS. Porównując obfitość każdego białka w pelletcie względem próbki całokomórkowej, obliczają prosty „wskaźnik nierozpuszczalności” — wyższe wartości sugerują silniejsze związanie ze strukturami komórkowymi, niższe wskazują na stan bardziej rozpuszczalny i wolny.
Zespół następnie eksponuje komórki przez zaledwie godzinę na dwa leki: MG132, bloker proteasomu, który uniemożliwia komórkom degradację niechcianych białek, oraz ML-792, inhibitor aktywacji SUMO, który zakłóca kluczowy system znakowania białek. Krótka ekspozycja jest celowa; ma uchwycić szybkie, wczesne przesunięcia w zachowaniu białek zanim zmiany ekspresji genów w pełni się rozwiną. Nawet w tym krótkim oknie są w stanie ilościowo ocenić zmiany rozpuszczalności i obfitości dla 8 694 białek oraz potwierdzić, że frakcjonowanie wyraźnie oddziela klasyczne białka rozpuszczalne, takie jak tubulina, od białek związanych z chromatyną, jak histony.
Leki przekształcające krajobraz białkowy komórki
MG132 i ML-792 powodują szeroko zakrojoną, lecz odmienną przebudowę rozpuszczalności białek. MG132 zwiększa nierozpuszczalność ponad tysiąca białek i zwiększa rozpuszczalność ponad sześciuset białek we wszystkich trzech liniach komórkowych. Wiele dotkniętych białek działa na styku kontroli jakości białek, odpowiedzi na uszkodzenia DNA, regulacji genów i autofagii — systemu samoczyszczenia komórki. Na przykład składowe kompleksu aktywatora proteasomu oraz adaptery pomagające znakować wadliwe białka stają się mniej rozpuszczalne, co sugeruje, że gdy degradacja jest zablokowana, kluczowe czynniki kontroli jakości same zostają zatrzymane na strukturach takich jak chromatyna czy błony komórkowe. Białka autofagii i uczestnicy odpowiedzi na uszkodzenia, w tym regulator stresu HSF1, również przesuwają się w kierunku bardziej nierozpuszczalnych, kondensatopodobnych stanów, zgodnie z formowaniem jądrowych ciał stresowych.
ML-792, w przeciwieństwie do tego, silnie oddziałuje na białka zaangażowane w transkrypcję i na sam system SUMO. Setki białek stają się bardziej nierozpuszczalne lub bardziej rozpuszczalne po zablokowaniu aktywacji SUMO, a podstawowe białka SUMO przechodzą do puli rozpuszczalnej, co jest zgodne z oczekiwaniami. Badanie uwypukla uderzające zachowania: podjednostki polimerazy RNA III stają się bardziej nierozpuszczalne, sugerując zmieniony transport do jądra lub wiązanie z chromatyną; kluczowi represory związane z ciałami jądrowymi, tacy jak SP100 i DAXX, stają się bardziej rozpuszczalni, co wskazuje, że znaczniki SUMO pomagają utrzymywać je w tych kompartmentach. Gdy oba leki stosowane są osobno lub kolejno, niektóre białka, w tym NAB2, SMAD2 i RB1, wykazują skoordynowane lub nawet przeciwstawne zmiany rozpuszczalności, odsłaniając subtelne współdziałanie między systemami ubikwityny i SUMO w kontroli lokalizacji białek.
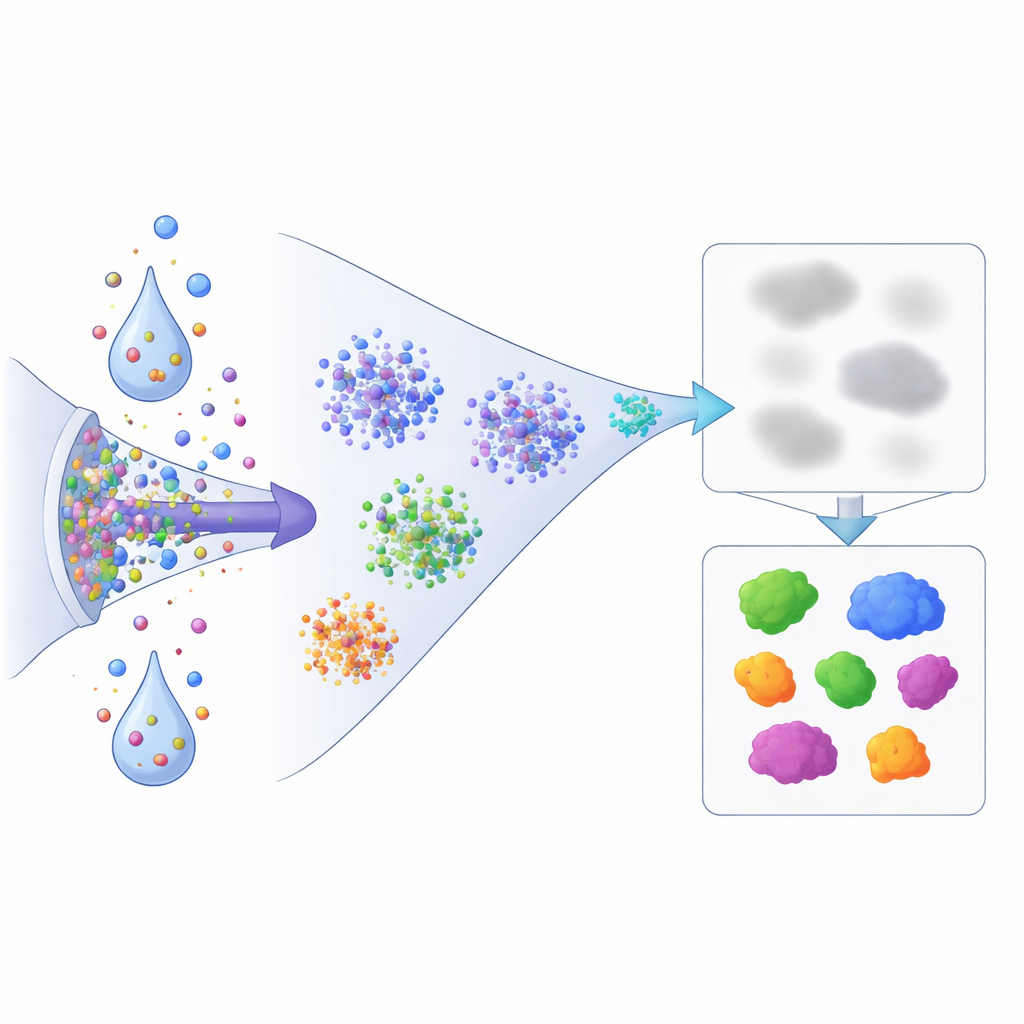
Co to oznacza dla przyszłego odkrywania leków
Dla nonspecjalistów zasadniczy przekaz jest taki, że białka nie tylko zmieniają swoją ilość, gdy komórki są zestresowane lub traktowane lekami; przemieszczają się także, kondensują i zmieniają stopień związania ze strukturami komórkowymi. Ta praca dostarcza szybkiego, obejmującego całe proteomy sposobu obserwacji tych przesunięć. Łącząc dostrojony przepływ pracy spektrometrii mas z prostym porównaniem rozpuszczalne kontra nierozpuszczalne, autorzy pokazują, że powszechne eksperymentalne leki szybko reorganizują wewnętrzny krajobraz białkowy w sposób, którego standardowe pomiary obfitości by nie uchwyciły. Podejście otwiera drzwi do mapowania, jak kandydujące leki przekształcają stany białek w całej komórce, pomagając badaczom odkrywać nieoczekiwane cele, ścieżki stresowe i punkty awarii, które mogą być kluczowe dla zrozumienia zarówno działania terapeutycznego, jak i skutków ubocznych.
Cytowanie: Xiong, Y., Zhang, H., Tan, L. et al. Supercharging-enhanced nDIA-MS enables global profiling of drug-induced proteome solubility shifts. Nat Commun 17, 2350 (2026). https://doi.org/10.1038/s41467-026-69025-8
Słowa kluczowe: rozpuszczalność proteomu, spektrometria mas, inhibitor proteasomu MG132, inhibitor SUMOylacji ML-792, przejścia stanów białek