Clear Sky Science · pl
Zaplanowana wewnętrzna architektura nanocząsteczek lipidowych o strukturze rdzeń-powłoka sprzyja efektywnemu uwalnianiu mRNA z endosomów
Dlaczego ten nowy trik dostarczania ma znaczenie
Wiele z najbardziej obiecujących nowych leków, od szczepionek przeciw COVID-19 po eksperymentalne terapie przeciwnowotworowe, opiera się na informacyjnym RNA, czyli mRNA. Jednak pojawia się uporczywy problem: gdy te kruche nici dostają się do komórek, większość z nich zostaje uwięziona i zniszczona w małych wewnętrznych pęcherzykach zwanych endosomami. W tym badaniu zaproponowano sprytne przeprojektowanie malutkich pęcherzyków tłuszczowych, znanych jako nanocząsteczki lipidowe, które przenoszą mRNA. Poprzez zorganizowanie ich wnętrza wokół stałego, złotego rdzenia, badacze diametralnie poprawili ilość mRNA, które ucieka do cytoplazmy komórki, gdzie może faktycznie produkować użyteczne białka.
Lepsze „plany ciała” dla malutkich kurierów
Obecne szczepionki i terapie oparte na mRNA w przeważającej mierze polegają na miękkich, bezkształtnych cząstkach z mieszaniny tłuszczów otaczających mRNA. Teoretycznie specjalne „jonizowalne” lipidy w tych cząstkach powinny nabierać ładunku dodatniego w kwaśnym wnętrzu endosomów i rozrywać błonę endosomalną, uwalniając mRNA. W praktyce ujemny ładunek mRNA znosi dużą część tego efektu, więc tylko około 2 procent dostarczonego mRNA trafia do aparatu wytwarzającego białka w komórce. Autorzy postawili proste, ale silne pytanie: zamiast jedynie zmieniać chemię lipidów, co jeśli przeprojektowaliby wewnętrzną architekturę cząstki, by kontrolować, gdzie mRNA i lipidy znajdują się względem siebie?
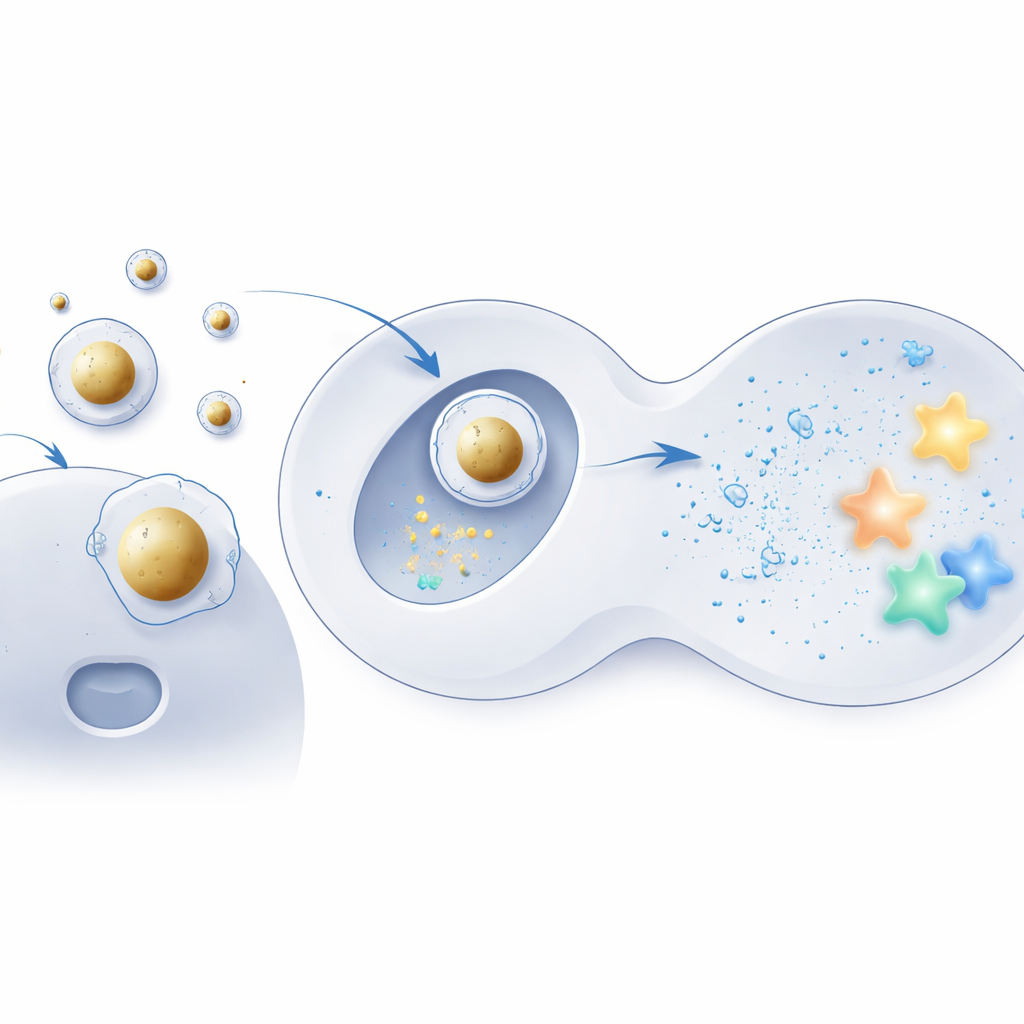
Budowa powłoki dostarczającej wokół złotego rdzenia
Aby przetestować ten pomysł, zespół użył maleńkich kul ze złota jako sztywnych rdzeni i powlekał je tymi samymi jonizowalnymi lipidami stosowanymi w konwencjonalnych formulacjach. Ujemnie naładowane mRNA najpierw zostało skondensowane na tych rdzeniach, a dopiero potem zespół otoczył całość znaną mieszanką lipidów pomocniczych i stabilizujących, tworząc uporządkowaną strukturę rdzeń–powłoka. Mikroskopia elektronowa i symulacje komputerowe wykazały, że te „Au‑LNP” były wysoce jednorodne, termodynamicznie stabilne i dobrze zachowywały kształt w wodnych, przypominających warunki biologiczne środowiskach. Co istotne, całkowity skład lipidowy pozostał taki sam jak w standardowych cząstkach, co pozwoliło wyizolować wewnętrzną strukturę — a nie składniki — jako kluczową zmianę.
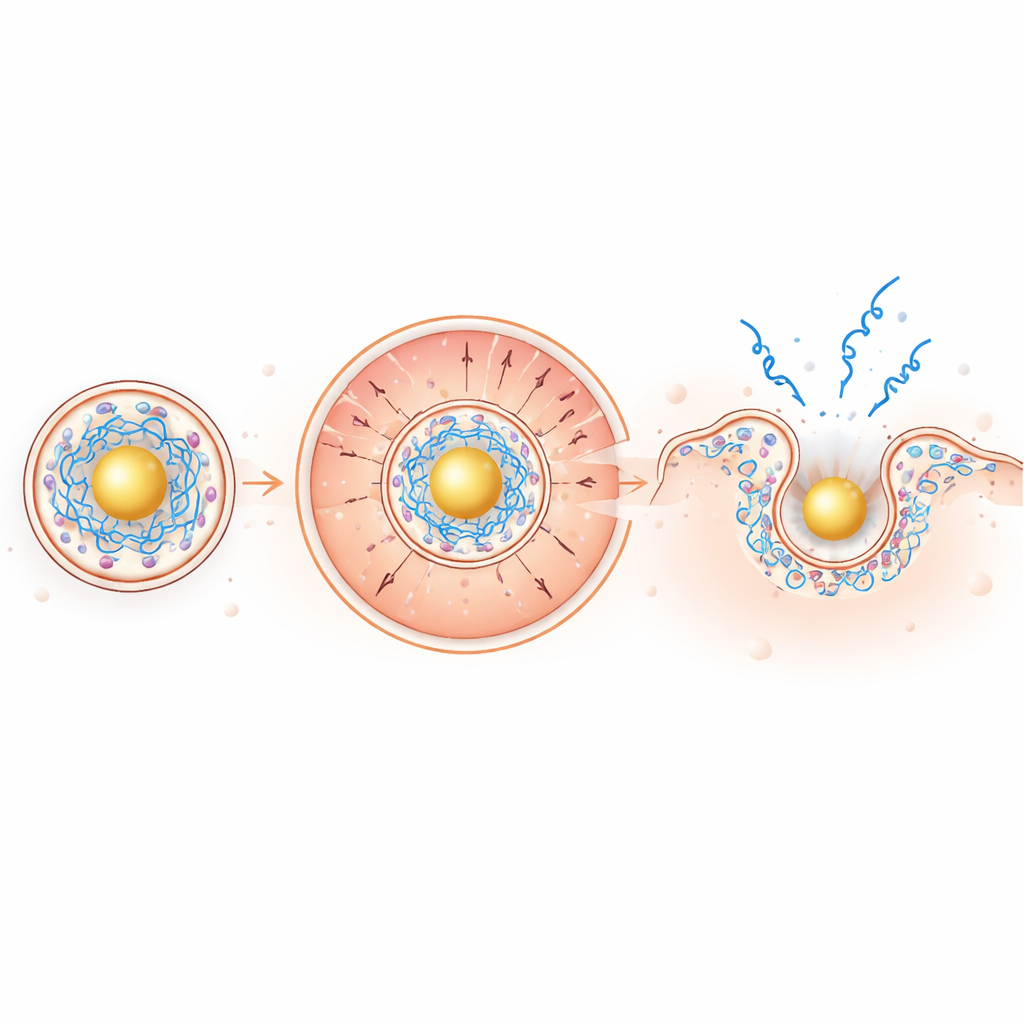
Jak przeorganizowane wnętrze zwiększa ucieczkę
W lekko kwaśnym środowisku endosomalnym rdzeń na bazie złota staje się silnie dodatni, przyciągając ujemnie naładowane mRNA do wnętrza i wypychając dodatnio naładowane jonizowalne lipidy na zewnątrz w kierunku otaczającej błony. Ta segregacja napędzana ładunkami koncentruje lipidy zaburzające błonę dokładnie tam, gdzie są potrzebne. W testach na modelowych błonach i w krwinkach czerwonych nowe cząstki były skuteczniejsze w tworzeniu przecieków błon przy niskim pH, pozostając jednocześnie obojętne przy neutralnym pH — pożądana cecha bezpieczeństwa. W żywych komórkach obrazowanie fluorescencyjnego mRNA wykazało około dwukrotny wzrost ucieczki z endosomów i zadziwiający ~100-krotny wzrost zasięgu rozproszenia mRNA w cytoplazmie w porównaniu z konwencjonalnymi cząstkami.
Z naczyń do myszy: silniejsze sygnały i lepsza ochrona
Te fizyczne zalety przełożyły się na realne korzyści biologiczne. W różnych typach komórek cząstki ze złotym rdzeniem wywoływały znacznie wyższą produkcję białek raportujących niż standardowe formulacje, zwłaszcza przy niskich dawkach. U myszy zwiększyły one wytwarzanie białka kierowanego przez mRNA nawet pięciokrotnie do siedmiokrotnie po wstrzyknięciach do mięśnia lub dożylnych, bez zmiany profilu gromadzenia się cząstek w organizmie. Przy zastosowaniu do dostarczenia mRNA kodującego białko kolca SARS‑CoV‑2 przeprojektowane cząstki w przybliżeniu podwoiły poziomy przeciwciał po pierwszym zastrzyku i dodatkowo je zwiększyły po dawce przypominającej, jednocześnie wytwarzając bardziej skuteczne przeciwciała neutralizujące wirusa. W wymagającym modelu trójnegatywnego raka piersi szczepionki przeciwnowotworowe oparte na mRNA dostarczane przez nowe cząstki skuteczniej zmniejszały guzy, obniżały sygnały aktywności nowotworu i zauważalnie przedłużały przeżycie.
Bezpieczeństwo i droga do przyszłych leków
Mimo stosowania złota w rdzeniu cząstki wydawały się dobrze tolerowane u myszy. Waga ciała, markery zapalne i badania tkanek nie wykazały istotnej toksyczności, a poziomy złota w narządach wracały do wartości wyjściowych w ciągu dwóch dni. Autorzy podkreślają, że złoto służy przede wszystkim jako szkielet dowodowy: ta sama zasada wewnętrznego projektu mogłaby zostać zastosowana do innych bezpiecznych lub biodegradowalnych materiałów. Główny przekaz dla czytelników niebędących specjalistami jest taki, że sposób, w jaki pakujemy mRNA wewnątrz jego maleńkiego nośnika, może być równie istotny jak to, z czym je pakujemy. Poprzez nadanie nanocząsteczkom lipidowym bardziej zdyscyplinowanego wewnętrznego układu, ta praca oferuje nowy sposób przezwyciężenia długotrwałego wąskiego gardła w dostarczaniu mRNA — odblokowując skuteczniejsze szczepionki i terapie w chorobach zakaźnych, onkologii i nie tylko.
Cytowanie: Li, T., Zhang, J., Guo, J. et al. Engineered internal architecture of core-shell lipid nanoparticles promotes efficient mRNA endosomal release. Nat Commun 17, 2187 (2026). https://doi.org/10.1038/s41467-026-69017-8
Słowa kluczowe: dostarczanie mRNA, nanocząsteczki lipidowe, ucieczka z endosomów, nanomedycyna, szczepionki RNA