Clear Sky Science · pl
FGF13 działa jako regulator osi ERK/aerobowej glikolizy w stanie zapalnym podczas septycznego uszkodzenia płuc
Dlaczego to badanie ma znaczenie dla pacjentów z ciężkimi zakażeniami
Posocznica (sepsa) to zagrażające życiu powikłanie zakażenia, które w ciągu kilku godzin może doprowadzić do niewydolności płuc, zmuszając pacjentów do wentylacji mechani cznej i zwiększając ryzyko zgonu. To badanie bada mało poznane białko wewnątrz komórek, zwane FGF13, i ujawnia, jak przyczynia się ono do napędzania wymykającego się spod kontroli stanu zapalnego oraz nadmiernego wykorzystania energii, które poważnie uszkadzają płuca podczas sepsy. Śledząc ten ukryty obwód regulacyjny, praca wskazuje nowe cele lekowe, które mogłyby złagodzić burzę w płucach bez wyłączania całego układu odpornościowego.
Ukryty czynnik uszkodzenia płuc podczas sepsy
Naukowcy zaczęli od porównania tkanki płucnej myszy i pacjentów z sepsą z tkanką od osobników bez sepsy. Zbadali rodzinę cząsteczek znanych jako czynniki wzrostu fibroblastów (FGF), które pomagają utrzymać zdrowie płuc. Wśród nich FGF13 wyróżniał się: jego poziomy były wyraźnie niższe w płucach pacjentów i zwierząt z sepsą. Gdy zespół zmapował lokalizację FGF13, okazało się, że występuje przede wszystkim w dwóch kluczowych typach komórek: komórkach śródbłonka wyściełających naczynia krwionośne oraz makrofagach — komórkach odpornościowych wyczuwających i wzmacniających stan zapalny. W płucach septycznych komórki śródbłonka i makrofagi pozytywne dla FGF13 były znacznie zredukowane, co sugeruje, że zmiany tego białka mogą wiązać się z ciężkim uszkodzeniem płuc.
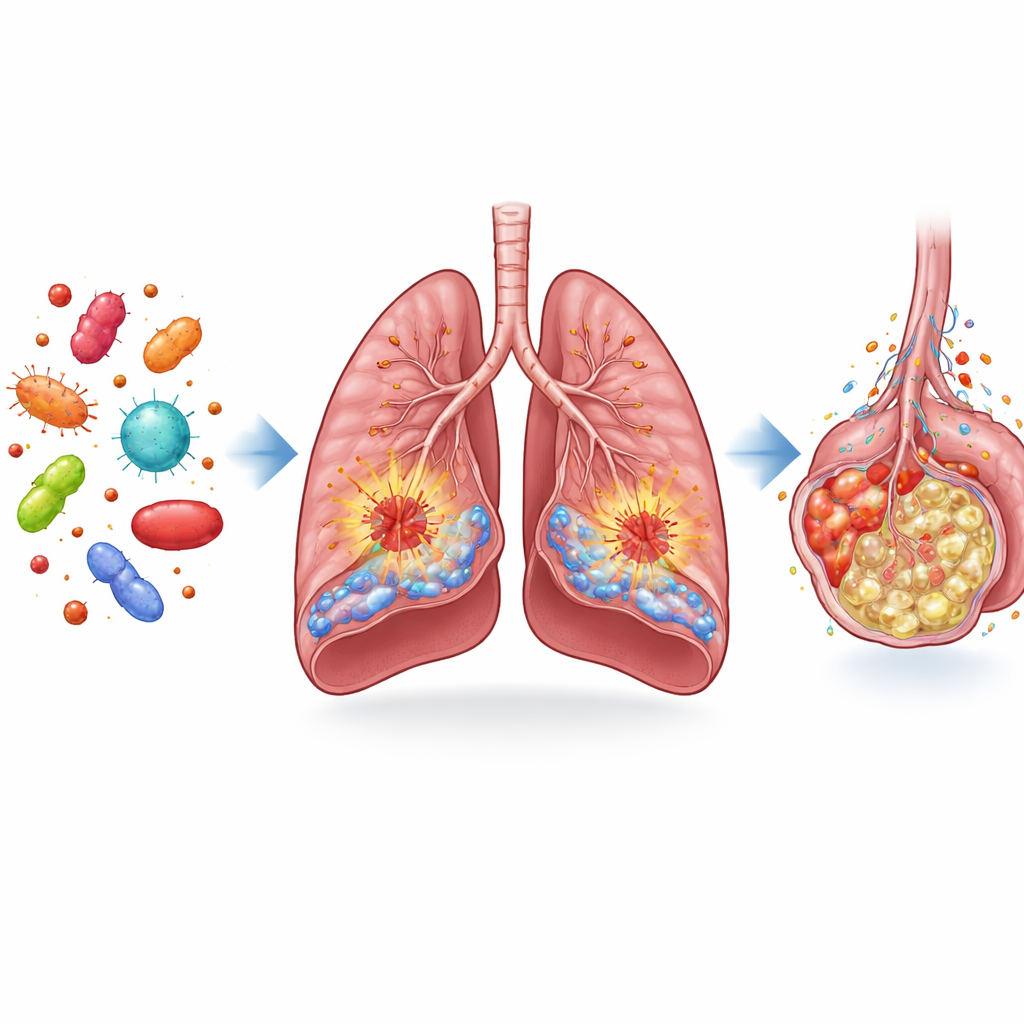
Jak FGF13 zamienia obrońców płuc w czynniki uszkodzenia
Aby sprawdzić, co FGF13 rzeczywiście robi, zespół użył narzędzi genetycznych u myszy, aby usunąć je z określonych komórek lub zmusić te komórki do wytwarzania go w nadmiarze. Gdy FGF13 zostało usunięte tylko w komórkach śródbłonka, myszy z sepsą miały mniej nieszczelne, mniej obrzęknięte płuca, mniej napływających komórek odpornościowych i lepsze przeżycie. Przeciwne skutki zaobserwowano, gdy komórki śródbłonka były zmodyfikowane do nadprodukcji FGF13: obrzęk płuc, krwawienia i nagromadzenie komórek zapalnych się nasiliły. Podobny obraz zaobserwowano w makrofagach. Myszy pozbawione FGF13 w tych komórkach wykazywały słabsze odpowiedzi zapalne i mniejsze uszkodzenie płuc, podczas gdy makrofagi nadmiernie produkujące FGF13 uwalniały więcej molekuł zapalnych i pogarszały uszkodzenia. W kulturach komórkowych obniżenie FGF13 sprawiało, że komórki naczyń krwionośnych i makrofagi były mniej „klejące się”, mniej zapalne i mniej toksyczne dla otoczenia.
Zapalne komórki przełączają się na tryb łaknący cukru
Komórki w stanie zapalnym, podobnie jak komórki nowotworowe, często zmieniają strategię energetyczną: zamiast wolnego spalania paliwa z użyciem tlenu, szybko rozkładają cukier w procesie zwanym aerobową glikolizą, produkując kwas mlekowy. Autorzy odkryli, że FGF13 silnie sprzyja temu przełączeniu. U myszy septycznych pozbawionych FGF13 w komórkach śródbłonka lub makrofagach poziom mleczanu we krwi był niższy. W hodowlach komórek komórki z obniżonym FGF13 pobierały mniej glukozy i wytwarzały mniej mleczanu po stymulacji zapalnej, natomiast komórki z dodatkowym FGF13 wykazywały wzmocnioną glikolizę. Gdy badacze zablokowali glikolizę lekiem, prozapalny efekt nadmiaru FGF13 został w dużej mierze stłumiony, co łączy szkodliwą rolę tej cząsteczki bezpośrednio z programem spalania cukru.
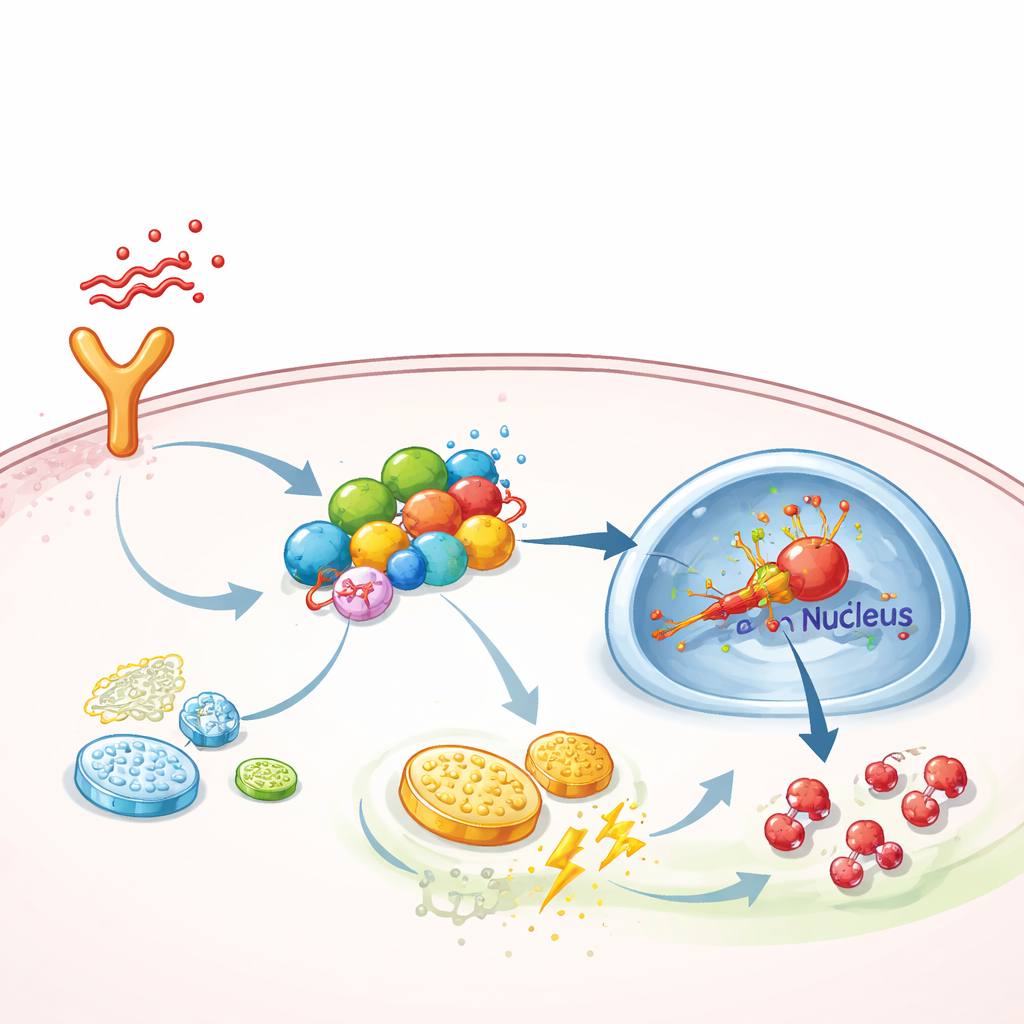
Szablon molekularny wzmacniający sygnalizację zapalną
Głębiej drążąc, zespół zapytał, jak FGF13 skłania komórki do tej wysokoprądowej przemiany metabolicznej. Odkryli, że FGF13 fizycznie wiąże się z kilkoma białkami sygnałowymi tworzącymi łańcuch od receptorów powierzchniowych do jądra komórkowego — konkretnie szlakiem TAK1–MEK–ERK, który jest znany z aktywacji kluczowego regulatora odpowiedzi na niski poziom tlenu, HIF-1α. FGF13 działa jak rusztowanie, utrzymując te komponenty razem, dzięki czemu sygnały przemieszczają się wydajniej. Gdy FGF13 było zmniejszone, aktywacja ERK i HIF-1α malała, a glikoliza słabła; gdy FGF13 było zwiększone, szlak stawał się nadaktywowany. Nadekspresja HIF-1α u myszy zniweczyła ochronny efekt usunięcia FGF13, podczas gdy selektywny inhibitor ERK, SCH772984, zneutralizował uszkodzenia spowodowane nadprodukcją FGF13 i poprawił stan płuc u zwierząt z sepsą.
Co to znaczy dla przyszłych terapii sepsy
Dla czytelnika niebędącego specjalistą kluczowy przekaz jest taki: septyczne uszkodzenie płuc to nie przypadkowe niszczenie tkanki; napędza je konkretny obwód molekularny w komórkach śródbłonka i makrofagach. FGF13 znajduje się w centrum tego obwodu, pomagając zmontować centrum sygnalizacyjne, które zmusza komórki do trybu łapczywej konsumpcji cukru i silnej odpowiedzi zapalnej. Chociaż poziomy FGF13 spadają podczas sepsy — prawdopodobnie jako część szerszej odpowiedzi na stres — to badanie pokazuje, że pozostające białko nadal jest silnym czynnikiem szkodliwym. Hamując partnerów sygnałowych FGF13 lub przemianę glikolityczną, którą promuje, może być możliwe zmniejszenie obrzęku, przecieków i zapalenia w płucach bez paraliżowania zdolności organizmu do walki z infekcją. Praca ta wskazuje zatem FGF13 oraz oś ERK–HIF‑1α–glikoliza jako obiecujące kierunki do opracowania bardziej precyzyjnych i bezpieczniejszych terapii w niewydolności płuc związanej z sepsą.
Cytowanie: Zhu, J., Wang, J., Jiang, C. et al. FGF 13 functions as a regulator of the ERK/aerobic glycolysis axis in the inflammatory state during septic lung injury. Nat Commun 17, 2383 (2026). https://doi.org/10.1038/s41467-026-69014-x
Słowa kluczowe: septyczne uszkodzenie płuc, FGF13, zapalenie śródbłonka, aerobowa glikoliza, sygnalizacja ERK