Clear Sky Science · pl
Połączona terapia celowana i epigenetyczna wzmacnia odporność przeciwnowotworową przez stabilizację ekspresji MHCI zależnej od GATA6 w gruczolakoraku przewodów trzustkowych
Dlaczego te badania są istotne dla raka trzustki
Gruczolakorak przewodów trzustkowych jest jednym z najbardziej śmiertelnych nowotworów, w dużej mierze dlatego, że ukrywa się przed układem odpornościowym i opiera się na działanie większości leków. To badanie ujawnia szczególny stan komórki nowotworowej, napędzany przez gen GATA6, który sprawia, że komórki raka trzustki są bardziej widoczne dla ataku immunologicznego. Autorzy pokazują także, jak połączenie dwóch typów leków może zachować ten podatny stan i zwiększyć zdolność cytotoksycznych limfocytów T do atakowania guzów w modelach doświadczalnych.
Stan komórek nowotworowych, który zaprasza układ odpornościowy
Nie wszystkie komórki raka trzustki zachowują się tak samo. Niektóre zachowują porządek i tożsamość nabłonkową, podczas gdy inne przechodzą w bardziej ruchliwy, agresywny stan przypominający mezenchymalny. Czynnik transkrypcyjny GATA6 pomaga utrzymać tożsamość nabłonkową i jest związany z lepszymi wynikami u pacjentów. W dużych kohortach pacjentów guzy o wysokim poziomie GATA6 zawierały więcej komórek układu odpornościowego, w tym CD8 — „zabójczych” limfocytów T, niż guzy z małą ilością lub bez GATA6. Zaawansowane obrazowanie przestrzenne próbek ludzkich guzów wykazało, że komórki nowotworowe pozytywne dla GATA6 częściej znajdowały się obok komórek CD8 i wykazywały wyższy poziom cząsteczki MHCI, która działa jak flaga pokazująca limfocytom, co znajduje się w komórce. Te obserwacje sugerują, że GATA6 oznacza populację komórek nowotworowych, która jest naturalnie bardziej widoczna dla układu odpornościowego. 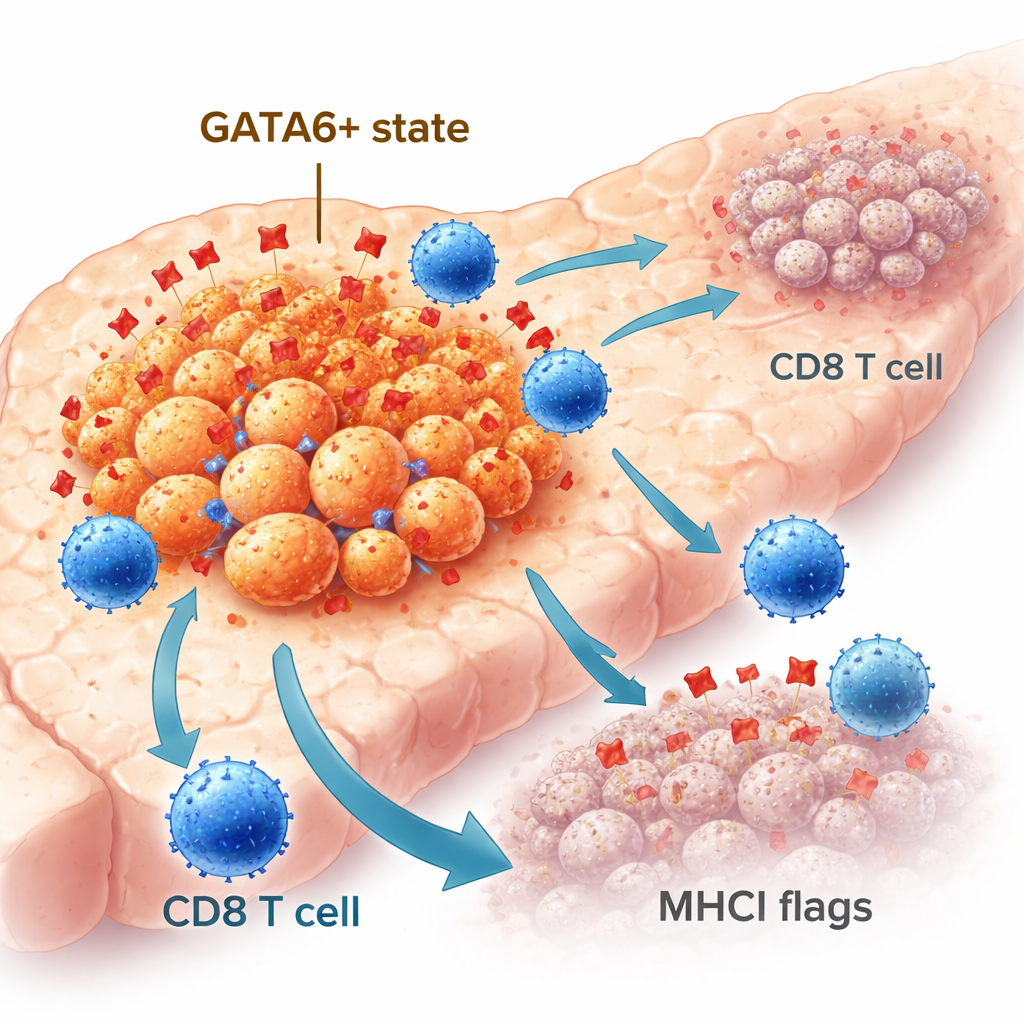
Terapia celowana zwiększająca widoczność guza — ale z kosztem
Zespół zapytał następnie, czy leki celowane mogą dodatkowo zwiększyć tę widoczność. Skoncentrowano się na inhibitorach MEK, klasie leków blokujących szlak sygnałowy wzrostu często aktywny w raku trzustki. W liniach komórkowych raka trzustki myszy oraz w guzach hodowanych u myszy i w ksenograftach uzyskanych od pacjentów, blokada MEK zwiększała poziom MHCI na powierzchni komórek nowotworowych o wysokim poziomie GATA6, czyniąc je potencjalnie lepszym celem dla limfocytów T. Gdy guzy o wysokim GATA6 leczono inhibitorami MEK u myszy, wzrost guza spowolnił, poziom MHCI wzrósł, a do guzów dostało się więcej komórek CD8 niosących cząsteczki cytotoksyczne. Bezpośrednie blokowanie GATA6, zarówno przez wyciszenie genu, jak i szybkie degradowanie białka, znosiło to indukowane przez inhibitor MEK podwyższenie MHCI i wynikającą z tego kontrolę guza, pokazując, że GATA6 jest niezbędne dla tego korzystnego efektu.
Jak guzy adaptują się: przejście w trudniejszy do zabicia stan
Jednak historia miała zwrot akcji. Długotrwałe leczenie inhibitorami MEK spowodowało, że wiele komórek nowotworowych przeszło ze stanu nabłonkowego z wysokim GATA6 w bardziej mezenchymalny stan z niskim poziomem GATA6, związany z opornością na leczenie. Zarówno w modelach mysich, jak i ksenograftach od pacjentów, guzy leczone inhibitorem MEK ostatecznie wykazywały mniej komórek pozytywnych dla GATA6, więcej markerów przejścia nabłonkowo-mezenchymalnego i ogólnie słabszy, krócej utrzymujący się efekt. Chociaż pojedyncze komórki z wysokim GATA6 nadal zwiększały ekspresję MHCI w odpowiedzi na lek, kurczenie się tej populacji ograniczało całkowitą poprawę prezentacji antygenów nowotworowych, co pomaga wyjaśnić, dlaczego same inhibitory MEK zawiodły w badaniach klinicznych raka trzustki.
Leki epigenetyczne, które utrzymują guzy w wrażliwym stanie
Aby przeciwdziałać tej ucieczce adaptacyjnej, badacze zwrócili się ku inhibitcom deacetylaz histonowych, czyli inhibitorom HDAC, klasie leków epigenetycznych znanych z wpływu na tożsamość komórek i ich widoczność immunologiczną. W hodowlach komórkowych i modelach mysich połączenie inhibitorów MEK z inhibitorami HDAC klasy I, takimi jak domatinostat, przywróciło ekspresję GATA6, która została stłumiona przez blokadę MEK, odwróciło cechy przejścia nabłonkowo-mezenchymalnego i dodatkowo zwiększyło poziomy MHCI na komórkach nowotworowych. Co ważne, ta terapia skojarzona prowadziła do silniejszej infiltracji i aktywacji komórek CD8 oraz do większej śmierci komórek nowotworowych w ortotopowych guzach mysich i w genetycznie modyfikowanym modelu myszy, który wiernie odwzorowuje ludzki rak trzustki. Usunięcie komórek CD8 znosiło znaczną część korzyści, potwierdzając, że to połączenie działa w dużej mierze przez wzmocnienie funkcji „zabójczych” limfocytów T.
W kierunku mądrzejszych terapii łączonych dla trudnego nowotworu
Syntetyzując te ustalenia, badanie proponuje strategię, w której celowana blokada MEK i epigenetyczna blokada HDAC są stosowane razem, aby ustabilizować stan komórek nowotworowych zależny od GATA6, charakteryzujący się wysoką zawartością MHCI i w związku z tym wysoce rozpoznawalny dla układu odpornościowego. Poprzez zarówno zwiększenie liczby komórek pozytywnych dla GATA6, jak i wzmocnienie ich „flag” MHCI, kombinacja sprzyja głębszej infiltracji komórek CD8, silniejszej aktywności cytotoksycznej i dłuższemu przeżyciu w agresywnych modelach mysich raka trzustki. Choć inhibitory HDAC mogą powodować istotne działania niepożądane i prace te mają charakter przedkliniczny, badania te wskazują drogę dla przyszłych podejść terapeutycznych, które mogłyby łączyć leki celowane na szlaki sygnałowe z ostro dobranymi modyfikatorami epigenetycznymi, by uczynić guzy trzustki bardziej podatnymi na własne mechanizmy obronne organizmu. 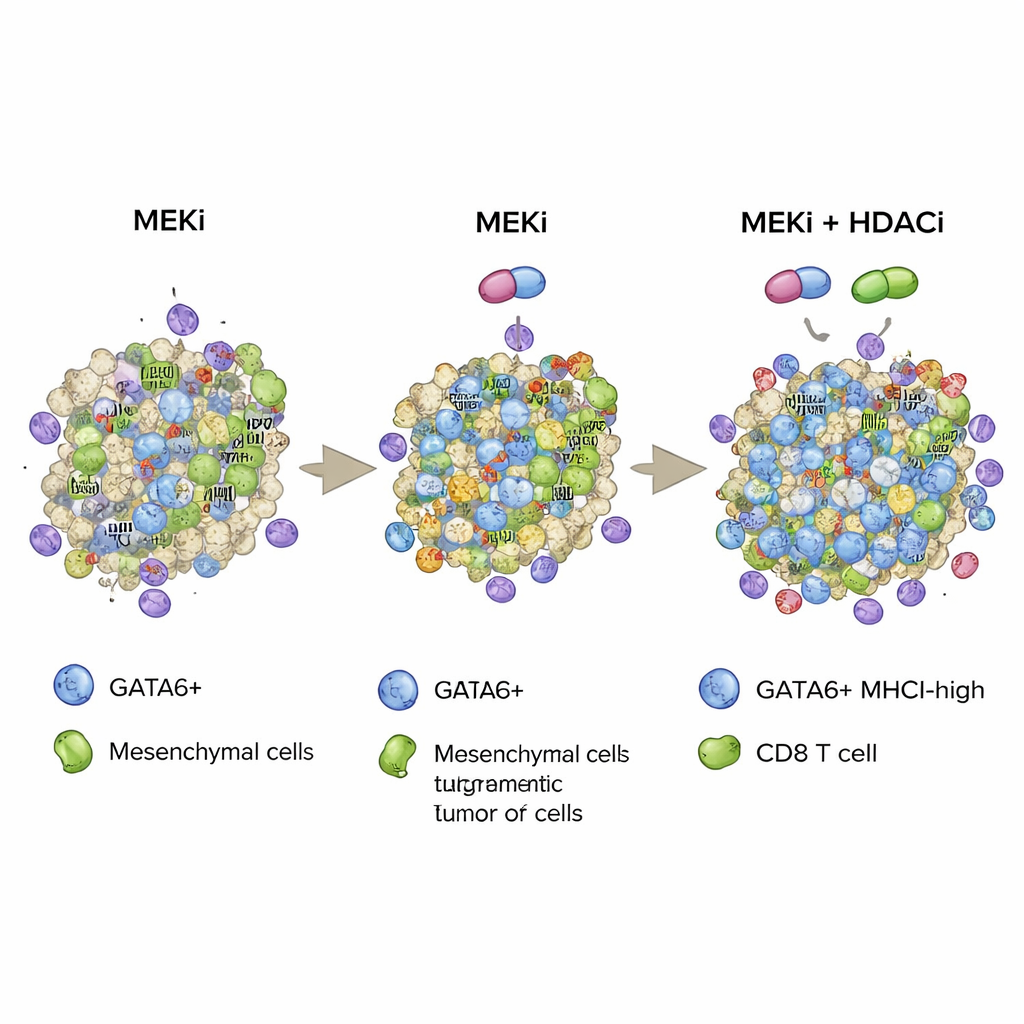
Cytowanie: Peng, J., Yang, J., Antonopoulou, G. et al. Combined targeted and epigenetic-based therapy enhances antitumor immunity by stabilizing GATA6-dependent MHCI expression in pancreatic ductal adenocarcinoma. Nat Commun 17, 1476 (2026). https://doi.org/10.1038/s41467-026-69013-y
Słowa kluczowe: rak trzustki, odporność przeciwnowotworowa, GATA6, inhibitor MEK, inhibitor HDAC