Clear Sky Science · pl
AACRNL przekształcony z czynnika wirulencji w epigenetycznego pasożyta napędzającego ekspansję genomu u eukariontów wolno żyjących
Kiedy stare toksyny uczą się nowych sztuczek
Nasze genomy nie są cichymi instrukcjami. To zatłoczone areny, na których geny, wirusy i ruchome DNA nieustannie walczą o miejsce i kontrolę. To badanie odsłania zaskakującego uczestnika tej walki: białko, które zaczynało jako toksyna używana przez mikroby do ataku na gospodarzy, lecz zostało przekształcone w organizmach wolno żyjących w coś w rodzaju „epigenetycznego pasożyta”, co pomaga powiększać jego własny ślad w genomie.
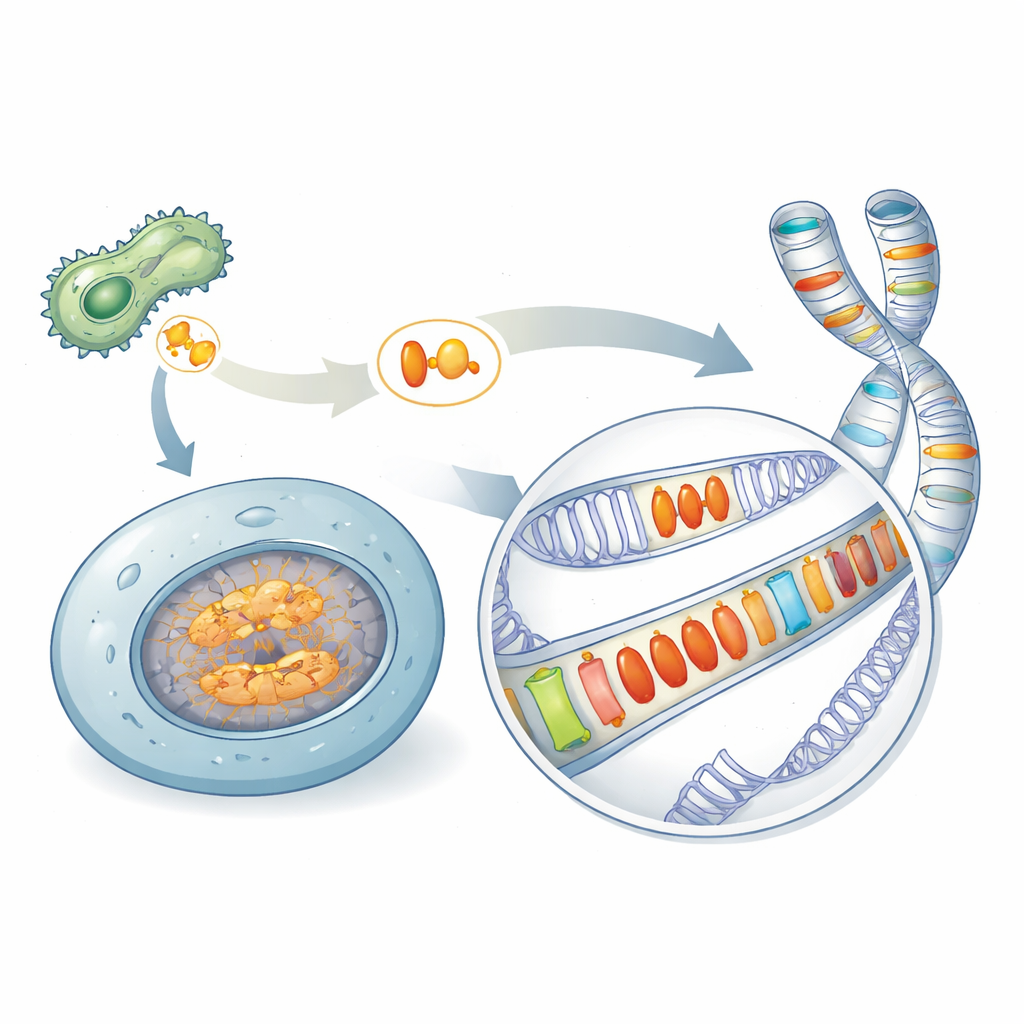
Ukryte dziedzictwo mikrobnych broni
Wiele chorobotwórczych mikrobów polega na wyspecjalizowanych białkach, zwanych efektorami, by sabotować mechanizmy obronne organizmów, które zakażają. Jedna znana rodzina, nazywana Crinklerami, uważana była za obecną jedynie w patogenach. Poprzez przeszukanie szerokiego spektrum gatunków autorzy odkryli spokrewnione białka — tutaj sklasyfikowane jako AACRNL — w nieoczekiwanych miejscach, w tym w gąbkach, koralach, jeżowcach i rybach kostnych, które nie są klasycznymi patogenami. Te białka AACRNL zachowują toksyczne jądro zdolne chemicznie modyfikować inne białka, ale ich przednia „sekcja dostarczająca”, której patogeny używają do wtargnięcia do komórek gospodarza, w dużej mierze się rozpadła. Ta zmiana strukturalna sugeruje przesunięcie od atakowania innych organizmów do działania wewnątrz własnych komórek gospodarza.
Samolubne przełączenie w genomie
U ryb kostnych geny AACRNL występują w wielu kopiach rozsianych po różnych chromosomach. Porównując sąsiednie odcinki DNA, badacze wykazali, że niektóre linie AACRNL przestały się kopiować, podczas gdy inne rozmnażały się z pomocą pobliskich ruchomych segmentów DNA zwanych transpozonami. Te transpozony działają jak genomowe wahadła: gdy się przemieszczają lub duplikują, mogą zabrać za sobą AACRNL. W efekcie powstaje mozaika powtórzonych kopii AACRNL osadzonych w sekwencjach transpozonów — znak rozpoznawczy genu, który rozprzestrzenia się dla własnej korzyści, a niekoniecznie dla dobra gospodarza.
Łamanie wyciszacza genomu
Zwykle komórki trzymają takie ruchome DNA na krótkiej smyczy. Jednym z kluczowych zabezpieczeń jest chemiczny znacznik na białkach opakowujących DNA, znany jako H3K27me3, który pomaga utrzymywać niebezpieczne lub hałaśliwe regiony w stanie wyciszenia. Autorzy odkryli, że aktywna wersja AACRNL u ryb, nazwana AACRNLβ, potrafi chemicznie modyfikować EZH2 — enzym nakładający ten represyjny znacznik. Gdy AACRNLβ modyfikuje EZH2, ilość H3K27me3 przy jego własnym locus genowym i przy pobliskich transpozonach spada, lokalne DNA się otwiera, a zarówno AACRNLβ, jak i jego transpozonowi sąsiedzi zaczynają być silniej eksprymowani. W praktyce białko naciska własny przycisk „włącz” i zwalnia hamulce na tych samych elementach ruchomych, które mogą przenieść je w nowe miejsca genomu.
Unikanie strażników układu odpornościowego
Uwolnienie transpozonów i nietypowej aktywności genetycznej grozi przyciągnięciem uwagi układu odpornościowego. Badanie pokazuje, że AACRNLβ radzi sobie z tym problemem również. Przyłącza mały chemiczny znacznik do TRAF6 — centralnego białka‑węzła, które pomaga w uruchamianiu sygnałów przeciwwirusowych i zapalnych. Oznaczony w ten sposób TRAF6 staje się mniej stabilny i coraz częściej tagowany do usunięcia przez komórkowe mechanizmy recyklingu. Przy osłabieniu tego węzła sygnałowego kluczowe ścieżki obronne działają słabiej, tworząc bardziej tolerancyjne środowisko, w którym AACRNLβ i powiązane z nim transpozony mogą przetrwać i kopiować się z mniejszym ryzykiem wykrycia.
Delikatny wyścig zbrojeń wewnątrz komórki
Opowieść nie kończy się na niekontrolowanym rozwoju AACRNLβ. To samo białko TRAF6, które jest celem AACRNLβ, potrafi z kolei przyłączać własne znaczniki do AACRNLβ, sygnalizując, by pasożytnicze białko zostało zniszczone. Ta wymiana przypomina molekularny wyścig zbrojeń: AACRNLβ wykorzystuje chemię pochodzącą od toksyn, by wyginać chromatynę i odporność na swoją korzyść, podczas gdy białka gospodarza odgryzają się, degradując je i utrzymując jego aktywność jako sporadyczną i ryzykowną. Autorzy twierdzą, że to szarpanie pozwoliło dawnej broni mikrobnej przetrwać jako samolubny lokator genomów organizmów wolno żyjących, powiększając zawartość DNA i przekształcając zasady konfliktu genetycznego od środka.
Dlaczego to ma znaczenie dla naszego obrazu genomów
Dla osoby niebędącej specjalistą kluczowy przekaz jest taki: genomy to nie tylko plany zoptymalizowane pod kątem przetrwania gospodarza. Skrywają też oportunistów. Ta praca pokazuje, że nawet klasyczne toksyny mogą zostać udomowione na takie elementy, wykorzystując swoją pierwotną destrukcyjną chemię, by przekradać się przez epigenetyczne zamki i alarmy immunologiczne oraz rozprzestrzeniać się w genomie w toku ewolucji. Zrozumienie tego rodzaju ukrytego konfliktu pomaga wyjaśnić, dlaczego genomy są tak duże, złożone i dynamiczne — i sugeruje, że inne „emerytowane” toksyny mogą potajemnie przepisywać DNA u wielu gatunków, być może także u nas samych.
Cytowanie: Xu, T., Geng, S., Lv, X. et al. AACRNL evolved from virulence factor to epigenetic parasite driving genome expansion in free-living eukaryotes. Nat Commun 17, 2130 (2026). https://doi.org/10.1038/s41467-026-69012-z
Słowa kluczowe: samolubne elementy genetyczne, ewolucja genomu, regulacja epigenetyczna, transpozony, odporność wrodzona