Clear Sky Science · pl
Wielo‑składnikowa synergistyczna immobilizacja poprzez strategie in-situ i dynamicznej wymiany do budowy hierarchicznych biofarmaceutyków
Dlaczego budowanie mądrzejszych leków ma znaczenie
Wiele z najpotężniejszych współczesnych leków to duże, delikatne cząsteczki biologiczne, takie jak białka i enzymy. Potrafią zwalczać raka, zabijać szkodliwe bakterie i przyspieszać gojenie, ale są łatwo uszkadzane i trudno je dostarczyć w odpowiednie miejsce w organizmie. W artykule opisano nowy sposób „pakowania” kilku z tych wrażliwych składników razem wewnątrz ochronnego, gąbczastego materiału, tak aby mogły działać kolejno, z większą siłą i mniejszymi efektami ubocznymi.
Przekształcanie kryształu w molekularny blok mieszkalny
Naukowcy zaczynają od specjalnego porowatego materiału zbudowanego z jonów metali i niewielkich organicznych elementów konstrukcyjnych. Zachowuje się on nieco jak maleńki, elastyczny blok mieszkalny pełen pokoi i korytarzy. Pokazują, że ta rama, nazwana zeolitycznym szkieletem pirymidynowym, może rosnąć wokół białek tak, że białka zostają zabezpieczone wewnątrz kryształu. To „in‑situ” unieruchomienie nie miażdży ani nie dezaktywuje białek, a staranne obrazowanie potwierdza, że są równomiernie rozmieszczone w całym wnętrzu, niczym lokatorzy zajmujący wszystkie piętra budynku.
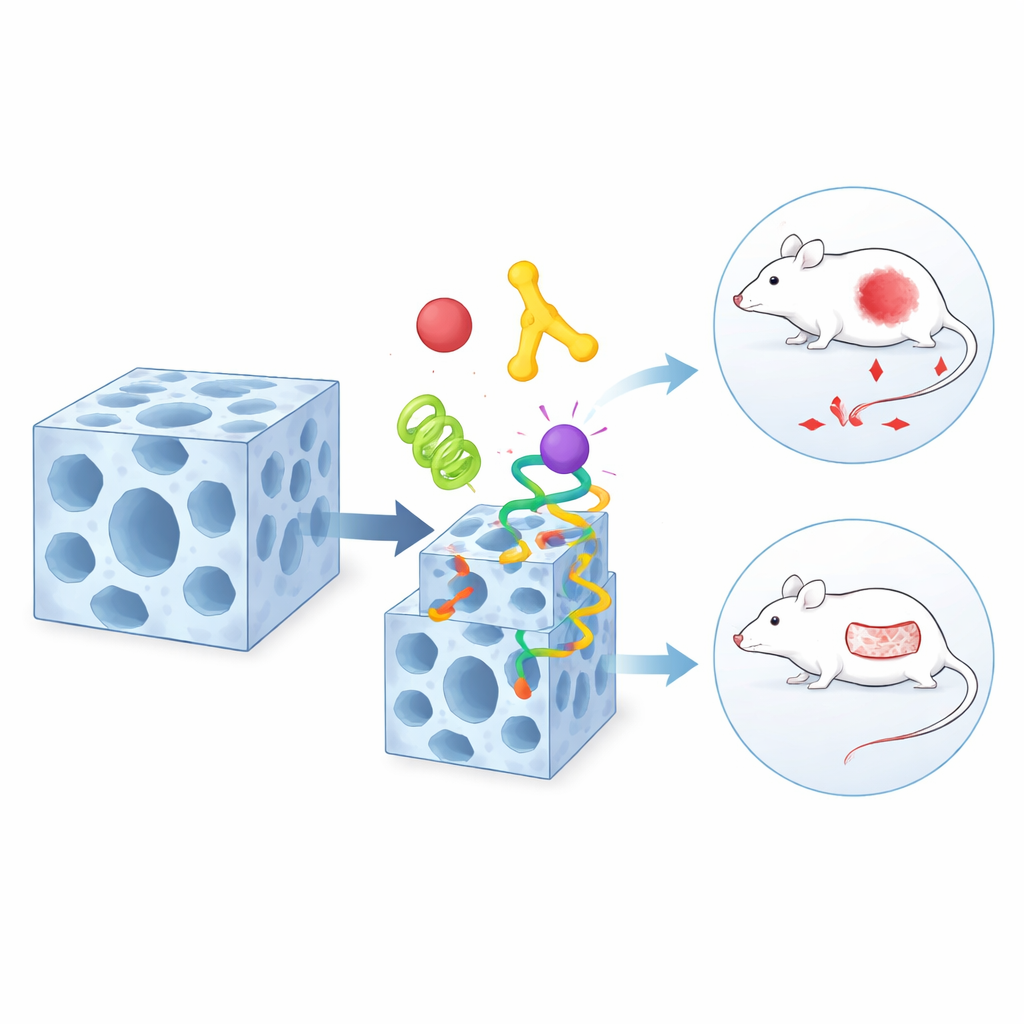
Gospodarz zmieniający kształt do dekorowania powierzchni
Ten sam materiał ma zaskakującą drugą właściwość: może odwracalnie zmieniać swoją wewnętrzną strukturę po wystawieniu na działanie określonych rozpuszczalników lub wody. Podczas tego łagodnego przekształcenia niektóre chemiczne wiązania w szkielecie poluzowują się, a następnie na nowo się tworzą. Zespół odkrył, że konkretne grupy chemiczne na powierzchni białek — takie jak występujące w pewnych aminokwasach — mogą wykorzystać ten moment osłabienia. Tymczasowo konkurują z oryginalnymi elementami konstrukcyjnymi ramy i wślizgują się w nowo powstałe „defekty” blisko powierzchni. W rezultacie warstwa białek zostaje zakotwiczona głównie na zewnątrz kryształu, podczas gdy wewnętrzne pozostają na miejscu. Ten proces dynamicznej wymiany pozwala naukowcom zdecydować, które składniki znajdują się głęboko wewnątrz, a które zdobią zewnętrzną powłokę.
Projektowanie enzymatycznych linii montażowych
Mając kontrolę nad przestrzeniami wewnętrznymi i zewnętrznymi, autorzy budują maleńkie enzymatyczne „linie montażowe”. W jednym przykładzie enzym przekształcający cukier w reaktywny produkt pośredni zostaje zamknięty wewnątrz ramy, podczas gdy drugi enzym, który bezpiecznie rozkłada ten produkt, jest umieszczony blisko powierzchni. Takie wewnętrzno‑zewnętrzne rozmieszczenie przyspiesza reakcję i zwiększa jej wydajność w porównaniu z tradycyjnymi projektami typu rdzeń‑powłoka czy przypadkowymi mieszaninami enzymów. Ponieważ zewnętrzne enzymy są łatwiej dostępne dla reagentów, a szkodliwy produkt pośredni jest szybko usuwany, system pozostaje aktywny przez wiele cykli i lepiej znosi wysoką temperaturę, trudne warunki oraz wielokrotne użycie.
Sprytne pakiety przeciwnowotworowe i przeciwbakteryjne
Prawdziwa siła tego podejścia ujawnia się w zastosowaniach medycznych. Zespół łączy białko kierujące do guza, enzym zużywający glukozę i standardowy lek chemioterapeutyczny w jednej, warstwowej cząstce. Element celujący na powierzchni prowadzi cząstkę do komórek nowotworowych, enzym odcina ich zapas energii poprzez zużycie lokalnego cukru, a lek małocząsteczkowy zadaje dodatkowy śmiertelny cios. U myszy z wszczepionymi ludzkimi guzami ten trzyczęściowy pakiet zmniejsza guzy znacznie skuteczniej niż którykolwiek ze składników osobno lub prościej zorganizowane mieszaniny. W odrębnym projekcie autorzy dostosowują ramę do zakażonych ran skóry, umieszczając peptyd przeciwbakteryjny i enzym remodelujący tkankę w różnych regionach tego samego nośnika. W modelach szczurów te cząstki znacząco redukują zakażenie i przyspieszają zamykanie trudnych ran w porównaniu z konwencjonalnymi terapiami.

Jak ta praca posuwa medycynę do przodu
Dla osoby niebędącej specjalistą kluczowe przesłanie jest takie: badanie przemienia pojedynczy porowaty kryształ w programowalny dom dla wielu rodzajów molekuł terapeutycznych. Decydując, kto mieszka wewnątrz, kto znajduje się na powierzchni i w jakim stosunku, badacze mogą zorganizować stopniowe terapie — najpierw kierowanie, potem atak, następnie naprawa — wewnątrz jednego maleńkiego obiektu. Ta strategia nie tylko chroni delikatne leki biologiczne, lecz także umożliwia im współdziałanie, co prowadzi do silniejszych, bardziej precyzyjnych terapii przeciwnowotworowych i przeciwbakteryjnych. Te same zasady projektowe można dostosować do wielu przyszłych „inteligentnych leków”, które wymagają, by wiele składników współdziałało we właściwym miejscu i czasie.
Cytowanie: Yang, M., Meng, X., Shi, R. et al. Multicomponent synergistic immobilization via in-situ and dynamic exchange strategies for constructing hierarchical biopharmaceuticals. Nat Commun 17, 2208 (2026). https://doi.org/10.1038/s41467-026-69009-8
Słowa kluczowe: metal-organiczne struktury porowate, immobilizacja enzymów, nanomedycyna przeciwnowotworowa, gojenie ran, dostarczanie biofarmaceutyków