Clear Sky Science · pl
Macierz zewnątrzkomórkowa pośredniczy w tworzeniu klastrów krążących komórek nowotworowych w przerzutach potrójnie ujemnego raka piersi
Jak zbuntowane komórki raka piersi łączą siły we krwi
Gdy rak piersi się rozsiewa, często dzieje się tak dlatego, że pojedyncze komórki nowotworowe dostają się do krwiobiegu i osadzają guzy w odległych narządach. To badanie stawia pozornie proste pytanie o daleko idące konsekwencje: jak najbardziej agresywne komórki raka piersi, które utraciły swoje zwykłe „rzepy” łączące je ze sobą, nadal potrafią podróżować w zwartch klastrach — i dlaczego to czyni je tak zabójczymi?
Lepsza, lepka osłonka cukrowa zastępująca klasyczny klej między komórkami
Autorzy koncentrują się na potrójnie ujemnym raku piersi (TNBC), szczególnie agresywnej postaci, która często zrzuca krążące komórki nowotworowe (CTC) do krwi. W wielu nowotworach klastry CTC są znacznie bardziej podatne na tworzenie przerzutów niż pojedyncze komórki. Zwykle takie klastry utrzymywane są przez adhezje międzykomórkowe nabłonka — specjalne kompleksy białkowe działające jak molekularne nitonitki łączące sąsiednie komórki. Jednak komórki TNBC często tracą te białka połączeniowe, co stawia paradoks: bez zwykłego kleju, co utrzymuje klastry w całości? Analiza dużych baz danych genów nowotworowych wykazała, że guzy TNBC są wzbogacone o geny związane z zewnętrznym szkieletem komórki, znanym jako macierz zewnątrzkomórkowa. Jednym z wyróżniających się genów jest HAS2, kodujący enzym produkujący hialuronan (HA) — długi, cukrowy polimer pokrywający komórki. Wysokie poziomy HAS2 i HA były silnie powiązane z agresywnymi, przerzutującymi cechami nowotworu.
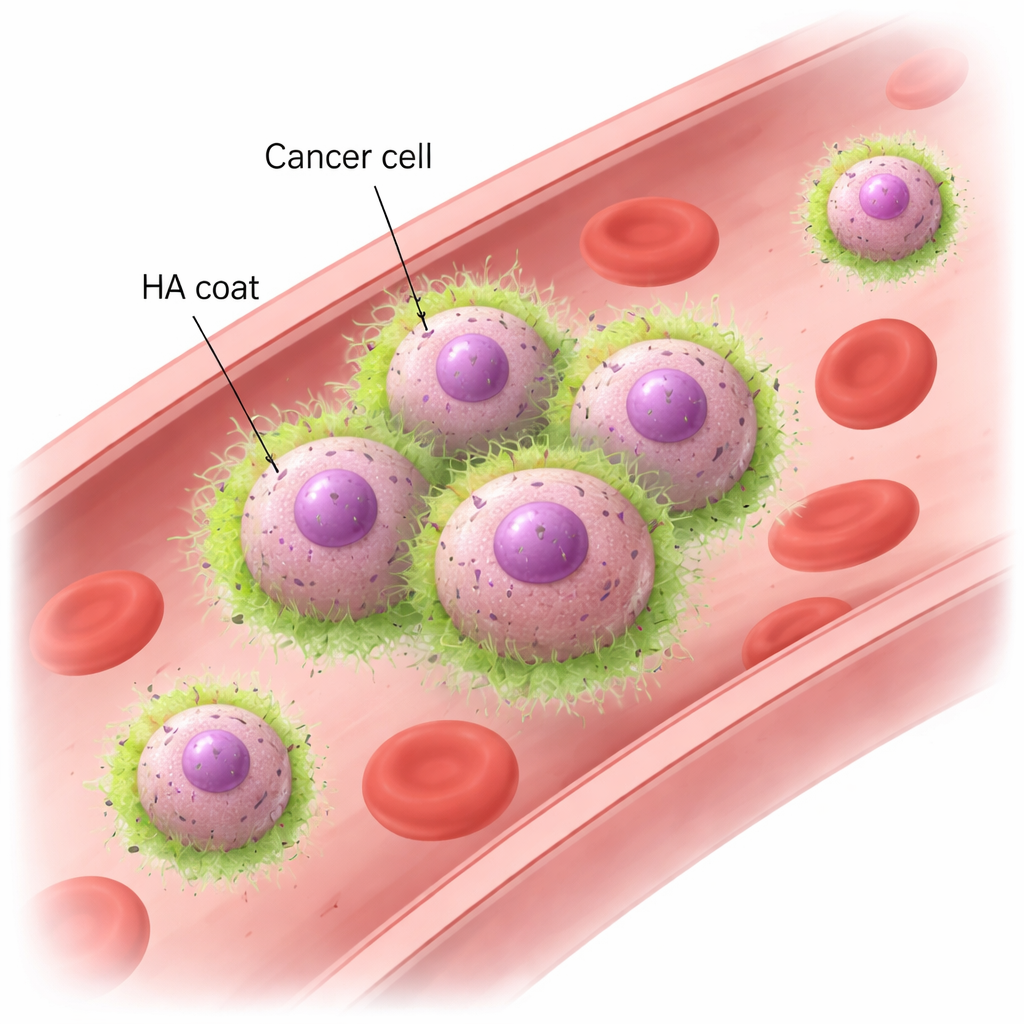
Hialuronan i CD44: nowy sposób trzymania się za ręce przez komórki
Wykorzystując modele mysie i ludzkie linie komórek raka piersi, zespół pokazał, że komórki TNBC zdolne do przerzutów szybko tworzą klastry po wystawieniu na wirowanie płynu naśladujące przepływ krwi. Te klastry pozostają nienaruszone nawet przy siłach porównywalnych z rzeczywistymi naczyniami, podczas gdy mniej agresywne komórki raka piersi rozpadają się i dryfują jako pojedyncze. Mikroskopia ujawniła, że komórki przerzutowe są owinięte „płaszczem” HA, który koncentruje się dokładnie w miejscach styku między komórkami. Usunięcie HA za pomocą enzymów lub zmniejszenie ekspresji HAS2 powodowało utratę zdolności do tworzenia klastrów pod wpływem przepływu, choć komórki nadal mogły osiadać razem, gdy pozostawiono je w spokoju. Kluczowym partnerem po stronie komórkowej jest CD44, powszechny receptor powierzchniowy wiążący HA. Komórki pozbawione CD44 nie utrzymywały HA na powierzchni ani nie tworzyły klastrów. Odwrotnie, komórki nie tworzące klastrów, zaprojektowane tak, by wytwarzały jednocześnie HAS2 i CD44, zyskały silną zdolność do grupowania się. Te eksperymenty wykazały, że interakcja HA z CD44 jest zarówno niezbędna, jak i wystarczająca, by komórki nowotworowe trzymały się razem w szybko płynącej krwi.
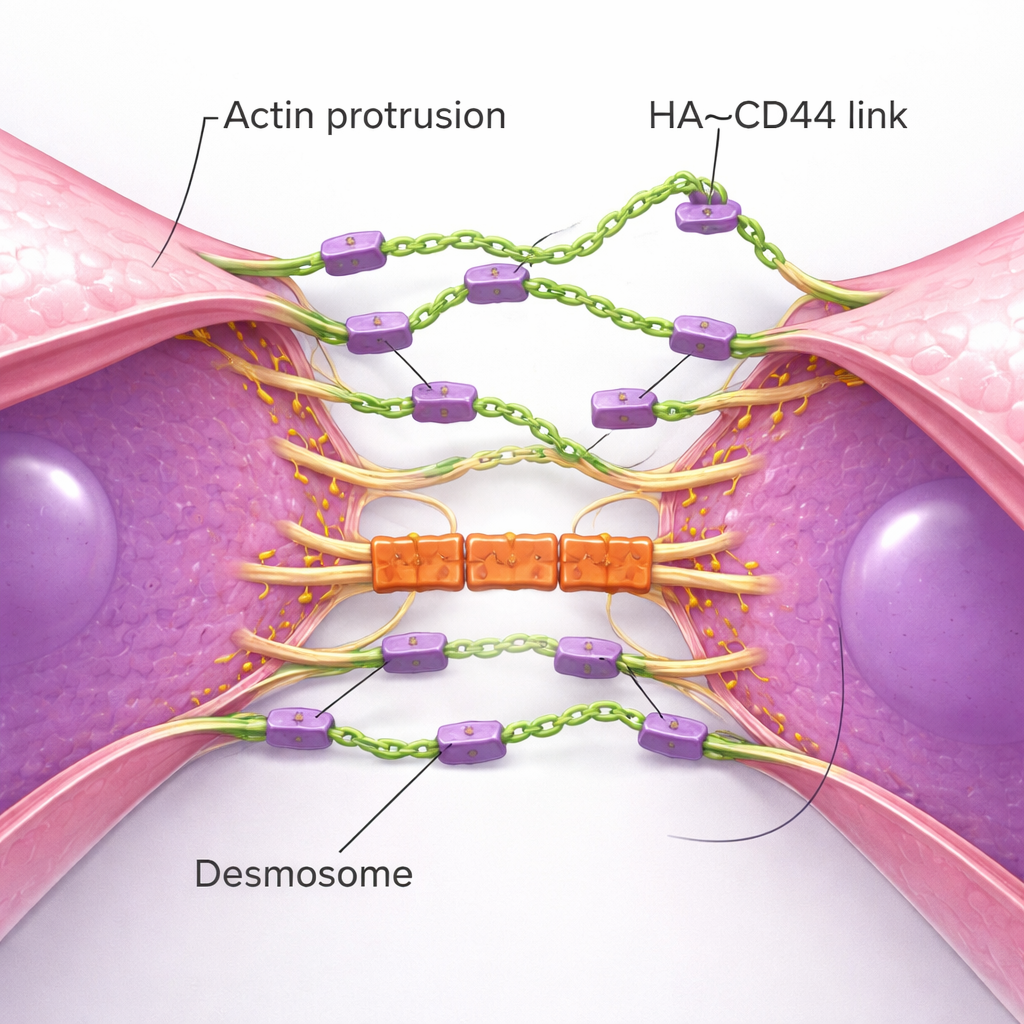
Maleńkie występy i mechaniczne zamki budują silne klastry
Obrazowanie o wysokiej rozdzielczości ujawniło fizyczną choreografię powstawania klastrów. Pojedyncze komórki TNBC wysuwają liczne cienkie wypustki błonowe oparte na aktynie — niczym czułki — obsypane CD44 i zakończone HA. Gdy dwie komórki driftują blisko siebie, te czułki spotykają się najpierw, tworząc początkowe mostki HA–CD44. Z czasem wypustki przesuwają się obok siebie, przyciągając całe ciała komórek bliżej, aż rozległe obszary błon leżą niemal równolegle. Proces ten przypomina tworzenie adhezji nabłonkowych w normalnych tkankach, lecz tutaj napędza go elastyczna osłonka cukrowa zamiast sztywnych łańcuchów białkowych. W miarę dojrzewania strefy kontaktu dołącza kolejny zestaw struktur: desmosomy, solidne połączenia łączące błony komórkowe z wewnętrznym szkieletem. Białka desmosomalne gromadzą się dopiero po ustanowieniu kontaktu opartego na HA i działają jak mechaniczne „zamki”, które pomagają klastrom opierać się siłom ścinającym przepływu krwi. Gdy komponenty desmosomów zostały zmniejszone, klastry powstawały, ale rozpadały się przy wyższym naprężeniu ścinającym.
Dlaczego grupowanie ma znaczenie dla przeżycia i przerzutów
System grupowania oparty na HA okazał się czymś więcej niż sposobem na pozostanie razem; bezpośrednio zwiększał przeżywalność. Przy długotrwałym symulowanym przepływie krwi klastry bogate w HA wykazywały znacznie niższe poziomy szkodliwych reaktywnych form tlenu i znacznie mniej śmierci komórkowej niż pozbawione HA pojedyncze komórki. W modelach mysich komórki TNBC pozbawione HAS2 generowały znacznie mniej CTC, tworzyły tylko drobne klastry i dawały dramatycznie mniej przerzutów w płucach — mimo że ich guzy pierwotne rosły równie dobrze. Gdy do myszy wstrzyknięto wcześniej przygotowane klastry kontrolnych i komórek niedoborowych w zakresie HAS2, komórki biedne w HA znacznie rzadziej skutecznie kolonizowały płuca. Co więcej, CTC pokryte HA mogły „rekrutować” inne komórki — zarówno komórki nowotworowe pozbawione HA, jak i normalne komórki układu odpornościowego, takie jak neutrofile — do mieszanych klastrów, o ile partnerzy ci ekspresjonowali CD44. Próbki krwi od pacjentek z przerzutowym TNBC wykazały ten sam wzorzec: CTC często nosiły płaszcz HA, z HA skoncentrowanym w punktach kontaktu między komórkami nowotworowymi oraz między komórkami nowotworowymi a komórkami nie-nowotworowymi.
Co to oznacza dla pacjentów i przyszłych terapii
Dla osoby niebędącej specjalistą główna konkluzja jest taka, że niektóre z najgroźniejszych komórek raka piersi nie podróżują samotnie, lecz jako maleńkie, współpracujące zespoły utrzymywane przez cukrową zewnętrzną powłokę i jej receptor, zamiast przez klasyczne „nitonitki” międzykomórkowe obecne w normalnych tkankach. Mechanizm oparty na HA–CD44 pomaga komórkom nowotworowym przetrwać trudne warunki przepływu krwi, łączyć się ze sobą i z komórkami wspierającymi we krwi oraz skuteczniej zasiedlać nowe guzy w odległych narządach. Hamowanie produkcji HA (np. przez blokowanie HAS2) lub blokowanie jego interakcji z CD44 mogłoby w teorii osłabić te klastry i utrudnić przerzutowanie TNBC, oferując nową strategię dla przyszłych terapii przeciwdziałających przerzutom.
Cytowanie: Bobkov, G.O., Patel, K.J., Lege, B.M. et al. Extracellular matrix mediates circulating tumor cell clustering in triple-negative breast cancer metastasis. Nat Commun 17, 1352 (2026). https://doi.org/10.1038/s41467-026-69007-w
Słowa kluczowe: potrójnie ujemny rak piersi, krążące komórki nowotworowe, hialuronan, CD44, przerzuty