Clear Sky Science · pl
Escherichia coli sprzyja przerzutom raka jelita grubego, utrzymując pętle enhancer–promoter poprzez uwalnianie neutrofilowych sieci zewnątrzkomórkowych
Jelitowe bakterie i sekretna autostrada nowotworu
Rak jelita grubego częściej zabija nie z powodu pierwotnego guza w jelicie, lecz dlatego, że komórki nowotworowe przemieszczają się do wątroby i tam osiadają. W badaniu odkryto niespodziewanego wspólnika tej podróży: powszechną bakterię jelitową, Escherichia coli. Śledząc łańcuch zdarzeń od bakterii w jelicie po agresywne guzy w wątrobie, badacze pokazują, jak mikroby, komórki odpornościowe i architektura DNA wewnątrz komórek nowotworowych współdziałają, napędzając przerzuty — i sugerują nowe sposoby przerwania tego łańcucha.
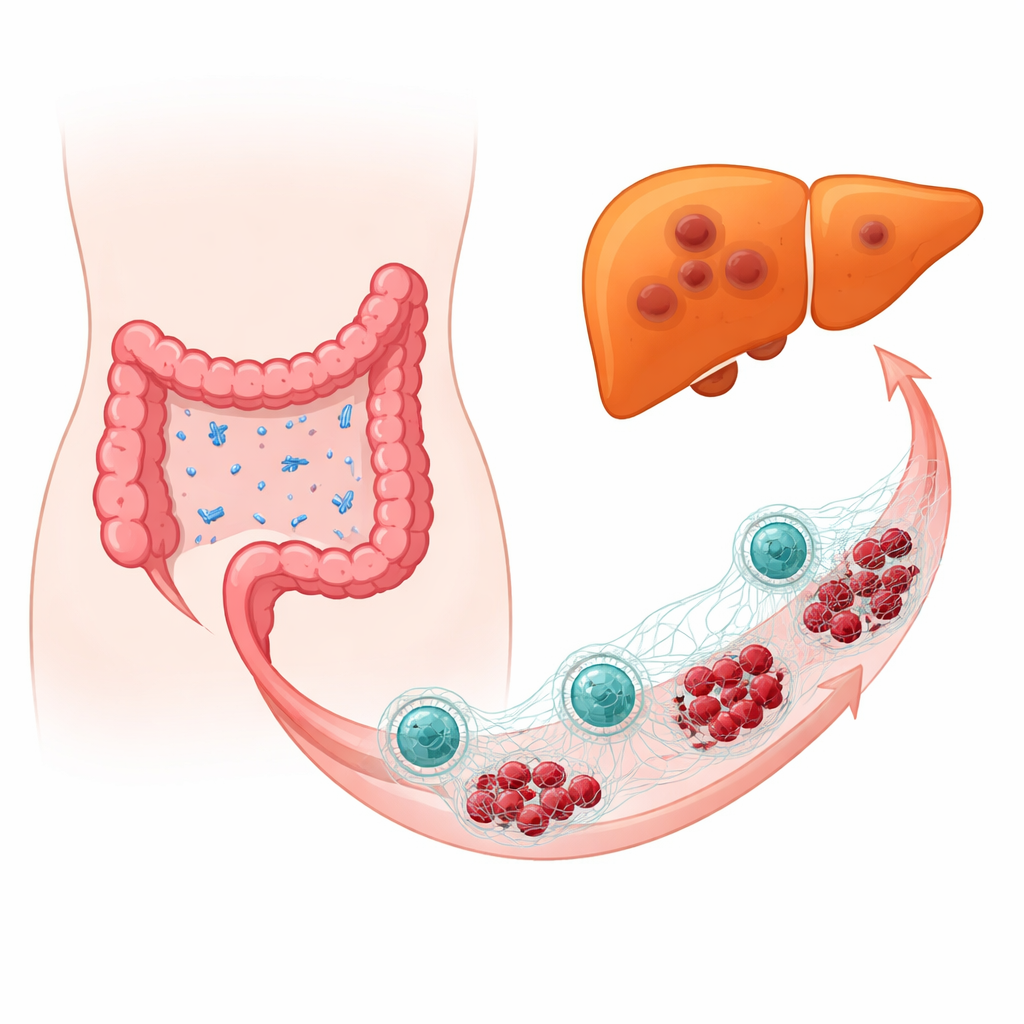
Gdy przyjazne bakterie stają się wrogami
Zespół przeanalizował próbki guzów od pacjentów z rakiem jelita grubego, porównując osoby, u których choroba rozsiało się do wątroby, z tymi, u których tego nie zaobserwowano. Przy użyciu wysokorozdzielczego profilowania DNA mikrobiomu stwierdzono, że E. coli była znacznie bardziej obfita w nowotworach, które już zasadziły się w wątrobie. W modelach mysich i u myszy z uodpornionym układem odpornościowym ludzkiego typu celowe wprowadzenie E. coli w pobliże guzów jelita grubego zwiększało rozmiar i częstość przerzutów do wątroby oraz skłaniało komórki nowotworowe do bardziej ruchomego, inwazyjnego fenotypu. Nawet gdy większość normalnej flory jelitowej usunięto antybiotykami i ponownie wprowadzono tylko E. coli, bakteria nadal wspierała wzrost i rozsiew guza, wskazując na rolę samej E. coli, a nie ogólnego zaburzenia mikrobiomu.
Sieci odpornościowe, które pomagają nowotworowi uciec
Neutrofile — komórki odpornościowe na pierwszym froncie, które zwykle atrapują i zabijają mikroby — okazały się kluczowymi pośrednikami. W odpowiedzi na E. coli neutrofile uwalniały sieci przypominające pajęczynę, zwane neutrofilowymi sieciami zewnątrzkomórkowymi, złożone z DNA i toksycznych białek. Sieci te mają wychwytywać bakterie, lecz w tym kontekście mimowolnie chroniły i wzmacniały komórki nowotworowe. Gdy badacze rozkładali sieci za pomocą enzymów lub blokowali kluczowe enzymy potrzebne do ich tworzenia, przerzuty do wątroby zmniejszały się, a guzy stawały się mniej agresywne. Wykluczenie neutrofili przynosiło podobny efekt ochronny, co wskazuje na paradoks: odpowiedź immunologiczna zwalczająca infekcję była wykorzystywana do wspierania rozsiewu raka.
Od sygnałów elektrycznych do przełączników genów
Jak lepka sieć DNA poza komórką nowotworową może zmieniać to, co dzieje się głęboko w jej jądrze? Odpowiedź tkwiła w wapniu, prostym jonie działającym jako sygnał elektryczny w komórkach. Badanie wykazało, że neutrofilowe sieci zwiększały poziom białka kanałowego TRPC1 na komórkach raka jelita grubego. TRPC1 umożliwiał napływ dodatkowego wapnia do komórki, co z kolei aktywowało regulator wrażliwy na wapń, NFATC3, tworząc pętlę samonapędzającą, która utrzymywała wysoki poziom TRPC1. Ten wzrost wapnia sprzyjał zespoleniu dwóch małych białek, S100A8 i S100A9, które następnie wiązały się z głównym białkiem kontrolującym wzrost, STAT3. Trio przenosiło się do jądra, gdzie dokonało czegoś szczególnie uderzającego: pomagało zginać i zapętlać DNA tak, by odległe regiony regulacyjne i miejsca startu genów zetknęły się, fizycznie stabilizując „pętle enhancer–promoter”, które nasilają ekspresję określonych genów.
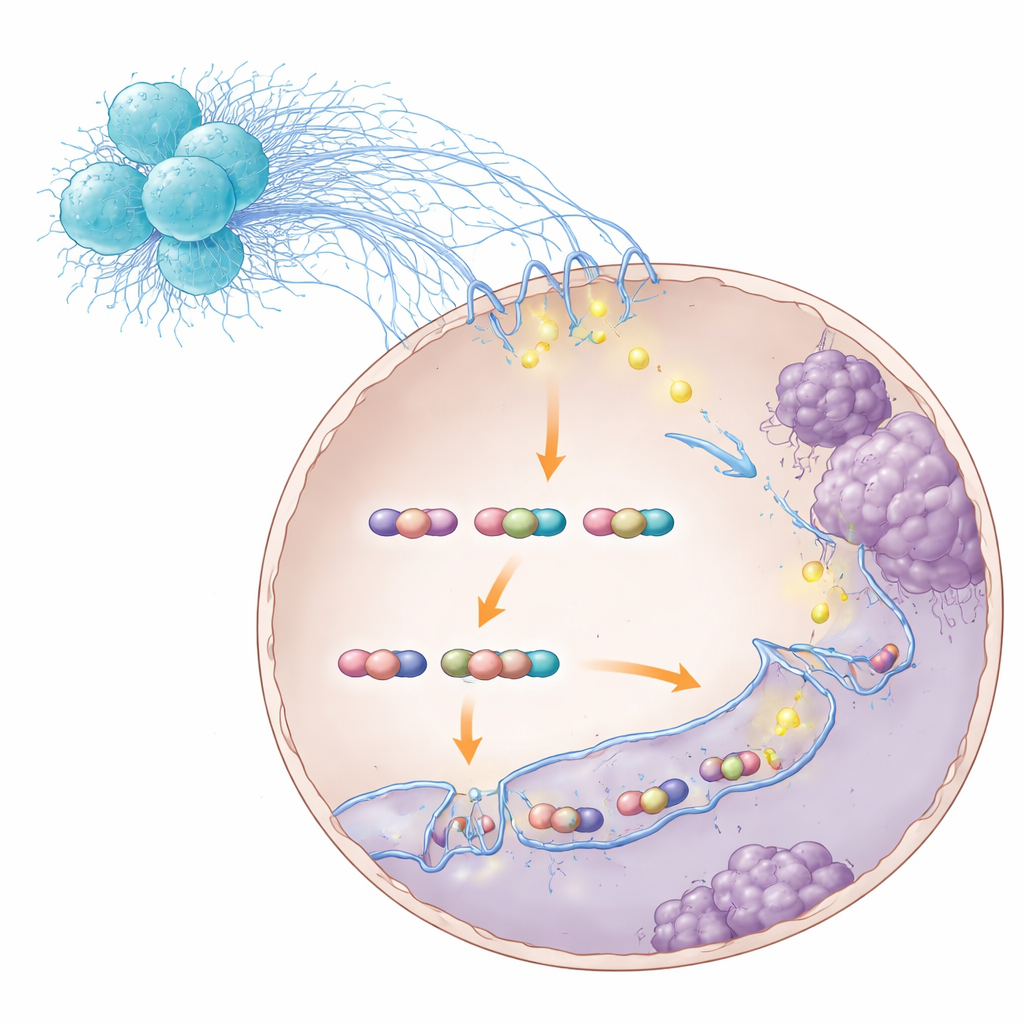
Przebudowa komórek nowotworowych pod kątem przerzutów
Mapując trójwymiarowe kontakty wzdłuż genomu, badacze odkryli, że kompleks STAT3–S100A8/9 promował pętle sprzyjające genom związanym z ruchem i inwazją komórek. Genem wyróżniającym się był TNS1, który sprawia, że komórki poluzowują połączenia i łatwiej migrują. Gdy kompleks STAT3–S100A8/9 został zaburzony, wiele z tych pętli osłabło lub zniknęło, poziomy TNS1 spadły, a komórki nowotworowe straciły część zdolności do inwazji i zasiewania wątroby. Co ważne, takie zakłócenie nie uniemożliwiało STAT3 całkowitego kontaktu z DNA — specyficznie destabilizowało architekturę pętlową, która nadmiernie napędza programy metastatyczne. W modelach zwierzęcych blokowanie różnych kroków w tym łańcuchu — od czujnika bakteryjnego RIPK2 w neutrofilach, przez S100A8/9, aż po sam STAT3 — zmniejszało przerzuty do wątroby i poprawiało przeżywalność.
Przerwać łańcuch między bakteriami a guzami
Dla czytelników nienależących do specjalistów kluczowa wiadomość jest taka, że powszechna bakteria jelitowa może pomagać rakowi jelita grubego w rozprzestrzenianiu się, najpierw prowokując komórki odpornościowe do formowania sieci DNA, a potem wykorzystując te sieci do uruchomienia napędzanego wapniem przekazu, który przebudowuje sposób, w jaki geny nowotworowe są włączane. Zamiast stosować szerokie spektrum antybiotyków, które mogą uszkodzić pożyteczne mikroby i osłabić immunoterapię przeciwnowotworową, wyniki wskazują na dokładniejsze cele leków: czujniki bakteryjne typu RIPK2, kaskadę TRPC1–wapń–S100A8/9 oraz pętle DNA napędzane przez STAT3, które blokują geny związane z przerzutami na wysokim poziomie. Przerwanie tego łańcucha na jednym lub kilku etapach może dać nową strategię zapobiegania przekształceniu miejscowego problemu jelit w śmiertelną chorobę w wątrobie.
Cytowanie: Pan, B., Yao, Y., Zhang, Z. et al. Escherichia coli promotes colorectal cancer metastasis by maintaining enhancer-promoter loops through releasing neutrophil extracellular traps. Nat Commun 17, 2290 (2026). https://doi.org/10.1038/s41467-026-69005-y
Słowa kluczowe: przerzuty raka jelita grubego, mikrobiom jelitowy, neutrofilowe sieci zewnątrzkomórkowe, szlak sygnałowy STAT3, epigenetyczna regulacja genów