Clear Sky Science · pl
Projektowanie inhibitorów kowalencyjnych wykazuje aktywność wobec form KRAS G12C związanych zarówno z GDP, jak i GTP
Dlaczego to ma znaczenie dla przyszłych terapii przeciwnowotworowych
Nowotwory napędzane mutacjami w genie KRAS od dawna uchodziły za jedne z najtrudniejszych do leczenia. Ostatnio nowe leki, które wyłączają jedną powszechną zmienioną postać, KRAS G12C, dotarły do pacjentów i zaczęły zmieniać ten obraz. Artykuł bada jeszcze bardziej ambitny pomysł: czy można zaprojektować leki blokujące KRAS G12C w obu jego głównych trybach funkcjonowania w komórce i czy to sprawiłoby, że leczenie nowotworów byłoby szybsze, silniejsze lub trwalsze?
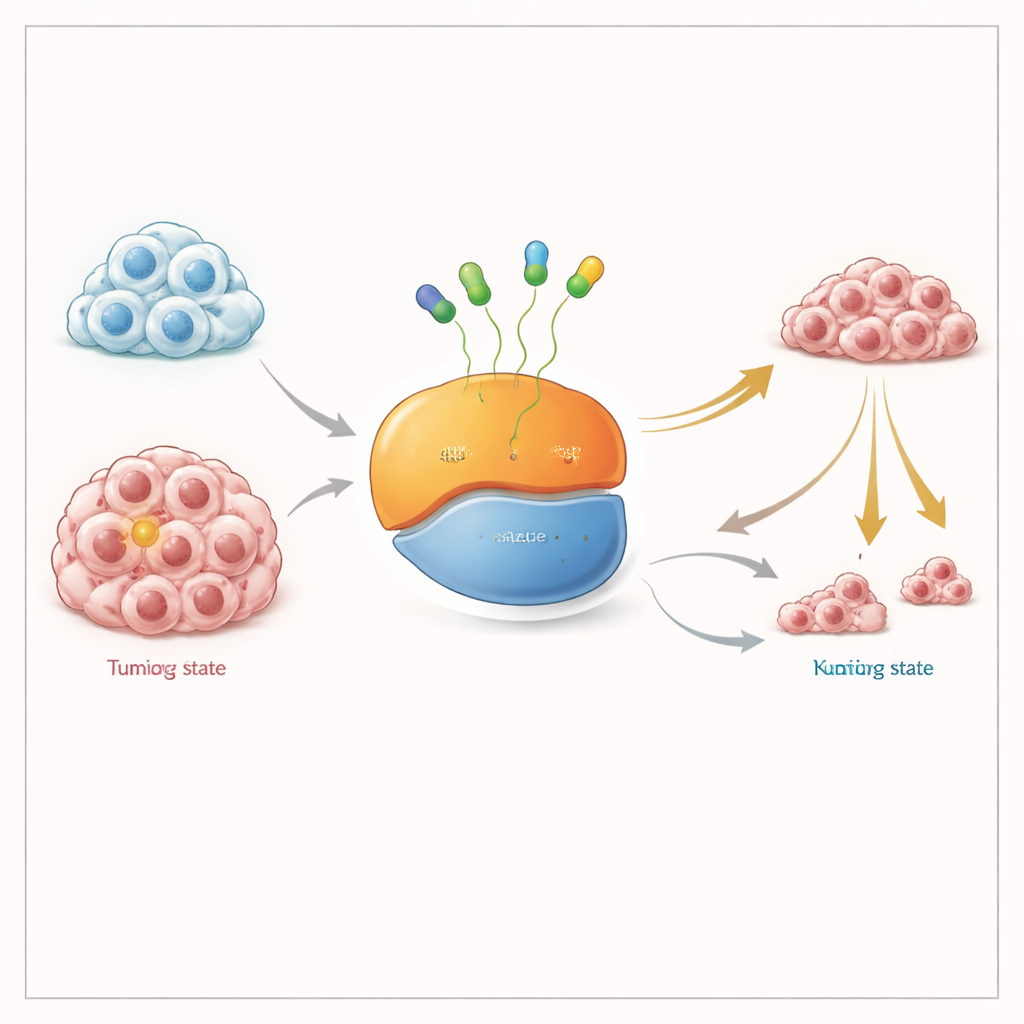
Wyłączanie molekularnego przełącznika w dwóch pozycjach
KRAS działa jak miniaturowy przełącznik włączający i wyłączający sygnały wzrostu komórkowego. Przełącza się między stanem „wyłączonym”, gdy wiąże GDP, a stanem „włączonym”, gdy wiąże GTP. Mutacja KRAS G12C powoduje częściowe przytrzymanie tego przełącznika w pozycji włączonej i napędza rozwój guza. Obecne leki zatwierdzone przez FDA wiążą się z formą nieaktywną i blokują ją; z czasem, gdy coraz więcej KRAS przechodzi przez tę formę, cała pula białka ulega unieczynnieniu. Wielu naukowców postulowało, że lek zdolny chwycić KRAS zarówno w formie aktywnej, jak i nieaktywnej powinien działać lepiej, zwłaszcza w guzach, które adaptują się, utrzymując więcej KRAS w stanie aktywnym.
Projektowanie nowego rodzaju molekularnego haka
Autorzy postanowili stworzyć takie dwufunkcyjne leki. Skupili się na małym rowku w pobliżu elastycznego obszaru KRAS zwanego Przełącznikiem II, gdzie wiążą się już obecne leki. Zamiast zmieniać siłę samego dopasowania do tego rowka, przeprojektowali część „głowicową” molekuły, która tworzy trwałe wiązanie chemiczne z mutantową cysteiną w pozycji 12. Poprzez modelowanie komputerowe i syntezę kilkudziesięciu wariantów odkryli specjalną trzyczęściową głowicę, która podchodzi do cysteiny pod nieco innym kątem. Ta subtelna zmiana tworzy wystarczająco dużo miejsca dla masywniejszej cząsteczki GTP, pozwalając nowym związkom wiązać się z KRAS niezależnie od tego, czy niesie GDP czy GTP. Testy biochemiczne potwierdziły, że związki wiodące mogą zaburzać interakcję KRAS z kluczowym partnerem sygnałowym RAF w obu stanach.
Obserwowanie, jak białko zmienia kształt
Aby zrozumieć, dlaczego te molekuły działały, zespół wyznaczył krystaliczne struktury o wysokiej rozdzielczości leku związanego z KRAS. Te migawki pokazały, że nowa głowica reaguje w nietypowym miejscu na szkielecie chemicznym, uwalniając atom fluoru i tworząc wiązanie kowalencyjne przy innym węglu niż w typowych lekach celujących cysteiny. Zmieniona chemia pomaga lekowi zmieścić się w kieszeni Przełącznika II nawet w obecności GTP. Struktury ujawniły także, że po związaniu inhibitora przesuwa on maleńką cząsteczkę wody i subtelnie przearanżowuje inną pętlę, Przełącznik I, która zwykle kontaktuje się z białkami przesyłającymi sygnał dalej. Ta allosteryczna zmiana przyciąga dwie aminokwasy bliżej siebie, tworząc ciasny most solny i deformując powierzchnię tak, że RAF nie może się już zadokować i przekazywać sygnałów wzrostu.
Szybkie wyłączenie, ale bez silniejszego efektu długoterminowego
Wykorzystując te strukturalne wglądy, badacze dopracowali dwa związki wiodące, które efektywnie i selektywnie wiążą się kowalencyjnie z KRAS G12C, jednocześnie w dużym stopniu oszczędzając inne białka zawierające cysteiny. W liniach komórkowych nowotworów te inhibitory dwustanowe szybko zablokowały kluczowy przekaźnik sygnalizacyjny znany jako ścieżka MAPK, co oceniano po utracie chemicznej etykiety na białku ERK i silnym zahamowaniu wzrostu komórek. Unieruchamiały KRAS w komórkach szybciej niż lek referencyjny celujący tylko w stan nieaktywny. W modelach guzów u myszy jeden z prowadzących związków wykazał dobrą dostępność po podaniu doustnym, szybko tworzył wiązania kowalencyjne z celem i zmniejszał guzy lub spowalniał ich wzrost. Jednak gdy porównano leki dwustanowe i te celujące tylko formę nieaktywną na dłuższą metę, obie klasy ostatecznie osiągnęły podobny poziom wyłączenia KRAS, hamowania ścieżki i kontroli guza.
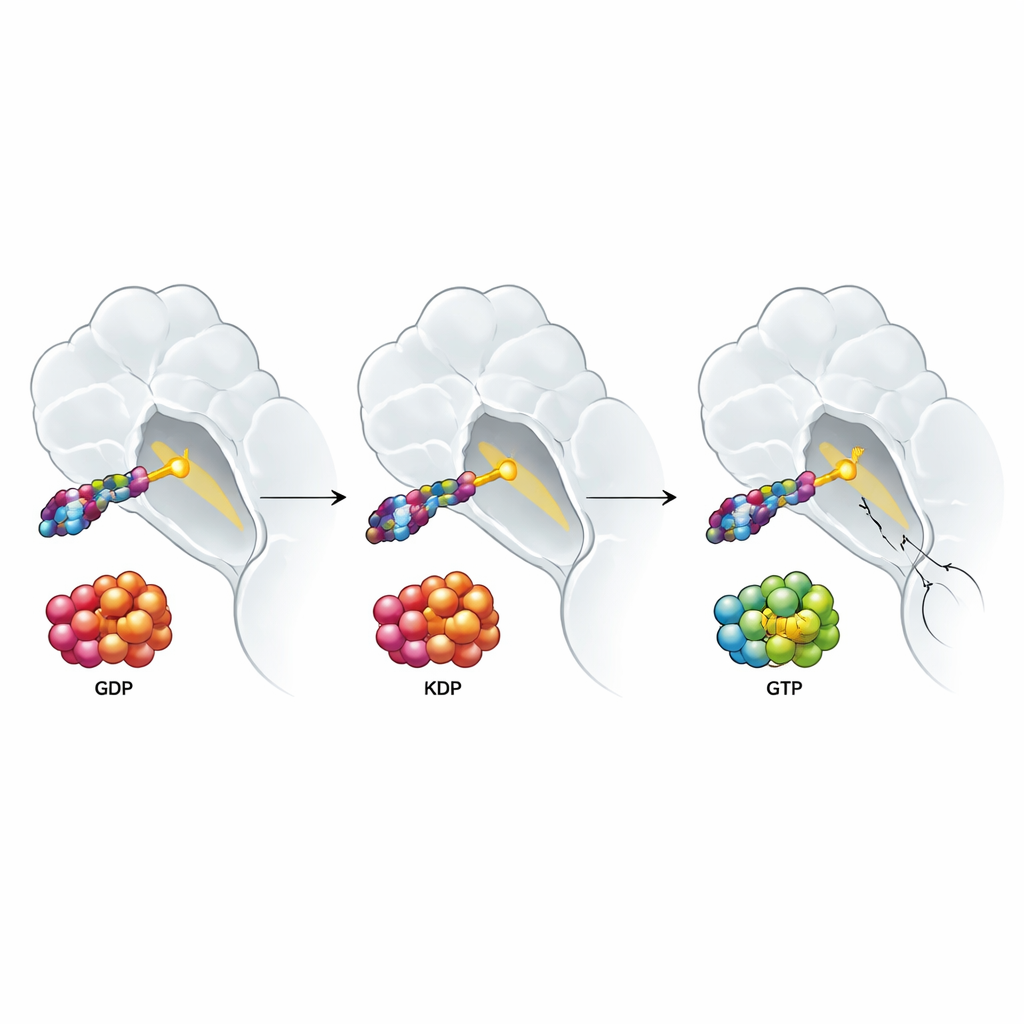
Dlaczego sygnały wzrostu ze środowiska guza nadal zwyciężają
Badanie zbadało też, jak sygnały ze środowiska guza wpływają na te leki. Czynniki wzrostu takie jak EGF i HGF, które są obfite wokół wielu guzów, popychają białka RAS w stronę aktywnej formy związanej z GTP i są znane z osłabiania odpowiedzi na terapie celowane. Można by oczekiwać, że lek wiążący aktywną formę KRAS G12C ominięłby ten problem. Zamiast tego autorzy odkryli, że zarówno inhibitory dwustanowe, jak i te celujące formę nieaktywną tracą moc w obecności takich czynników wzrostu. Szczegółowe eksperymenty wskazały zaskakującego winowajcę: aktywację normalnych, niemutowanych form RAS (H‑RAS i N‑RAS), które mogą ominąć KRAS G12C i utrzymać przepływ sygnałów wzrostu. Gdy badacze usunęli H‑RAS i N‑RAS w linii komórek raka płuca, oporność napędzana czynnikami wzrostu w dużej mierze zniknęła dla wszystkich typów leków ukierunkowanych na KRAS G12C, podczas gdy lek blokujący krok poniżej w ścieżce był w pierwszej kolejności mniej dotknięty.
Co to oznacza dla pacjentów i rozwoju leków
Podsumowując, praca pokazuje, że chemiczne i strukturalne jest wykonalne zbudowanie kowalencyjnych leków na KRAS G12C, które chwytają białko w obu jego stanach, i że inhibitory dwustanowe mogą szybciej wyłączać sygnalizację niż istniejące leki. Jednak szybkie zaangażowanie nie przełożyło się na wyraźnie lepszą kontrolę guza ani rozwiązanie problemu oporności wywołanej czynnikami wzrostu w modelach przedklinicznych. Dla pacjentów sugeruje to, że samo dodanie aktywności przeciwko aktywnej formie KRAS może nie wystarczyć; mogą być potrzebne strategie kombinacyjne, które również adresują inne członki rodziny RAS lub węzły sygnalizacyjne poniżej. Nowa głowica i przedstawiony tu plan strukturalny rozszerzają jednak zestaw narzędzi do celowania w KRAS i będą informować przyszłe generacje precyzyjnych terapii przeciwnowotworowych.
Cytowanie: Condakes, M.L., Zhang, Z., Danahy, D.B. et al. Covalent inhibitor design confers activity against both GDP- and GTP-bound forms of KRAS G12C. Nat Commun 17, 2233 (2026). https://doi.org/10.1038/s41467-026-69003-0
Słowa kluczowe: KRAS G12C, inhibitor kowalencyjny, inhibicja dwustanowa, sygnalizacja MAPK, oporność na leki