Clear Sky Science · pl
Genetycznie określony obwód korowo‑przedczołowo‑wzgórzowy reguluje sensoryczne i afektywne wymiary bólu u samców myszy
Dlaczego ten obwód mózgowy ma znaczenie dla bólu
Ból to nie tylko ostry ukłucie czy tępy ból; niesie też ładunek emocjonalny i może na lata przekształcać nastrój oraz zachowanie. Wielu pacjentów z bólem przewlekłym nie znajduje ulgi przy dostępnych lekach i często doświadcza poważnych skutków ubocznych. Badanie przeprowadzone na samcach myszy wyłania precyzyjnie zdefiniowany obwód mózgowy, który pozwala mózgowi zwiększać lub zmniejszać doświadczanie bólu — zarówno pod względem jego natężenia, jak i uciążliwości emocjonalnej. Mapując i manipulując tą ścieżką, praca wskazuje na nowe, bardziej ukierunkowane sposoby łagodzenia bólu przewlekłego bez polegania wyłącznie na tradycyjnych analgetykach.
Ukryta droga od „myślącego” mózgu do centrum bólu
Naukowcy skoncentrowali się na korze przedczołowej przyśrodkowej, obszarze czołowej części mózgu zaangażowanym w podejmowanie decyzji, emocje i kontrolę bólu, oraz na wzgórzu, głębokim centrum przekaźnikowym kształtującym zarówno intensywność, jak i nieprzyjemność bólu. Odkryli, że specyficzna grupa komórek w korze przedczołowej przyśrodkowej, oznaczona przez gen Foxp2, tworzy główną drogę wyjściową do wzgórza. Komórki te leżą głównie w najgłębszej warstwie kory i wysyłają długie włókna do określonych jąder wzgórza, unikając jednocześnie wielu innych typowych celów kory przedczołowej. Dzięki metodom trasowania i mapowania całego mózgu zespół wykazał, że neurony oznaczone Foxp2 silnie łączą się z trzema regionami wzgórza znanymi z wpływu na przetwarzanie bólu: jądrem parataenialnym, wzgórzem przyśrodkowo‑grzbietowym (mediodorsal) i wzgórzem brzuszno‑przyśrodkowym (ventromedial). 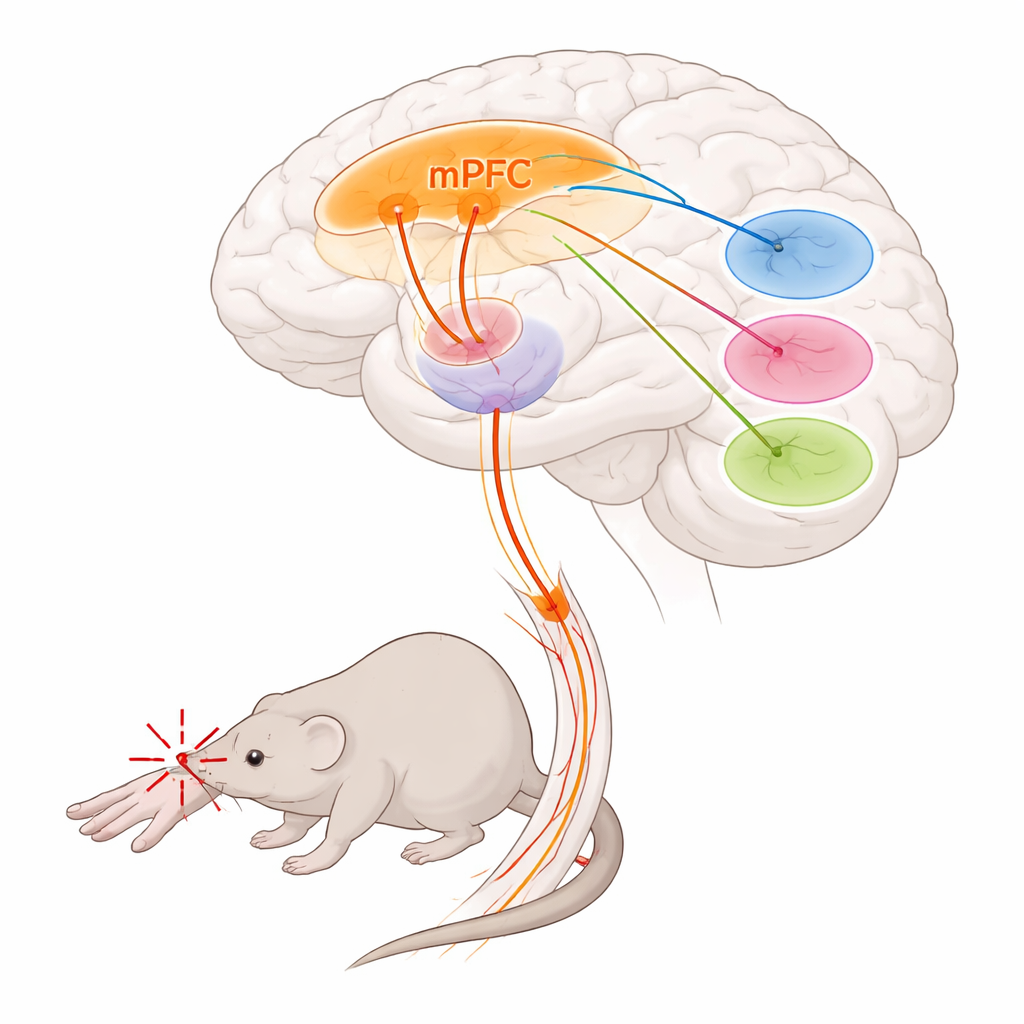
Gdy pojawia się ból, kluczowe centrum kontroli wycisza się
Aby sprawdzić, jak ta ścieżka zachowuje się podczas bólu, naukowcy wszczepili maleńkie soczewki nad korą przedczołową przyśrodkową i rejestrowali aktywność pojedynczych neuronów oznaczonych Foxp2 u czuwających myszy. Podczas krótkich mechanicznych szczypań, bólu chemicznego wywołanego formaliną oraz długotrwałego bólu zapalnego te komórki konsekwentnie się wyciszały: większość wykazywała mniej wybuchów aktywności podczas epizodów bólowych i w dniach po urazie zapalnym. To wyłączenie nie było subtelne; w niektórych warunkach ponad jedna trzecia do niemal połowy komórek stała się znacząco mniej aktywna. Odkrycie sugeruje, że stany bólowe ostre i przewlekłe mogą częściowo odzwierciedlać uciszenie naturalnego przedczołowego systemu hamującego, który w normalnych warunkach pomagałby utrzymywać ból pod kontrolą.
Włączanie i wyłączanie obwodu zmienia odczuwanie bólu
Zespół zapytał następnie, czy to wyciszenie jest tylko skutkiem bólu, czy też jego przyczyną. Przy użyciu narzędzi genetycznych albo długotrwale zablokowali wyjście neuronów oznaczonych Foxp2, albo krótko zwiększyli ich aktywność. Trwała inaktywacja uczyniła myszy bardziej wrażliwymi na dotyk i ciepło, co wskazuje, że ta ścieżka zwykle ogranicza napływ sygnałów bólowych. Przeciwnie, krótkotrwała aktywacja podniosła próg bólu, zmniejszyła lizanie w późnej fazie testu formalinowego (miara trwającego, zapalnego bólu) i sprawiła, że myszy wolały środowiska, w których obwód był włączony — co sygnalizuje ulgę od emocjonalnego ciężaru bólu. Świecenie światłem na konkretne odgałęzienia ścieżki wykazało, że projekcje do jądra parataenialnego zmniejszają zarówno wrażliwość fizyczną, jak i reakcje radzenia sobie, podczas gdy projekcje do wzgórza przyśrodkowo‑grzbietowego i brzuszno‑przyśrodkowego głównie modulują wymiary emocjonalne i behawioralne. Razem wyniki ukazują precyzyjnie rozdzielony schemat połączeń, w którym różne odgałęzienia tej samej populacji przedczołowej kontrolują odmienne aspekty doświadczenia bólu.
Chemiczne strojenie: cholinergiczne wzmocnienie dla ulgi w bólu
Co kontroluje te przedczołowe neurony przynoszące ulgę w bólu? Eksperymenty trasowania ujawniły silne wejście z obszaru cholinergicznego w podstawie przodomózgowia zwanym poziomą wstęgą diagonalną. Wiele komórek wysyłających sygnały z tego obszaru do neuronów oznaczonych Foxp2 używa acetylocholiny — przekaźnika zaangażowanego w uwagę i pobudzenie. Aktywacja tej projekcji cholinergicznej zmniejszyła wrażliwość mechaniczną i reakcje radzenia sobie oraz złagodziła nadreaktywność zapalną, choć nie przesunęła wyraźnie negatywnego tonu emocjonalnego bólu. Po stronie odbiorczej neurony oznaczone Foxp2 okazały się wzbogacone w szczególny typ receptora acetylocholiny, znany jako receptor nikotynowy α4β2. Bezpośrednie podanie selektywnego agonisty α4β2 do kory przedczołowej przyśrodkowej uczyniło myszy mniej wrażliwymi na bolesne ciepło i dotyk, nawet w stanach przewlekłego zapalenia, i zwiększyło aktywność neuronów oznaczonych Foxp2. Zablokowanie tych neuronów znosiło korzyść leku, co pokazuje, że ten receptor łagodzi ból specyficznie przez pobudzanie tego typu komórek. 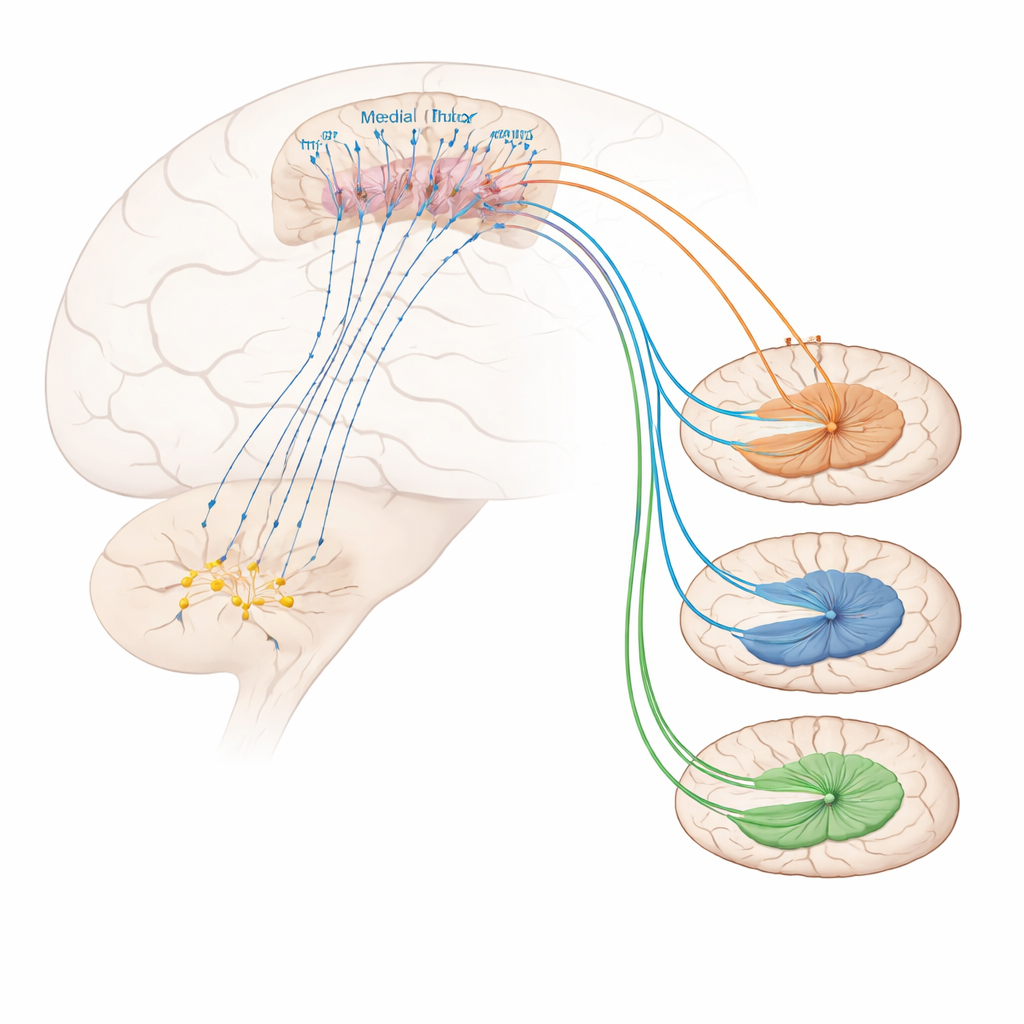
Co to oznacza dla przyszłych terapii bólu
Mówiąc prostymi słowami, badanie identyfikuje precyzyjną, trzyetapową ścieżkę: cholinergiczny „starter” w podstawie przodomózgowia, wyspecjalizowany zestaw komórek kontrolnych w korze przedczołowej przyśrodkowej oraz odrębne węzły przekaźnikowe we wzgórzu, które oddzielnie rządzą tym, jak silnie ból boli, jak bardzo jest on emocjonalnie nieprzyjemny i jak na niego reagujemy. Wygląda na to, że ból wycisza ten obwód; ponowne jego uruchomienie, albo przez bezpośrednią stymulację, albo przez ukierunkowanie receptorów acetylocholiny, zmniejsza zarówno pieczenie, jak i cierpienie związane z bólem zapalnym u samców myszy. Choć wciąż wiele pracy przed nami, aby przenieść te ustalenia na ludzi i inne formy bólu przewlekłego, wyniki wskazują obiecującą strategię: zamiast tłumić całe odczuwanie, przyszłe terapie mogłyby przywracać lub precyzyjnie regulować własne mózgowe obwody łagodzące ból, co może dać skuteczniejsze i potencjalnie bezpieczniejsze długoterminowe leczenie.
Cytowanie: Xie, G., Liu, Y., Qi, X. et al. A molecularly defined basalo-prefrontal-thalamic circuit regulates sensory and affective dimensions of pain in male mice. Nat Commun 17, 2134 (2026). https://doi.org/10.1038/s41467-026-69001-2
Słowa kluczowe: ból przewlekły, kora przedczołowa przyśrodkowa, wzgórze, sygnalizacja cholinergiczna, receptory nikotynowe