Clear Sky Science · pl
Indukowany przez mikrobiotę EI24 poprawia homeostazę, ale osłabia funkcję makrofagów pęcherzykowych poprzez regulację metabolizmu
Dlaczego mali strażnicy płuc mają znaczenie
Każdy oddech przynosi do płuc nie tylko tlen, ale też kurz, mikryby i inne intruzy. Patrolują tę granicę makrofagi pęcherzykowe — wyspecjalizowane komórki odpornościowe, które pochłaniają zanieczyszczenia i pomagają odpierać infekcje oraz nowotwory. To badanie ujawnia zaskakujący sposób, w jaki nasze codzienne mikroorganizmy „szkolą” te komórki: cząsteczka nazwana EI24, włączana przez mikrobiotę, utrzymuje strażników płuc w stanie stabilnym i wyciszonym, kosztem osłabienia ich zdolności do walki z wirusami i guzami. Zrozumienie tego kompromisu może otworzyć nowe drogi do bezpieczniejszych i skuteczniejszych immunoterapii.
Poznaj mieszkańców sprzątających płuca
Makrofagi pęcherzykowe osiadają w drobnych pęcherzykach płucnych, gdzie zachodzi wymiana gazowa. Żyją tam przez lata, odnawiając się i cicho usuwając surfaktant, martwe komórki i drobne cząstki, unikając przy tym niepotrzebnego zapalenia, które uszkodziłoby delikatną tkankę. Autorzy skupili się na białku o nazwie EI24, wcześniej powiązanym z odpowiedziami na stres komórkowy i recyklingiem komórkowym, ale słabo poznanym w kontekście odporności płuc. Odkryli, że spośród wielu typów makrofagów tkankowych w organizmie, makrofagi pęcherzykowe wykazują szczególnie wysoką ekspresję EI24, co sugeruje, że to białko może być kluczowe dla życia na odsłoniętej powierzchni płuc.
Stabilność kontra siła u obrońców płuc
Aby sprawdzić, co naprawdę robi EI24, badacze wychowali myszy pozbawione tego białka specyficznie w makrofagach. Zwierzęta te rozwijały się normalnie i wytwarzały prawidłową liczbę młodych prekursorów makrofagów w płucach, ale w miarę dojrzewania około połowa ich makrofagów pęcherzykowych znikała. Pozostałe komórki wykazywały wyraźne cechy zwiększonej śmierci komórkowej napędzanej klasycznym enzymem apoptotycznym, kaspazą-3. Tymczasem te nieliczne komórki nie były słabe: wykazywały bardziej „czuwający” profil, z wyższym pobieraniem bakterii w testach in vitro oraz silniejszą produkcją molekuł zapalnych przy stymulacji. Analizy genetyczne i chromatynowe pokazały, że setki genów zaangażowanych w prezentację antygenów, zabijanie komórek i reakcje zapalne były wzmocnione, podczas gdy szlaki regulacyjne zwykle hamujące aktywację zostały rozluźnione.
Wysoko nakręcony metabolizm z ukrytym kosztem
Dzięki głębszym badaniom zespół odkrył, że makrofagi pozbawione EI24 przebudowały swój metabolizm. Zamiast opierać się głównie na spokojnym, energooszczędnym stanie, wykazywały wyższe poziomy zarówno spalania cukrów (glikolizy), jak i produkcji energii w mitochondriach. Te wzmocnione szlaki energetyczne napędzały silniejsze odpowiedzi zapalne i bardziej intensywne pochłanianie drobnoustrojów oraz komórek nowotworowych. Jednak ten metaboliczny wyżyn również zwiększał powstawanie reaktywnych produktów ubocznych w mitochondriach, które z kolei aktywowały kaspazę-3 i popychały komórki w kierunku zaprogramowanej śmierci. Blokowanie tych szlaków metabolicznych lub neutralizowanie reaktywnych cząsteczek zmniejszało zarówno nadmierne zapalenie, jak i skłonność do obumierania, wiążąc ze sobą wykorzystanie energii przez komórkę, jej zdolność zabijania i długość życia.
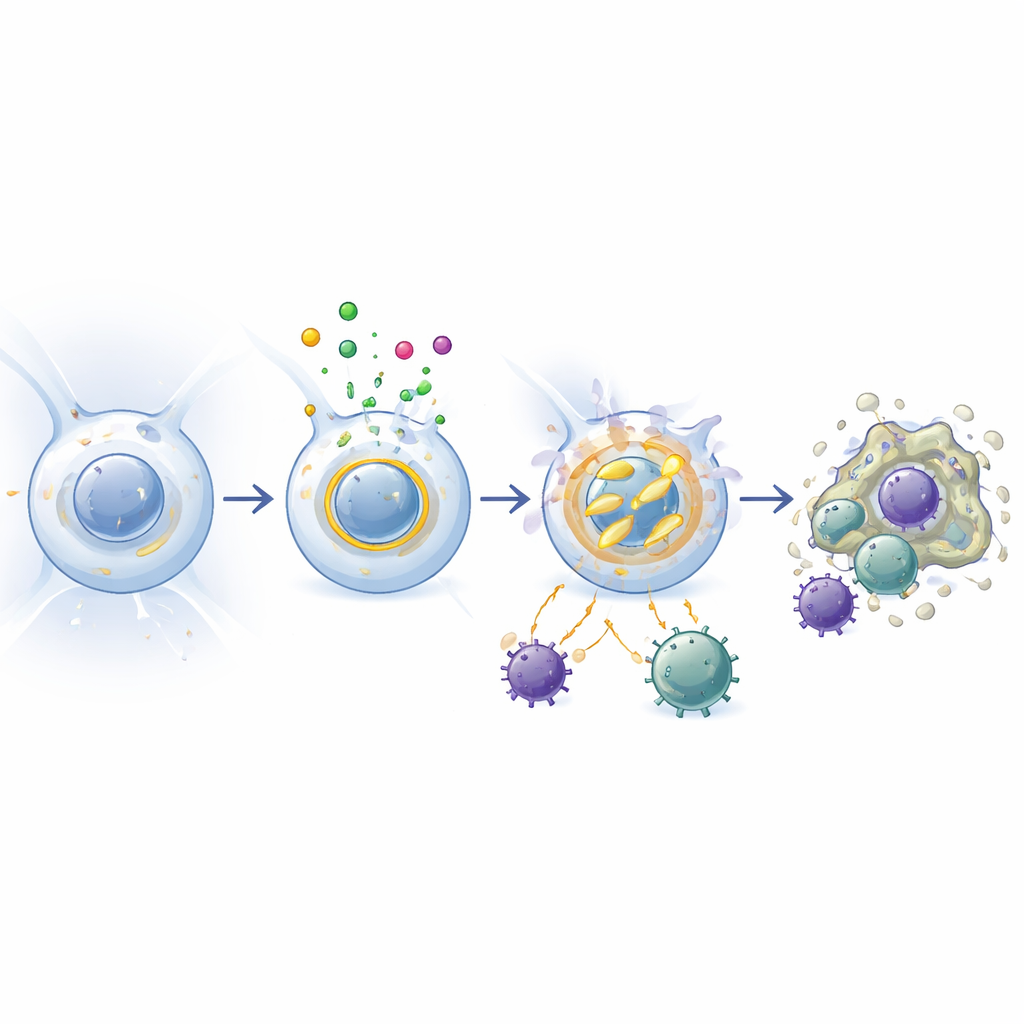
Jak przyjazne mikroby ustawiają pokrętło
Płuca nie są hermetyczną komorą; stale napotykają nieszkodliwe i korzystne mikroorganizmy z powietrza i z jelit. Badacze porównali myszy normalne z bezmikrobiowymi zwierzętami hodowanymi bez jakichkolwiek mikroorganizmów. U myszy bezmikrobiowych makrofagi pęcherzykowe wytwarzały znacznie mniej EI24, a usunięcie EI24 miało niewielki wpływ na ich liczbę i zachowanie. Gdy te bezmikrobiowe myszy później zostały wystawione na normalną mikrobiotę, ich makrofagi płucne zwiększyły produkcję EI24. Eksperymenty wykorzystujące ścieżki czujników mikrobiologicznych wykazały, że sygnały wykrywane przez receptory Toll-podobne 2 i 4 — molekularne „dzwonki” dla składników bakteryjnych — odpowiadały za to zwiększenie. W praktyce mikrobiota popycha makrofagi pęcherzykowe w stronę bardziej stabilnego, mniej reaktywnego stanu poprzez zwiększenie EI24, pomagając utrzymać spokój w środowisku, które inaczej generowałoby ciągłe alarmy immunologiczne.
Przyciszanie EI24, aby zwiększyć skuteczność terapii
Mimo posiadania mniejszej liczby makrofagów, myszy pozbawione EI24 w tych komórkach były lepiej chronione przed ciężką infekcją grypową i eksperymentalnymi przerzutami do płuc z czerniaka. Szybciej usuwały wirusa, wytwarzały więcej antywirusowych interferonów w pęcherzykach powietrznych, a ich makrofagi chętniej pochłaniały komórki nowotworowe. Co ważne, zwierzęta te nie rozwijały przewlekłego uszkodzenia płuc ani utraty funkcji oddechowej, co sugeruje, że selektywne usunięcie EI24 może wzmocnić obronę bez oczywistych szkód w krótkim i średnim okresie. Zespół wykazał też, że makrofagi pochodzące ze szpiku kostnego, w których celowo wyeliminowano EI24, były bardziej efektywne po przeniesieniu do innych myszy, przewyższając normalne makrofagi w ograniczaniu zarówno zakażeń wirusowych, jak i rozprzestrzeniania się nowotworu w płucach.
Co to oznacza dla przyszłych terapii
Dla czytelnika ogólnego przesłanie jest takie, że nasze rezydujące mikroby pomagają utrzymać komórki odpornościowe płuc przy życiu i w spokoju poprzez włączanie EI24 — ale ten sam mechanizm bezpieczeństwa może osłabiać zdolność tych komórek do zwalczania infekcji i raka. Poprzez ostrożne przyciszanie EI24 naukowcy mogą przesunąć makrofagi w stronę bardziej energetycznego, agresywnego stanu, który lepiej eliminuje wirusy i komórki nowotworowe, przy jednoczesnym zachowaniu ogólnego zdrowia płuc w modelach doświadczalnych. Ta praca sugeruje, że ukierunkowanie EI24 lub obwodów metabolicznych, które ono kontroluje, mogłoby pewnego dnia uczynić terapie oparte na makrofagach potężniejszymi sprzymierzeńcami w walce z zakażeniami układu oddechowego i przerzutowym rakiem.
Cytowanie: Huang, Y., Su, M., Zhang, Y. et al. Microbiota-induced EI24 improves homeostasis but impedes function of alveolar macrophages via metabolic regulation. Nat Commun 17, 2227 (2026). https://doi.org/10.1038/s41467-026-69000-3
Słowa kluczowe: makrofagi pęcherzykowe, odporność płuc, mikrobiota, metabolizm makrofagów, obrona przed rakiem i wirusami