Clear Sky Science · pl
Modyfikacja kowalencyjna reszty glutaminianu inspirowana technologią HaloTag
Przekształcanie „kotwic” białkowych w cele leków
Wiele nowoczesnych leków przeciwnowotworowych działa przez przyłączanie się do białek wewnątrz komórek. Jednak niektóre z kluczowych białek nie mają łatwych „uchwytów”, za które leki mogłyby je chwycić. W tym badaniu przedstawiono sprytny trik chemiczny, zainspirowany popularnym narzędziem laboratoryjnym HaloTag, który pozwala przyczepić się do zwykle trudno dostępnego miejsca na białku, regulującego sygnały wzrostowe istotne dla nowotworów. Praca ta może otworzyć nowe drogi do leków, które trwale wyłączają ścieżki napędzające rozwój guza.
Dlaczego większość leków kowalencyjnych celuje w to samo miejsce
W ostatnich latach tzw. ukierunkowane leki kowalencyjne stały się ekscytującą klasą leków. Niosą one łagodnie reaktywną grupę chemiczną, która tworzy trwałe wiązanie z konkretnym aminokwasem w białku, unieruchamiając lek. Prawie wszystkie te leki atakują cysteinę — stosunkowo rzadki, ale wysoce reaktywny aminokwas. Dla porównania dwa inne aminokwasy, asparaginian i glutaminian, występują znacznie częściej i często są kluczowe dla kształtu i funkcji białka, jednak ich kwasowe grupy karboksylanowe są dużo mniej reaktywne w wodnym środowisku komórki. Utrudnia to ich selektywną modyfikację i przed tymi badaniami istniało tylko kilka udanych przykładów inhibitorów kowalencyjnych celujących w glutaminian lub asparaginian.
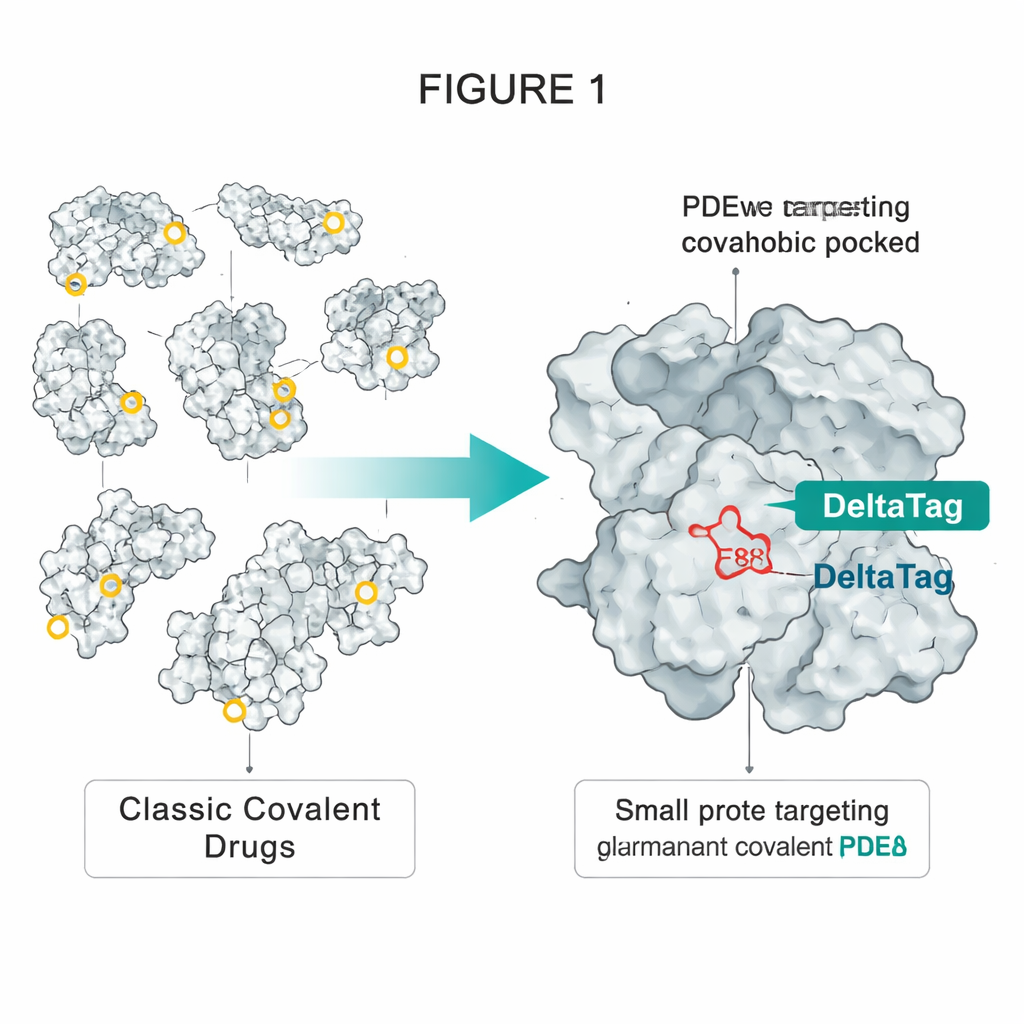
Zaprzęgnięcie triku z technologii HaloTag
Autorzy zaczerpnęli inspirację z HaloTag, szeroko stosowanego inżynieryjnego białka, które można trwale znakować barwnikami fluorescencyjnymi. W HaloTag specjalnie umieszczony asparaginian głęboko w hydrofobowym kieszonce reaguje z prostym chloroalkanem na barwniku, tworząc stabilne wiązanie estrowe. Zespół zauważył, że inne białko, PDEδ, ma podobną hydrofobową kieszonkę zawierającą pojedynczy dostępny glutaminian, oznaczony E88. PDEδ transportuje lipidowo modyfikowane białka sygnałowe, takie jak mały GTPaza Rheb, przez komórkę, pomagając im docierać do błon, gdzie aktywowane są kompleksy promujące wzrost, takie jak mTORC1. Wcześniejsze inhibitory niespecyficzne kowalencyjnie PDEδ mogły blokować ten transport, ale ich efekt był ograniczony, ponieważ inne białko, Arl2, potrafiło z czasem wypchnąć je z kieszonki.
Zaprojektowanie DeltaTag do związania glutaminianu
Aby przezwyciężyć problem „wyciśnięcia”, badacze zaczęli od znanego blokeru PDEδ o dużym powinowactwie i przeprojektowali jeden z jego łańcuchów bocznych tak, by niósł haloalkanowy „materiał wybuchowy” podobny do tych używanych w ligandach HaloTag. Po kilku rundach modyfikacji strukturalnych, wspieranych krystalograficznymi strukturami białka, uzyskali związek nazwany DeltaTag. Jego kluczową cechą jest grupa fenetylo-bromkowa ustawiona tak, że gdy cząsteczka zagnieździ się w lipidowej kieszeni PDEδ, brom jest precyzyjnie wyrównany, by zareagować z E88. Pomiary biofizyczne i wysokorozdzielcze struktury rentgenowskie potwierdziły, że DeltaTag tworzy kowalencyjne wiązanie estrowe specyficznie z tym glutaminianem, a inne potencjalnie bardziej reaktywne aminokwasy w PDEδ pozostają nienaruszone. Związek jest na tyle reaktywny, by efektywnie znakować białko, a jednocześnie wystarczająco stabilny w wodzie i w obecności głównego siarkowego antyoksydantu komórkowego, glutationu, by unikać szeroko zakrojonych, nieselektywnych uszkodzeń.
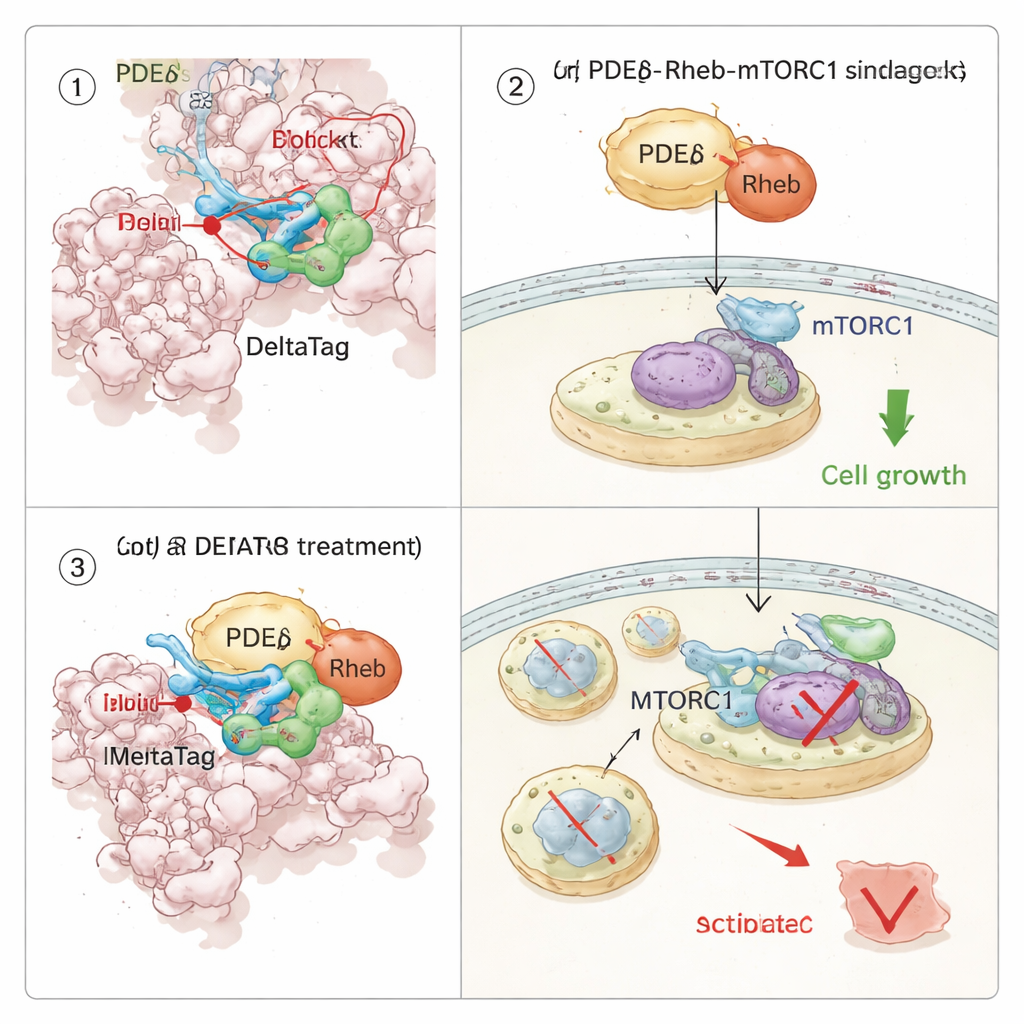
Przełączenie ścieżki wzrostu wewnątrz komórek nowotworowych
Ponieważ PDEδ opiekuje się Rheb, a Rheb aktywuje ścieżkę wzrostu mTORC1, zespół zbadał, jak kowalencyjne zahamowanie PDEδ wpłynie na sygnalizację komórkową. Używając profilowania stabilności termicznej obejmującego tysiące białek, pokazali, że DeltaTag wiąże się selektywnie z PDEδ w ekstraktach komórkowych i wpływa na białka powiązane z osią Rheb–mTOR. W eksperymentach obrazowania komórek na żywo DeltaTag spowodował przemieszczanie się Rheba z rozproszonego wzoru wewnątrz komórki do bardziej skupionych wewnętrznych błon, co jest zgodne z zaburzeniem jego normalnego transportu. Globalne fosfoproteomowe analizy i ukierunkowane Western bloty wykazały, że aktywność mTORC1, śledzona przez fosforylację białka rybosomalnego S6, spada z czasem, podczas gdy sygnały kompensacyjne w powiązanych ścieżkach rosną. Co ważne, w kilku ludzkich liniach komórek nowotworowych napędzanych mutantem KRAS i zależnych od silnej sygnalizacji mTOR, DeltaTag spowolnił proliferację komórek skuteczniej niż blisko spokrewnione inhibitory odwracalne, a jego efekt był słabszy w komórkach pozbawionych PDEδ, co sugeruje, że jego główne działanie jest na celowane białko.
Otwarcie drzwi do nowych typów celów leków
Praca ta pokazuje, że możliwe jest skonstruowanie małych cząsteczek tworzących trwałe, wysoce specyficzne wiązanie z pojedynczym glutaminianem schowanym w hydrofobowej kieszeni białka, używając stosunkowo prostej chemii haloalkanowej zapożyczonej z HaloTag. W układzie modelowym PDEδ takie kowalencyjne połączenie daje trwalsze zablokowanie ścieżki wzrostu istotnej dla nowotworu niż wcześniejsze leki odwracalne. Szerzej, ta sama logika projektowa może zostać zastosowana do innych białek mających hydrofobowe wnęki, ale pozbawionych zwykłych „reaktywnych” aminokwasów, o ile występuje w nich strategicznie umieszczony glutaminian lub asparaginian. Przy dalszej optymalizacji inhibitory kowalencyjne celujące w glutaminian, takie jak DeltaTag, mogą stać się użytecznymi narzędziami w chemicznej biologii, a ostatecznie także punktami wyjścia do nowych terapii przeciw białkom dotąd trudnym do zaatakowania.
Cytowanie: Zhang, R., Liu, J., Gasper, R. et al. Covalent modification of a glutamic acid inspired by HaloTag technology. Nat Commun 17, 1257 (2026). https://doi.org/10.1038/s41467-026-68999-9
Słowa kluczowe: inhibitory kowalencyjne, celowanie w glutaminian, PDEδ, sygnalizacja mTOR, projektowanie leków przeciwnowotworowych