Clear Sky Science · pl
Platforma nanodysków z glikoproteinami wirusów do analiz szczepionek
Przekształcanie białek wirusów w mierzalne cele
Nowoczesne szczepionki coraz częściej opierają się na precyzyjnie zaprojektowanych wersjach białek pokrywających powierzchnię wirusów. Te białka są głównymi celami ochronnych przeciwciał, lecz w swojej naturalnej, związanej z błoną formie bywają niezwykle trudne do zbadania. Artykuł opisuje nową platformę laboratoryjną, która umieszcza pełnej długości białka powierzchniowe wirusa w małych, płaskich cząstkach lipidowych zwanych nanodyskami. Takie rozwiązanie pozwala naukowcom mierzyć, jak dobrze kandydaci na szczepionki naśladują prawdziwe wirusy, jak przeciwciała się do nich przyczepiają i jak przeprojektować szczepionki, by dawały lepszą ochronę.
Dlaczego odtworzenie powierzchni wirusa ma znaczenie
Wiele z najważniejszych białek wirusowych jest zakotwiczonych w tłuszczowej błonie, tak jak na prawdziwym wirusie. Tradycyjne podejścia laboratoryjne odcinają część błonową, aby ułatwić wytwarzanie i oczyszczanie tych białek w roztworze. Jednak takie uproszczenie usuwa regiony bliskie błonie, które zawierają szczególnie wartościowe cele dla przeciwciał, w tym fragment HIV znany jako membrana-proxymalny obszar zewnętrzny (MPER). Regiony te mogą wyglądać i zachowywać się inaczej, gdy nie są osadzone w realistycznym środowisku lipidowym, co oznacza, że rozpuszczalne fragmenty białek mogą dawać niepełny lub mylący obraz tego, jak szczepionka sprawdzi się w organizmie.
Budowa uniwersalnej platformy nanodysków
Naukowcy opracowali uproszczony, pięciodniowy schemat pracy, pozwalający pozyskiwać pełnej długości białka powierzchniowe wirusa z komórek ludzkich, zachować ich naturalne segmenty przechodzące przez błonę i ponownie wprowadzić je do kontrolowanego dysku lipidowego. Najpierw ekspresowali zaprojektowane glikoproteiny HIV i Eboli na powierzchni komórek, potem delikatnie ekstrahowali je detergentem i wychwytywali na matrycy oczyszczającej. Gdy białka były wciąż związane, dodawali zdefiniowane lipidy i białko-szablon w kształcie pasa, które samoorganizuje się w małą, dyskopodobną błonę. W miarę usuwania detergentu białka wirusowe osiadały w tych nanodyskach. Otrzymane preparaty były wysoko czyste, stabilne przez miesiące w lodówce i nosiły osłonę glikanową (cukrową) bardzo zbliżoną do tej występującej na natywnych kolcach wirusa. 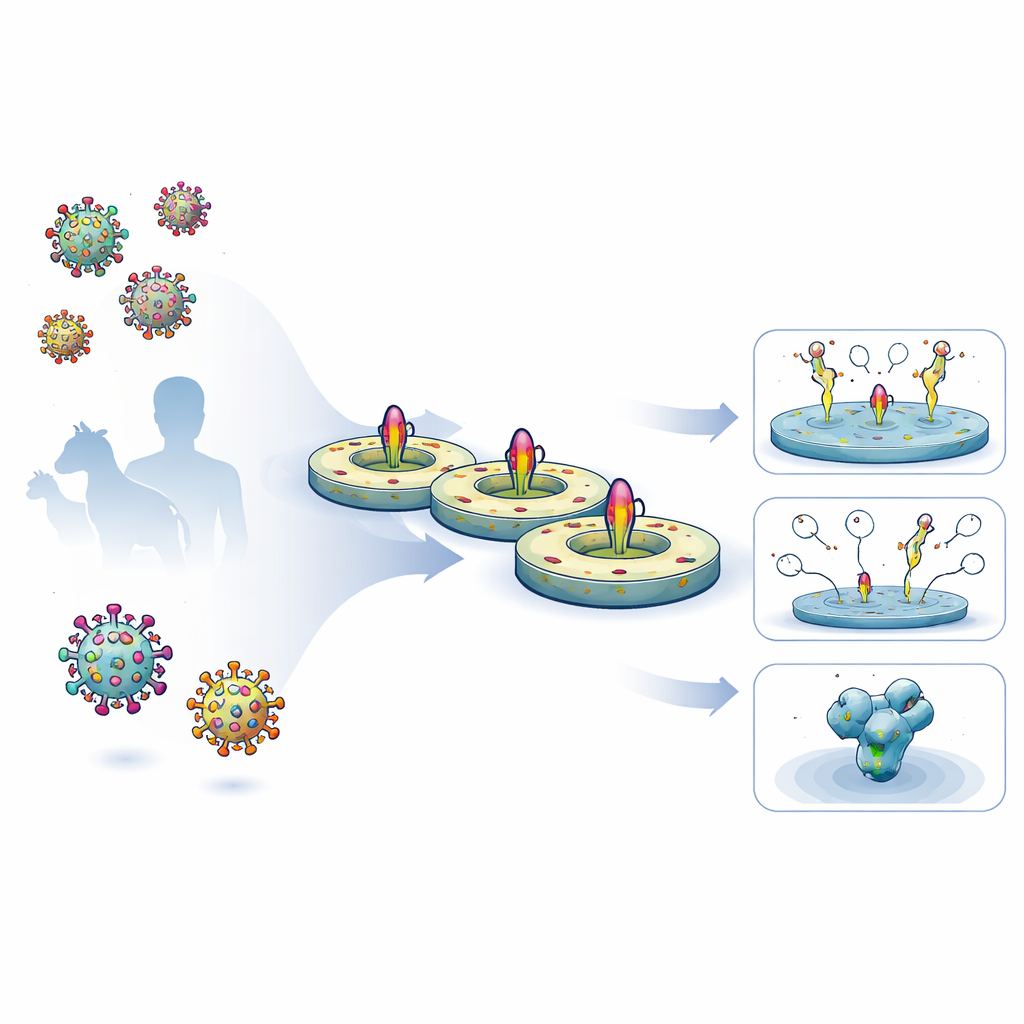
Pomiary wiązania przeciwciał i odpowiedzi immunologicznych
Z nanodyskami zawierającymi białka zespół testował, jak dobrze różne przeciwciała potrafią wiązać się w kilku konfiguracjach powierzchniowej spektroskopii plazmonów (SPR), techniki śledzącej wiązanie w czasie rzeczywistym. Używając nanodysków HIV zaprojektowanych tak, by eksponować region MPER, wykazali, że silne szeroko neutralizujące przeciwciało o nazwie 10E8 wiązało się około 70 razy silniej z nowym konstruktem niż z wcześniejszym projektem, głównie dlatego, że uwalniało się znacznie wolniej. Kontrolne mutacje naruszające region MPER całkowicie eliminowały wiązanie 10E8, potwierdzając, że platforma czułe raportuje, jak zmiany konstrukcyjne wpływają na kluczowe epitopy. Te same nanodyski działały jako sondy w cytometrii przepływowej, gdzie pomogły wyłowić komórki B od immunizowanych myszy i małp, które rozpoznawały pełną, transbłonową formę białka HIV, włączając części nieobecne w standardowych rozpuszczalnych sondach. 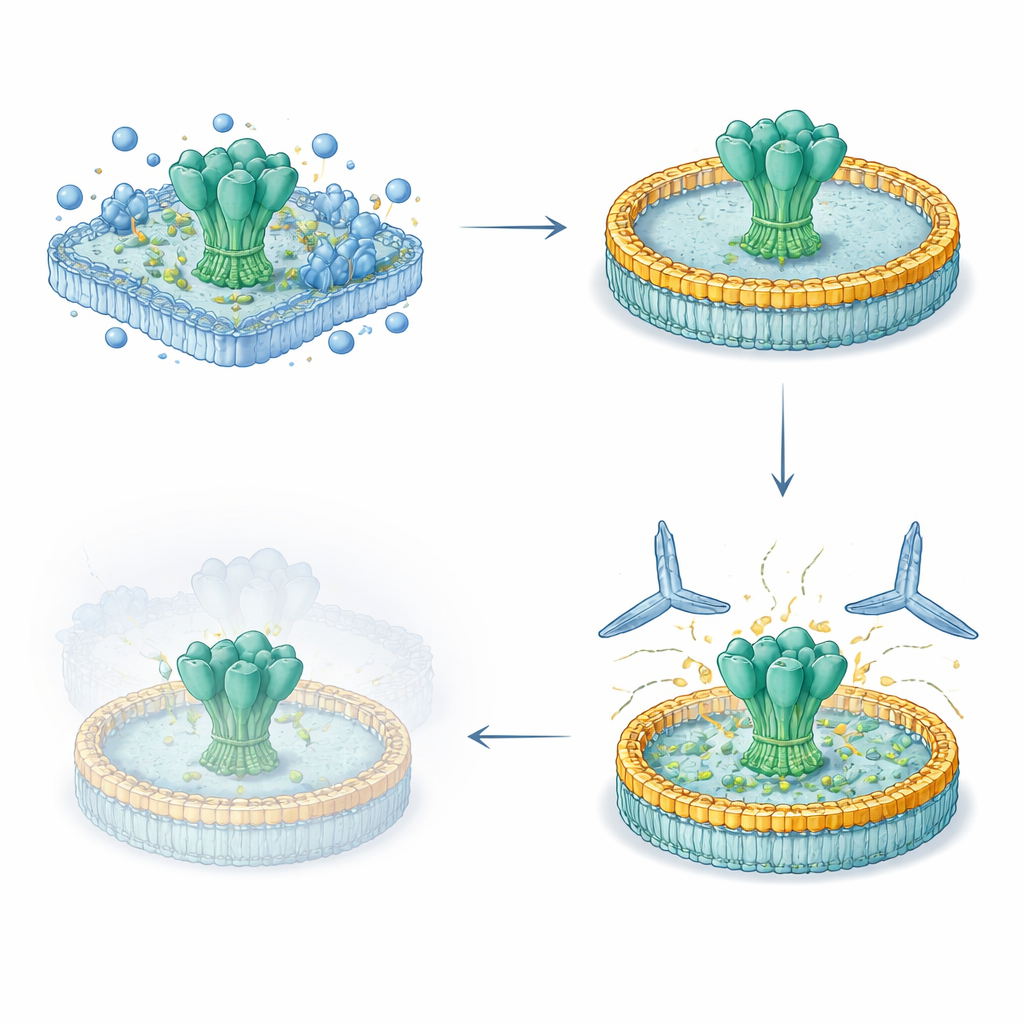
Obserwacja pełnego celu w atomowych szczegółach
Aby dokładnie zrozumieć, jak przeciwciała rozpoznają MPER w jego rodzinnym otoczeniu, autorzy użyli krioelektronowej mikroskopii do obrazowania zaprojektowanych nanodysków HIV związanych z trzema różnymi szeroko neutralizującymi przeciwciałami. Uzyskali strukturę o rozdzielczości 3,5 Å jednego przeciwciała, 10E8, wiążącego fragment MPER, podczas gdy reszta kolca HIV pozostawała zakotwiczona w dysku lipidowym. Odkryto ciągłą sieć kontaktów między 10E8 a zarówno MPER, jak i pobliskimi częściami zewnętrznego białka, w tym głęboką kieszeń na styku dwóch podjednostek. Porównując tę strukturę z wcześniejszymi obrazami 10E8 związanym jedynie z krótkim peptydem, zespół pokazał, że środowisko błonowe i pełnej długości kolca umożliwiają dodatkowe kontakty i dynamiczne ruchy niewidoczne w prostszych modelach, oraz że konkretne aminokwasy w wirusie silnie wpływają na to, jak łatwo 10E8 może go neutralizować.
Szerokie zastosowania dla inteligentniejszych szczepionek
W praktyce ta platforma nanodysków daje projektantom szczepionek sposób oceniania kandydatów transbłonowych za pomocą tych samych potężnych narzędzi analitycznych, które dotąd zarezerwowane były dla rozpuszczalnych fragmentów białek. Działa w różnych wirusach, wspiera szczegółowe pomiary wiązania, umożliwia precyzyjne sortowanie i sekwencjonowanie komórek B wywołanych szczepionką oraz dostarcza struktur o wysokiej rozdzielczości, które odwzorowują realistyczne epitopy bliskie błonie. Dla czytelnika ogólnego wniosek jest taki, że naukowcy dysponują teraz bardziej realistycznym polem testowym dla białek powierzchniowych wirusów — narzędziem, które pokaże, które projekty szczepionek rzeczywiście wyglądają i zachowują się jak prawdziwy wirus oraz jak je poprawić, by wywołać silniejsze i szersze odpowiedzi przeciwciał. To powinno przyspieszyć rozwój szczepionek następnej generacji nie tylko przeciw HIV, lecz także przeciw wielu innym wirusom osłonkowym.
Cytowanie: Rantalainen, K., Liguori, A., Ozorowski, G. et al. Virus glycoprotein nanodisc platform for vaccine analytics. Nat Commun 17, 2561 (2026). https://doi.org/10.1038/s41467-026-68985-1
Słowa kluczowe: nanodyski, szczepionki przeciw HIV, glikoproteiny wirusowe, szeroko neutralizujące przeciwciała, cryo-EM