Clear Sky Science · pl
Radikalne odciskowanie w całej krwi ssaków
Obserwowanie białek w pracy w rzeczywistej krwi
Białka we krwi nieustannie zmieniają kształt, wykonując istotne zadania, takie jak zwalczanie infekcji, transport żelaza i reagowanie na choroby. Do tej pory większość narzędzi służących do badania tych drobnych zmian konformacyjnych działała jedynie w uproszczonych próbkach laboratoryjnych lub w izolowanych komórkach. W tym badaniu po raz pierwszy pokazano, że naukowcy potrafią odczytywać kształty białek bezpośrednio w niezmienionej krwi ssaków, otwierając drogę do obserwowania procesów chorobowych tak, jak zachodzą one w organizmie.
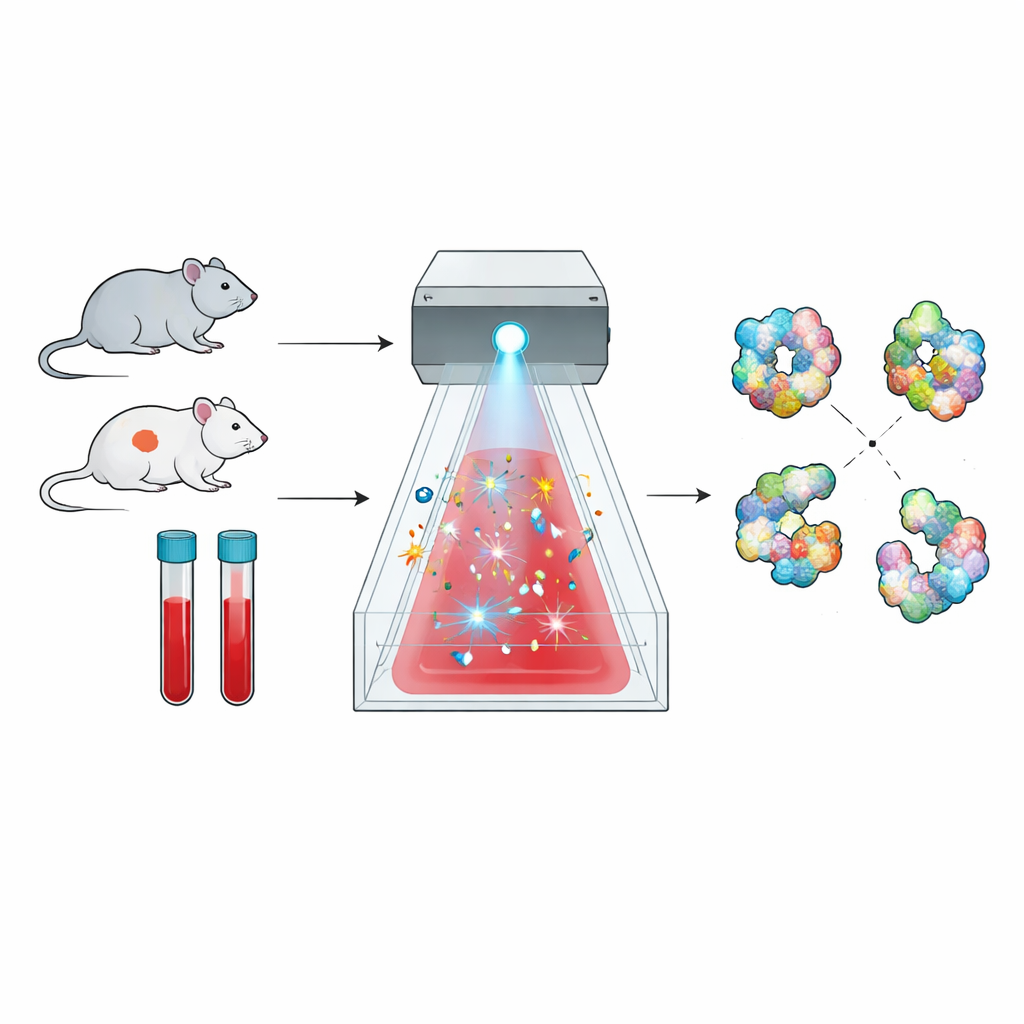
Nowy sposób mapowania kształtów białek
Białka nie są sztywnymi koralikami; składają się w złożone formy trójwymiarowe, a te formy determinują ich funkcje. Metoda opisana tutaj, zwana radykalnym odciskowaniem białek, wykorzystuje to założenie. Krótkie impulsy wysoce reaktywnych cząsteczek działają jak chemiczna „lampa błyskowa”, uderzając tylko w odsłonięte fragmenty białka. Później spektrometria mas służy do zliczenia miejsc tych modyfikacji, tworząc rodzaj mapy powierzchni — odcisku — danego białka. Zmiany w tym odcisku między stanem zdrowia a chorobą ujawniają subtelne przesunięcia w fałdowaniu białka lub w jego interakcjach z partnerami.
Wdrożenie techniki do pracy w całej krwi
Zastosowanie tego podejścia bezpośrednio do krwi było od dawna wyzwaniem. Krew silnie absorbuje światło ultrafioletowe i zawiera dużo enzymów, takich jak katalaza, które szybko niszczą zwykłe związki generujące rodniki, zanim zdołają one oznakować białka. Badacze rozwiązali ten problem, przechodząc na nadsiarczan sodu, który po rozszczepieniu jasnym, szerokopasmowym błyskiem światła daje silne rodniki siarczanowe. Korzystając z komercyjnego systemu FOX, wykazali, że nadsiarczan można aktywować niezawodnie, a wbudowany odczyt dozymetrii pozwala śledzić liczbę wytworzonych rodników, co umożliwia precyzyjną kontrolę „ekspozycji” każdej próbki.
Ochrona komórek przy zachowaniu szczegółów
Ponieważ metoda ma badać białka w stanie zbliżonym do naturalnego, kluczowe było, by same komórki krwi nie ulegały zniszczeniu. Testy na krwi mysiej pokazały, że dodanie skoncentrowanego nadsiarczanu powodowało jedynie niewielkie, odwracalne zmiany kształtu erytrocytów i mniej niż dwuprocentową lizie komórek, co jest podobne do efektu prostych roztworów soli. Zespół opracował też ulepszoną mieszaninę „ugasiacza”, która szybko wychwytuje pozostałe reaktywne gatunki, zapobiegając przypadkowemu uszkodzeniu spowodowanemu przez wolniejsze reakcje uboczne po błysku. Te udoskonalenia pozwoliły im znakować białka w nieuszkodzonej krwi mysiej przy zachowaniu struktury komórek i bardzo niskim poziomie szumu tła.
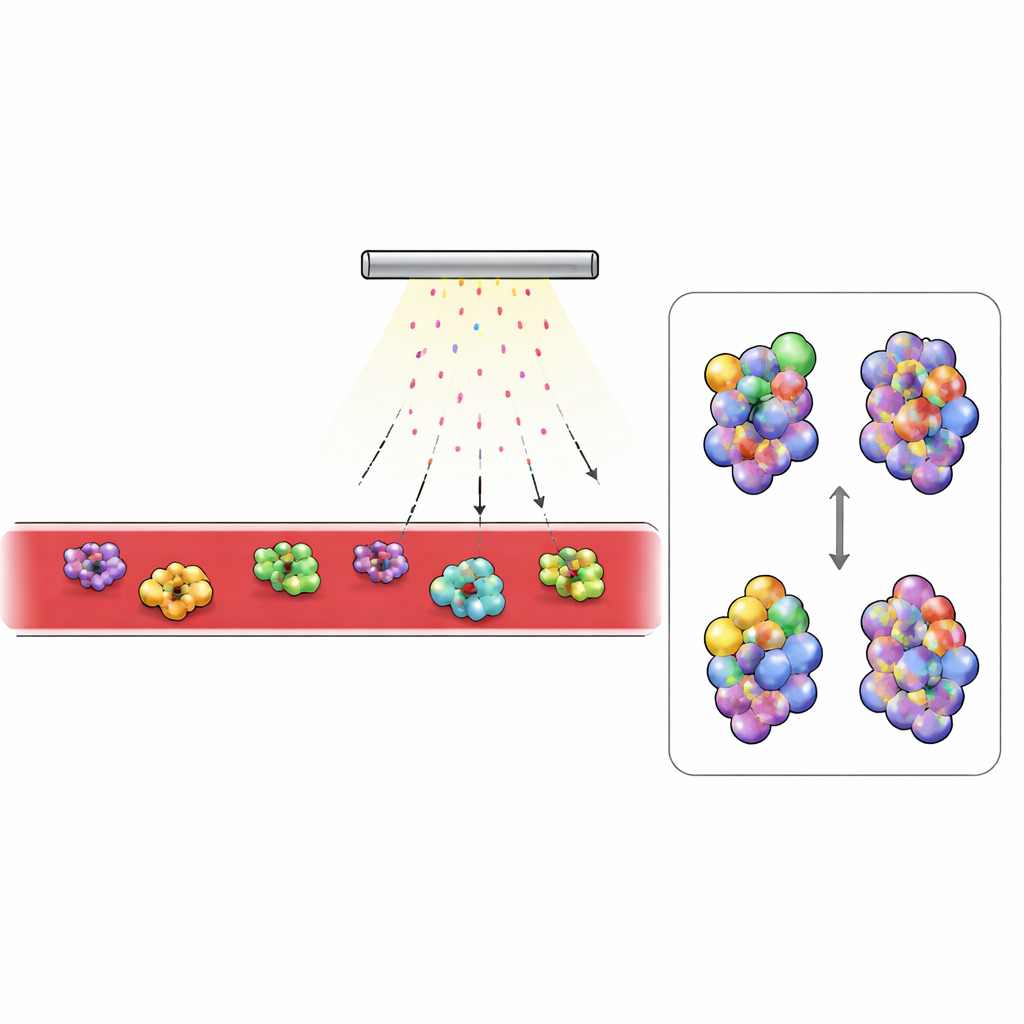
Co się zmienia w krwi cukrzycowej
Mając tę platformę, badacze porównali krew zdrowych myszy z krwią z powszechnie stosowanego modelu cukrzycy typu 2. Skupili się na najobficiej wykrywanych białkach, zwłaszcza tych krążących poza komórkami. Białka zewnątrzkomórkowe otrzymały znacznie więcej znakowań niż te wewnątrzkomórkowe, co odzwierciedlało ograniczone przenikanie nadsiarczanu do wnętrza komórek. Wyróżniły się dwa białka krwi: dopełniacz C3, kluczowy składnik układu odpornościowego, oraz transferryna, transportująca żelazo. U myszy cukrzycowych regiony C3, które ukrywają się, gdy białko przechodzi w aktywną formę, były mniej znakowane, podczas gdy normalnie ukryte obszary były bardziej odsłonięte. Wzorzec ten odpowiadał znanej zmianie strukturalnej przy konwersji C3 do aktywnego fragmentu C3b, a badania krwi potwierdziły, że u zwierząt chorych na cukrzycę występowała znacznie większa ilość aktywowanego C3. W transferrynie obszary przy miejscu wiązania żelaza były bardziej chronione w krwi cukrzycowej, co zgadza się z większym ładunkiem żelaza przez to białko. Niezależne pomiary wykazały wyższe stężenie żelaza w surowicy i większy odsetek transferryny nasyconej żelazem u myszy cukrzycowych.
Dlaczego to ma znaczenie dla zdrowia i medycyny
Dla osoby niebędącej specjalistą najważniejszy przekaz brzmi: autorzy stworzyli sposób, by „wyczuwać” kształty wielu białek jednocześnie bezpośrednio w prawdziwej krwi, a następnie używać tych wzorców kształtów do wnioskowania, jak choroba zmienia chemię organizmu. W tym modelu myszy z cukrzycą typu 2 metoda ujawnia nadmierną aktywację dopełniacza i większe obciążenie transferryny żelazem — zmiany, które klasyczne testy mogą przegapić lub dostrzec tylko pośrednio. Ponieważ podejście działa na małych próbkach krwi i wykorzystuje standardowe źródło światła, może w przyszłości pomóc wykrywać wczesne strukturalne sygnały ostrzegawcze chorób, śledzić zachowanie leków biologicznych we krwi oraz ukierunkować projektowanie skuteczniejszych terapii.
Cytowanie: Zhao, M., Tobin, L., Misra, S.K. et al. Radical footprinting in mammalian whole blood. Nat Commun 17, 2470 (2026). https://doi.org/10.1038/s41467-026-68982-4
Słowa kluczowe: proteomika strukturalna, białka krwi, cukrzyca typu 2, układ dopełniacza, metabolizm żelaza