Clear Sky Science · pl
Warianty końca C białek wpływają na proteostazę
Jak końcówka białek kształtuje zdrowie
Każde białko w naszych komórkach kończy się malutkim „ogonkiem” złożonym z kilku aminokwasów. Te ogonki mogą wyglądać na dodatek, ale badanie pokazuje, że to one cicho decydują, które białka utrzymują się dłużej, a które są szybko usuwane. Ponieważ poziomy białek leżą u podstaw raka, chorób genetycznych i reakcji komórek na stres, zrozumienie tych ogonków otwiera nowe możliwości oceny ryzyka chorób, a nawet projektowania przyszłych terapii.
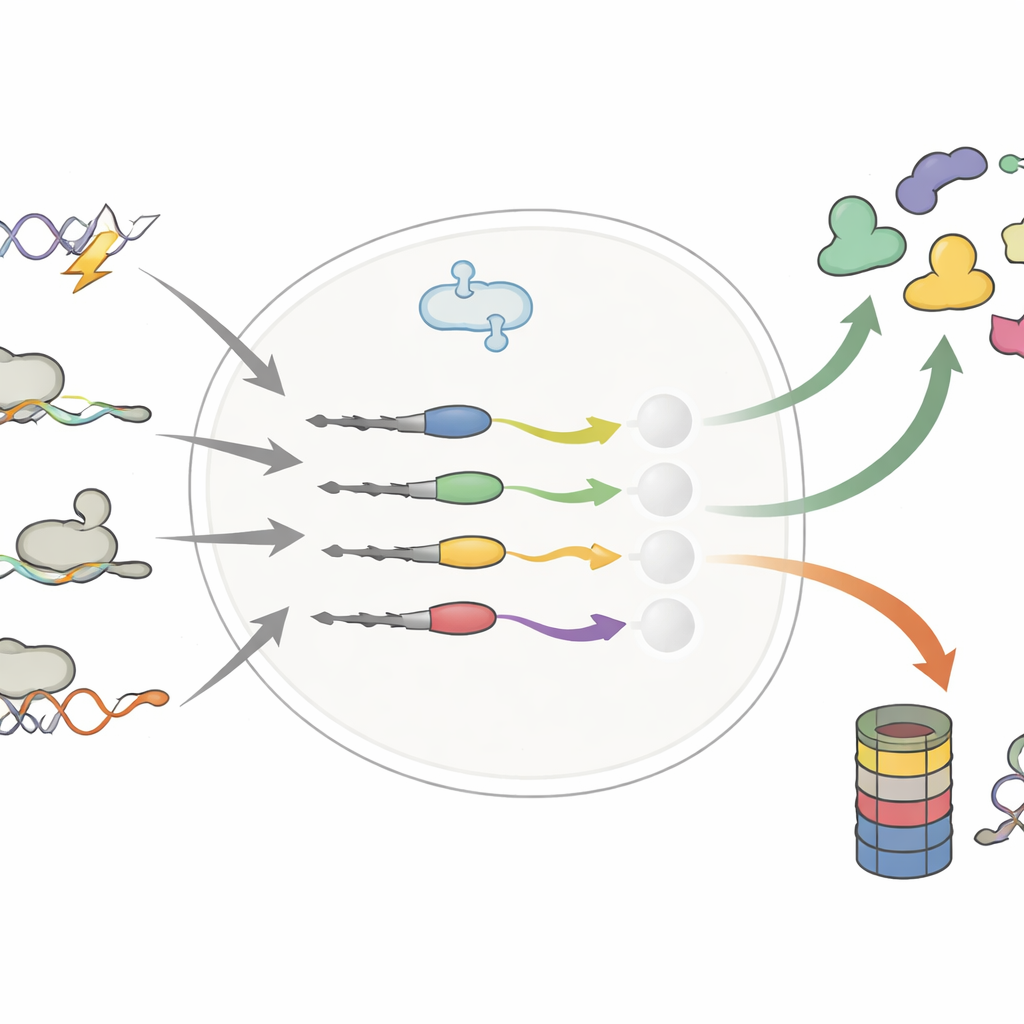
Małe zmiany w ogonku, duże przesunięcia w długości życia
Autorzy skupili się na dalekim końcu białek — końcu C, gdzie nawet kilka dodatkowych lub zamienionych reszt może powstać wskutek mutacji DNA, alternatywnego składania RNA lub przeczytania przez rybosom poza zwykłym sygnałem stop. Wcześniejsze prace sugerowały, że takie „błędne” ogonki głównie działają jako metki do likwidacji, kierując wadliwe białka do komórkowej niszczarki. Poprzez systematyczne porównanie tysięcy normalnych i zmienionych ogonków to badanie obala to proste ujęcie. Zespół pokazuje, że zmienione ogonki mogą skracać lub wydłużać życie białka, czasem stabilizując onkogeny, a innym razem destabilizując supresory nowotworów.
Kiedy błędy genetyczne pomagają lub szkodzą białkom
Jednym z głównych źródeł zmian ogonków są mutacje nonstop, które usuwają normalny sygnał stop, dzięki czemu rybosom kontynuuje translację w obszarze RNA zwykle nieaktywym. Badacze przetestowali ponad 3000 wariantów nonstop związanych z chorobami, używając dwukolorowego raportera mierzącego, jak dany ogonek chroni lub osłabia białko modelowe. Średnio ogonki mutantów nadal czyniły białka mniej stabilnymi niż ich normalne odpowiedniki, ale znaczna część działała odwrotnie: około jedna na dziesięć mutacji nonstop stabilizowała białka, podczas gdy prawie jedna trzecia je destabilizowała. Te zmiany dotyczyły znanych onkogenów i supresorów guza, co sugeruje, że pozornie drobne mutacje mogą przechylić równowagę wzrostu i śmierci komórkowej.
Wrodzona różnorodność przez składanie i przeczytanie
Nie wszystkie różnice w ogonkach są przypadkowe. Nasze geny rutynowo produkują wiele wersji białek przez alternatywne składanie i zaprogramowane przeczytanie kodonu stop. Analiza katalogów genów ludzkich wykazała, że niemal dwie trzecie genów wytwarza białka z więcej niż jednym wzorem ogonka, a wiele z nich różni się tylko w kilku ostatnich resztach. Testy wybranych przykładów pokazały, że te niemal identyczne wersje często mają wyraźnie różne połowiczne czasy życia. Niektóre ogonki powstałe w wyniku przeczytania zwiększały stabilność białek, inne zmniejszały ją. Sugeruje to, że komórki celowo wykorzystują warianty ogonków jako precyzyjny regulator, dostosowując, jak długo konkretne formy białek utrzymują się w różnych tkankach lub warunkach.
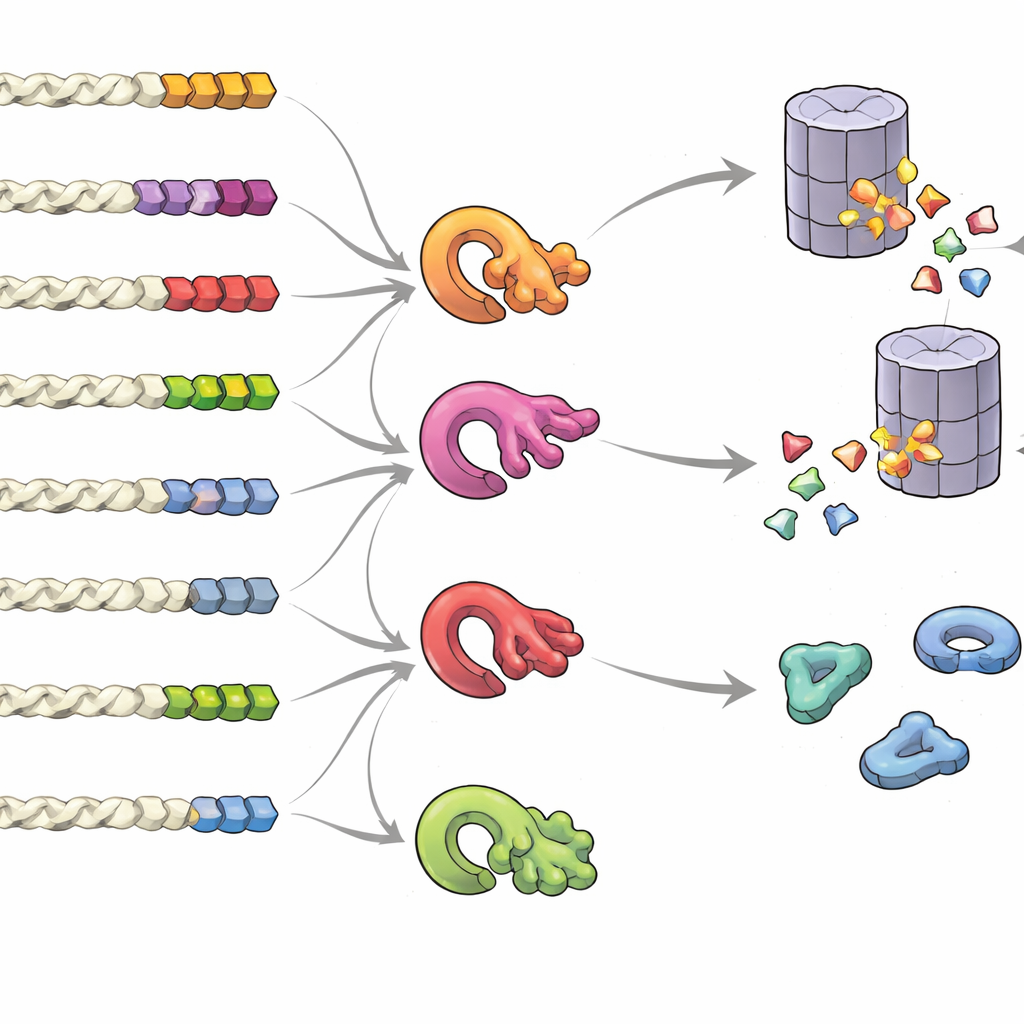
Co sprawia, że ogonek to sygnał „zachowaj mnie” lub „wyrzuć mnie”
Aby zrozumieć, jakie cechy ogonka wpływają na los białka, zespół stworzył biblioteki losowych ogonków i zmierzył ich oddziaływanie masowo. Stwierdzili, że nie chodzi o jeden stały „motyw”, lecz o ogólny skład aminokwasowy, pozycję i skupienie określonych reszt. Ogonki bogate w małe lub hydrofobowe reszty, a także rzadsze cysteinę i tryptofan, skłaniały do degradacji, szczególnie gdy te reszty występowały w skupiskach. W przeciwieństwie do tego ogonki wzbogacone w reszty kwaśne sprzyjały stabilności. Analiza wielu gatunków wykazała, że normalne ogonki białkowe noszą wyraźne ślady presji ewolucyjnej, by unikać ryzykownych wzorców, podczas gdy ogonki powstałe w wyniku błędnego przeczytania lub przesunięcia ramek były skłonne do destabilizujących kompozycji. Grupa odkryła również, że różne enzymy kontroli jakości — różne ligazy ubikwitynowe — wyspecjalizowały się w rozpoznawaniu odmiennych hydrofobowych wzorców ogonków, tworząc złożoną sieć decydującą o tym, które białka zostaną zniszczone.
Dlaczego to ma znaczenie dla medycyny i biotechnologii
Praca przekształca postrzeganie ogonków białkowych z pasywnych zakończeń w aktywnych regulatorów obfitości białek. Dla laika oznacza to, że wiele chorób może wynikać nie tylko z uszkodzonych białek, lecz także z subtelnych zmian w czasie utrzymywania się białek, wywołanych drobnymi różnicami na ich końcach. To także ostrzeżenie, że terapie celowo promujące przeczytanie sygnałów stop, stosowane w leczeniu niektórych chorób genetycznych, mogą niezamierzenie zmieniać żywotność wielu normalnych białek. Jednocześnie wyniki sugerują potężne nowe strategie: poprzez inżynierię sekwencji ogonków lub skłanianie komórek do faworyzowania określonych form składania lub przeczytania, naukowcy mogą kiedyś regulować poziomy białek z wyjątkową precyzją.
Cytowanie: Chu, CY., Hsu, SY., Yeh, CW. et al. Protein C-terminal variations impact proteostasis. Nat Commun 17, 2288 (2026). https://doi.org/10.1038/s41467-026-68979-z
Słowa kluczowe: stabilność białek, ogon C-terminalny, degradacja białek, mutacje genetyczne, proteostaza