Clear Sky Science · pl
VSIG10L jest głównym czynnikiem utrzymania homeostazy przełyku i dziedzicznej predyspozycji do przełyku Barretta
Dlaczego ma to znaczenie dla osób z zgagą
Przewlekła zgaga jest powszechna, ale tylko niewielka część osób rozwija przełyk Barretta, schorzenie mogące prowadzić do raka przełyku. W badaniu postawiono proste, lecz istotne pytanie: dlaczego niektóre rodziny są znacznie bardziej podatne na przełyk Barretta niż inne? Śledząc pojedynczy gen i obserwując, jak kształtuje on wyściółkę przełyku u ludzi i myszy, badacze odkrywają brakujące ogniwo łączące dziedziczne ryzyko, uszkodzenia spowodowane refluksem i zdolność organizmu do utrzymania zdrowia przełyku.
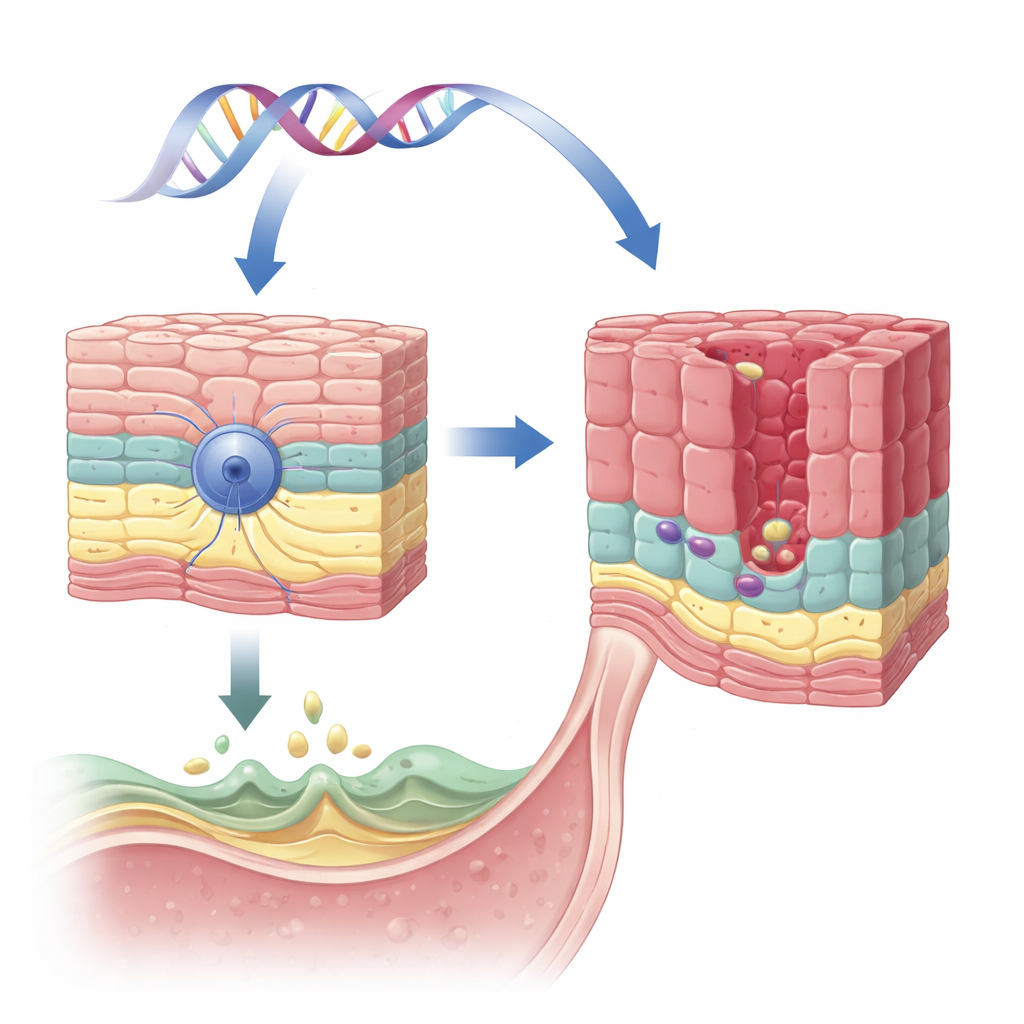
Gen ochronny w nabłonku przełyku
Zespół skupił się na genie nazwanym VSIG10L, wcześniej wskazanym w jednej dużej rodzinie z wieloma przypadkami przełyku Barretta i powiązanych nowotworów. VSIG10L jest aktywny w górnych warstwach płaskich (szkliwiejących) komórek wyściełających przełyk, ale nie w głębszych, podobnych do komórek macierzystych komórkach bazalnych. Stosując czułą metodę wykrywania RNA w tkankach ludzkich, świńskich i mysich oraz w trójwymiarowych hodowlach ludzkich komórek przełyku, badacze wykazali, że VSIG10L jest konsekwentnie włączony tylko w „dojrzewających” komórkach tuż nad warstwą bazalną. Ten wzór sugeruje, że VSIG10L pomaga komórkom płaskim zakończyć ostateczne etapy dojrzewania i uformować stabilną barierę.
Dziedziczne zmiany osłabiające barierę
Przez sekwencjonowanie genu VSIG10L u 684 osób z 302 rodzin dotkniętych przełykiem Barretta i rakiem przełyku badacze odkryli kilka rzadkich, szkodliwych wariantów. Aby sprawdzić działanie tych wariantów, wytworzyli organoidy przełyku pochodzące ze zróżnicowanych komórek macierzystych pacjenta noszącego jedną z takich mutacji. W porównaniu z organoidami od zdrowego dawcy, mutantne organoidy nie zbudowały normalnej, warstwowej struktury płaskiej. Zamiast tego często tworzyły nieprawidłowe, gruczołopodobne kuliste skupiska komórek, które pozostawały w stanie bazalnym, niedojrzałym, oznaczonym białkiem p63. To zaburzenie normalnego układu warstw i dojrzewania odzwierciedla wczesne etapy uważane za poprzedzające przełyk Barretta u pacjentów.
Modele myszy odtwarzające ludzką chorobę
Aby wyjść poza hodowle komórkowe, zespół stworzył myszy niosące albo precyzyjną kopię rodzinnej mutacji VSIG10L znalezionej u ludzi, albo całkowitą utratę tego genu. U zdrowych myszy odpowiadający gen Vsig10l jest ponownie aktywny tylko w komórkach szkliwiejących ponad warstwą bazalną. W mikroskopii elektronowej u myszy z mutacją zaobserwowano wyraźny ubytek desmosomów — drobnych „nitów” łączących sąsiednie komórki — w tych warstwach. Mapy aktywności genów z nabłonka leśnego żołądka myszy, regionu przypominającego dolny przełyk, ujawniły szerokie zaburzenia programów strukturalnych i różnicowania. Po karmieniu myszy dietą zawierającą kwas żółciowy deoksycholowy, naśladując przewlekły refluks, 70–100% zwierząt z mutacją Vsig10l rozwinęło rozległe, przypominające przełyk Barretta zmiany śluzówkowe bogate w mucyny na złączu szkliwiejąco‑walcowatym, podczas gdy myszy typu dzikiego rozwinęły jedynie niewielkie, ograniczone zmiany.
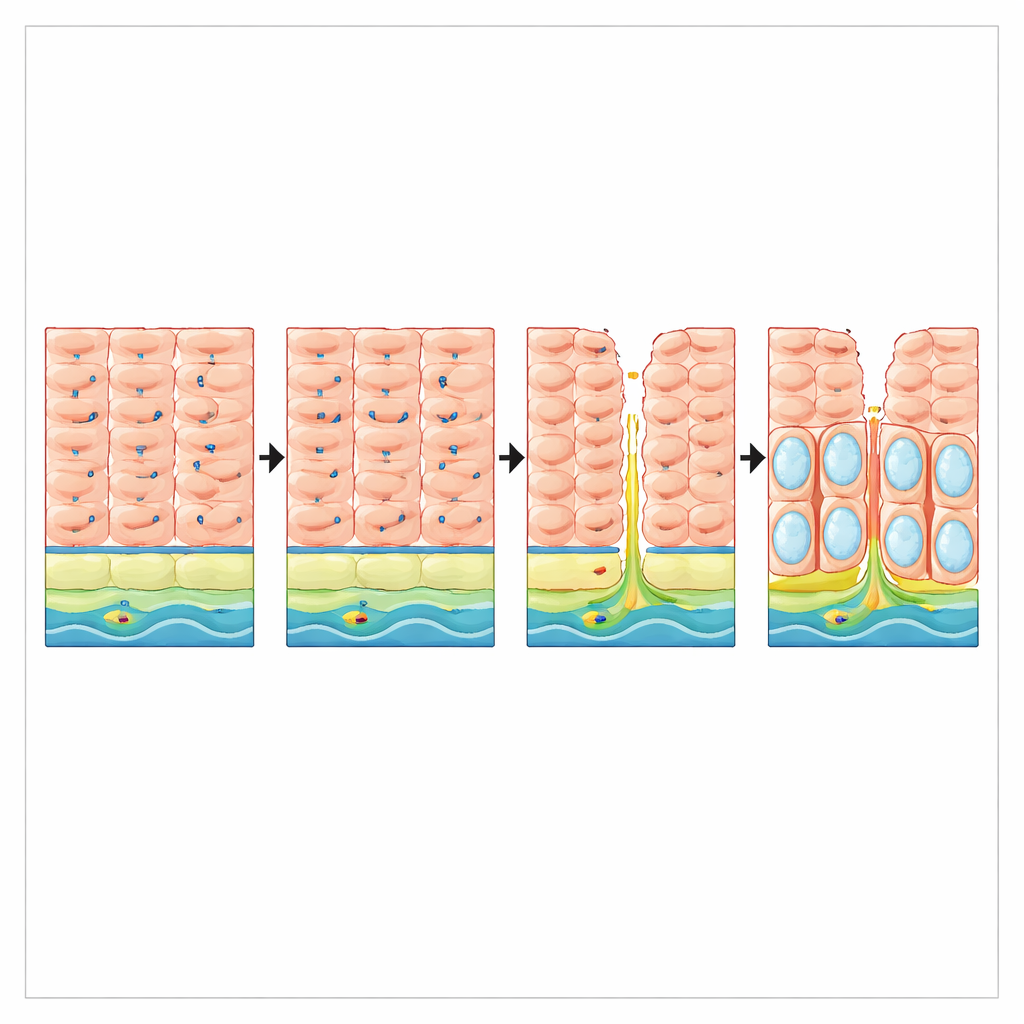
Uraz wywołany refluksem i utrata ochrony u pacjentów
Badacze zapytali następnie, czy sam refluks może zaburzać VSIG10L u ludzi. W wycinkach od pacjentów z długotrwałą chorobą refluksową przełyku, ale pozbawionych przełyku Barretta, poziomy RNA VSIG10L były około trzykrotnie niższe niż u osób bez refluksu, mimo że podstawowy marker komórek płaskich TP63 pozostawał niezmieniony. W przekrojach tkankowych zdrowa wyściółka przełyku wykazywała wyraźny pas komórek pozytywnych dla VSIG10L nad warstwą bazalną. Natomiast w śluzówce uszkodzonej przez refluks zaobserwowano ekspansję komórek o cechach bazalnych, bogatych w p63, oraz niemal całkowitą utratę gradientu różnicowania oznaczonego VSIG10L. Wyniki te sugerują, że przewlekły refluks narusza nie tylko fizyczną integralność wyściółki, lecz także program genowy utrzymujący jej uporządkowaną odnowę.
Składanie elementów w całość
Podsumowując, praca wspiera prosty model: VSIG10L jest kluczowym strażnikiem bariery szkliwiejącej przełyku. Dziedziczne uszkodzenia tego genu lub nabyte jego zahamowanie wskutek przewlekłego refluksu prowadzą do zaburzeń dojrzewania wyściółki, mniejszej liczby łączy międzykomórkowych i bardziej przeciekającej powierzchni. W takim podatnym stanie powtarzające się narażenie na kwas i żółć sprzyja nieprawidłowemu, gruczołopodobnemu gojeniu zamiast przywrócenia pierwotnej wyściółki płaskiej, co tworzy podłoże do rozwoju przełyku Barretta. Dla pacjentów i rodzin badania te wskazują drogę do przyszłych testów genetycznych, które mogą wyłonić osoby o najwyższym ryzyku, oraz do nowych terapii mających na celu zachowanie lub przywrócenie funkcji VSIG10L, z długoterminowym celem zapobiegania przełykowi Barretta i jego progresji do raka.
Cytowanie: Ravillah, D., Singh, S., Katabathula, R.M. et al. VSIG10L is a major determinant of esophageal homeostasis and inherited predisposition to Barrett’s esophagus. Nat Commun 17, 2167 (2026). https://doi.org/10.1038/s41467-026-68975-3
Słowa kluczowe: przełyk Barretta, refluks żołądkowo-przełykowy, predyspozycja genetyczna, homeostaza nabłonka, ryzyko raka przełyku