Clear Sky Science · pl
Wykorzystanie allosteryczności ludzkiej fukozylotransferazy 8 za pomocą inhibitora kowalencyjnego w celu zahamowania podstawowej fukozylacji
Dlaczego zablokowanie małego cukru może mieć znaczenie w nowotworach
Nasze komórki nieustannie dekorują białka krótkimi łańcuchami cukrowymi, które precyzyjnie modyfikują funkcję tych białek. Jedna szczególna modyfikacja cukrowa, nazwana podstawową fukozylacją, pomaga nowotworom rosnąć, przenikać do innych tkanek, uchodzić uwadze układu odpornościowego, a nawet opierać się nowoczesnym terapiom przeciwnowotworowym. W artykule opisano, jak naukowcy odnaleźli ukryty punkt kontrolny w ludzkiej enzymie odpowiedzialnej za dodawanie tego cukru i opracowali nową, nisko toksyczną cząsteczkę, która przyczepia się do tego punktu, wyłączając enzym. Ich praca otwiera nową ścieżkę dla leków, które subtelnie przeprogramowują cukrowe oznaczenia na powierzchni komórek zamiast atakować bezpośrednio DNA czy białka.
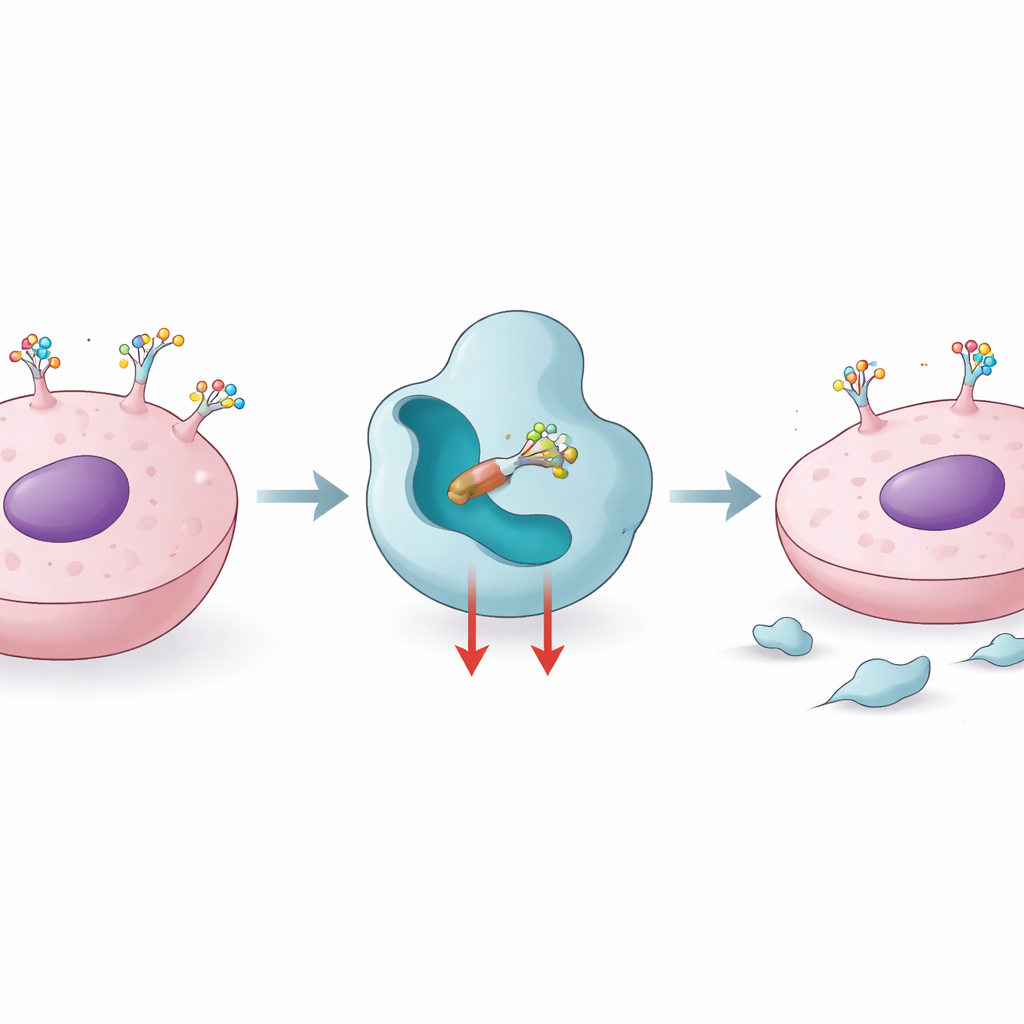
Jak komórki używają znaczników cukrowych do kształtowania choroby
Białka opuszczające komórkową „fabrykę” przechodzą przez molekularną „linię wykończenia”, gdzie przyłączane i edytowane są łańcuchy cukrowe. Podstawowa fukozylacja to jeden z takich etapów wykończeniowych, przeprowadzany przez enzym o nazwie FUT8, który dodaje pojedynczą resztę fukozy w kluczowym miejscu wielu glikanów związanych z białkami. Gdy poziom FUT8 rośnie, ten cukrowy znak staje się bardziej powszechny na cząsteczkach kontrolujących wzrost komórek, migrację i rozpoznawanie przez układ odpornościowy. Badania powiązały wysoką aktywność FUT8 z agresywnym czerniakiem, rakiem piersi potrójnie ujemnym, rakiem płuca oraz z opornością na leki celowane i niektóre terapie przeciwciałami. Zablokowanie FUT8 może pozbawić powierzchni komórkowej pewnych białek hamujących odporność, jak PD‑1, i uczynić guzy bardziej widocznymi dla układu odpornościowego, co czyni FUT8 atrakcyjnym celem dla immunoterapii przeciwnowotworowej i poprawy leków biologicznych.
Potrzeba mądrzejszych, bardziej selektywnych blokerów
Projektowanie leków przeciw FUT8 było trudne, ponieważ wiele powiązanych enzymów korzysta z tego samego podstawowego „paliwa” cukrowego. Wcześniejsze inhibitory często naśladowały to paliwo, prowadząc do szerokiego, nieselektywnego wyłączenia wielu szlaków fukozylacji i niepożądanych skutków ubocznych, w tym zaburzeń krzepnięcia, które zatrzymały badania kliniczne. Autorzy założyli, że lepsza strategia polega na uniknięciu zatłoczonego głównego miejsca aktywnego i zamiast tego poszukaniu unikalnego „odległego” miejsca na FUT8, które mogłoby działać jak przełącznik kontrolny. Korzystając z testu wysokoprzepustowego monitorującego aktywność enzymu, przeszukali ponad sześć tysięcy związków i wytypowali kilka cząsteczek o kształcie łańcuchowym, które spowalniały FUT8 i jednocześnie ograniczały inwazyjność komórek nowotworowych w hodowlach.
Odkrycie ukrytej kieszeni kontrolnej
Za pomocą krystalografii rentgenowskiej zespół rozwiązał trójwymiarową strukturę FUT8 związanej z dwoma z tych inhibitorów. Ku ich zaskoczeniu żaden związek nie siedział w zwykłym miejscu, gdzie wiążą się donor i akceptor cukrowy. Zamiast tego oba ulokowały się w długiej, przypominającej kanał kieszeni między dwoma głównymi płatami enzymu, blisko, lecz odrębnie od centrum aktywnego. Wiązanie w tym miejscu przesunęło pewne pętle i kluczowe aminokwasy z pozycji, szczególnie elementy, które zwykle pomagają obejmować donora cukru. Symulacje komputerowe wykazały, że gdy kieszeń była wypełniona, ogólna dynamika i krajobraz energetyczny FUT8 ulegały przesunięciu, faworyzując konformacje słabo katalizujące reakcję. Innymi słowy, inhibitory działały allosterycznie: naciskały odległy „przycisk”, który powodował rozestawienie pracujących części enzymu.
Przekształcenie trafu w precyzyjne narzędzie kowalencyjne
Uzbrojeni w tę mapę strukturalną, badacze poszukiwali cząsteczek, które nie tylko wypełniłyby kieszeń, ale także utworzyły trwałe wiązanie z pobliskim resztą lizyny (K216), która naturalnie odchyla się w stronę kanału. Odkryli, że reagent o nazwie SSO, niosący reaktywny ester N‑hydroksy‑succinimidu, wiązał się w tym samym rowku i tworzył kowalencyjne połączenie z K216, blokując enzym w stanie nieaktywnym. Bazując na wspólnych cechach SSO i wcześniejszego trafu NH125, połączyli fragmenty obu związków, tworząc nową cząsteczkę nazwaną CAIF. Struktury krystaliczne potwierdziły, że CAIF przesuwa się wzdłuż kanału, dopasowuje się ciasno wśród hydrofobowych reszt i tworzy kowalencyjne wiązanie z K216. To rozwiązanie zwiększyło hamowanie FUT8 wielokrotnie w porównaniu z pierwotnymi związkami, jednocześnie oszczędzając blisko spokrewnione enzymy, co podkreśla unikalny kształt allosterycznej kieszeni FUT8.
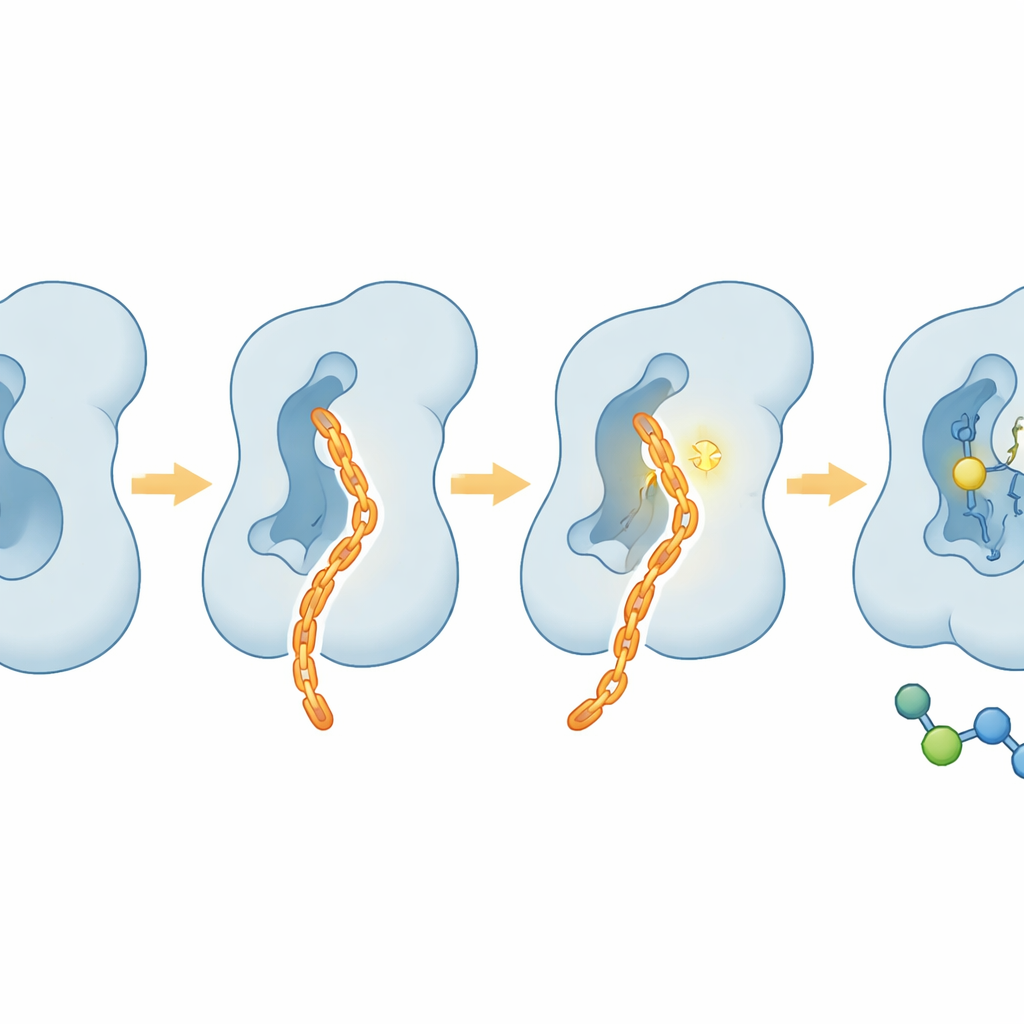
Łagodny dla komórek, surowy dla zachowań guza
Ponad próbówkami, zespół zbadał, jak CAIF zachowuje się w żywych komórkach. W kilku ludzkich liniach komórkowych CAIF wykazywał minimalną toksyczność nawet przy wysokich dawkach, co wskazuje, że nie zatruwa szeroko maszynerii komórkowej. Jednocześnie znacząco zmniejszał podstawową fukozylację na powierzchni komórek, co ujawniono za pomocą barwników wiążących cukry, i robił to z dużo lepszą selektywnością wobec FUT8 niż wcześniejsze pan‑inhibitory. W testach inwazji komórek nowotworowych CAIF przewyższał powszechnie stosowany blokujący związek na bazie cukrów w ograniczaniu zdolności komórek nowotworowych do przemieszczania się przez macierz, co jest znakiem potencjału metastatycznego. Efekty te odpowiadają znanej roli FUT8 w nasilaniu inwazji i ucieczki przed układem odpornościowym, zamiast bezpośredniego napędzania podziałów komórkowych.
Co to oznacza dla przyszłych terapii przeciwnowotworowych
To badanie nie twierdzi, że CAIF sam w sobie jest gotowy na lek. Pokazuje natomiast, że FUT8 zawiera wcześniej nieznaną, podatną na działanie farmakologiczne kieszeń allosteryczną, którą można celować za pomocą starannie ukształtowanych cząsteczek tworzących trwałe wiązanie z pojedynczą lizyną. Wykorzystując to miejsce, badacze mogą selektywnie stłumić enzym modyfikujący cukry, który stoi na skrzyżowaniu progresji nowotworu, ucieczki immunologicznej i oporności na leki, pozostawiając przy tym powiązane enzymy w dużej mierze nienaruszone. Praca ta oferuje plan projektowania następnej generacji inhibitorów, które przekształcają wzory cukrowe istotne dla choroby na białkach i mogą ostatecznie poszerzyć zestaw narzędzi dla immunoterapii przeciwnowotworowej oraz ulepszonych leków przeciwciałowych.
Cytowanie: Jiang, J., He, D., Ke, M. et al. Exploiting human fucosyltransferase 8 allostery with a covalent inhibitor for core fucosylation suppression. Nat Commun 17, 2607 (2026). https://doi.org/10.1038/s41467-026-68971-7
Słowa kluczowe: Inhibicja FUT8, podstawowa fukozylacja, kowalencyjne inhibitory allosteryczne, glikozylacja w nowotworach, projektowanie leków przeciwko glikozylotransferazom