Clear Sky Science · pl
FANCD2 hamuje postęp widełek i zapobiega kruchości w wczesnych originach podczas re-replikacji
Kiedy kopiowanie DNA delikatnie zbacza z kursu
Za każdym razem, gdy komórka dzieli się, musi dokładnie raz skopiować cały swój zbiór DNA. Jeśli fragmenty tego zbioru zostaną skopiowane dwukrotnie albo w pośpiechu i niestarannie, skutkiem mogą być pęknięte chromosomy i mutacje sprzyjające nowotworom. W tym badaniu przyjrzano się, co się dzieje, gdy mechanizmy chroniące przed dodatkowymi rundami kopiowania zawodzą, i wykazano, jak białko naprawcze FANCD2 wkracza, by powstrzymać łagodnie „nieposłuszne” komórki przed przejściem w pełną genomiczną chaotyczność.
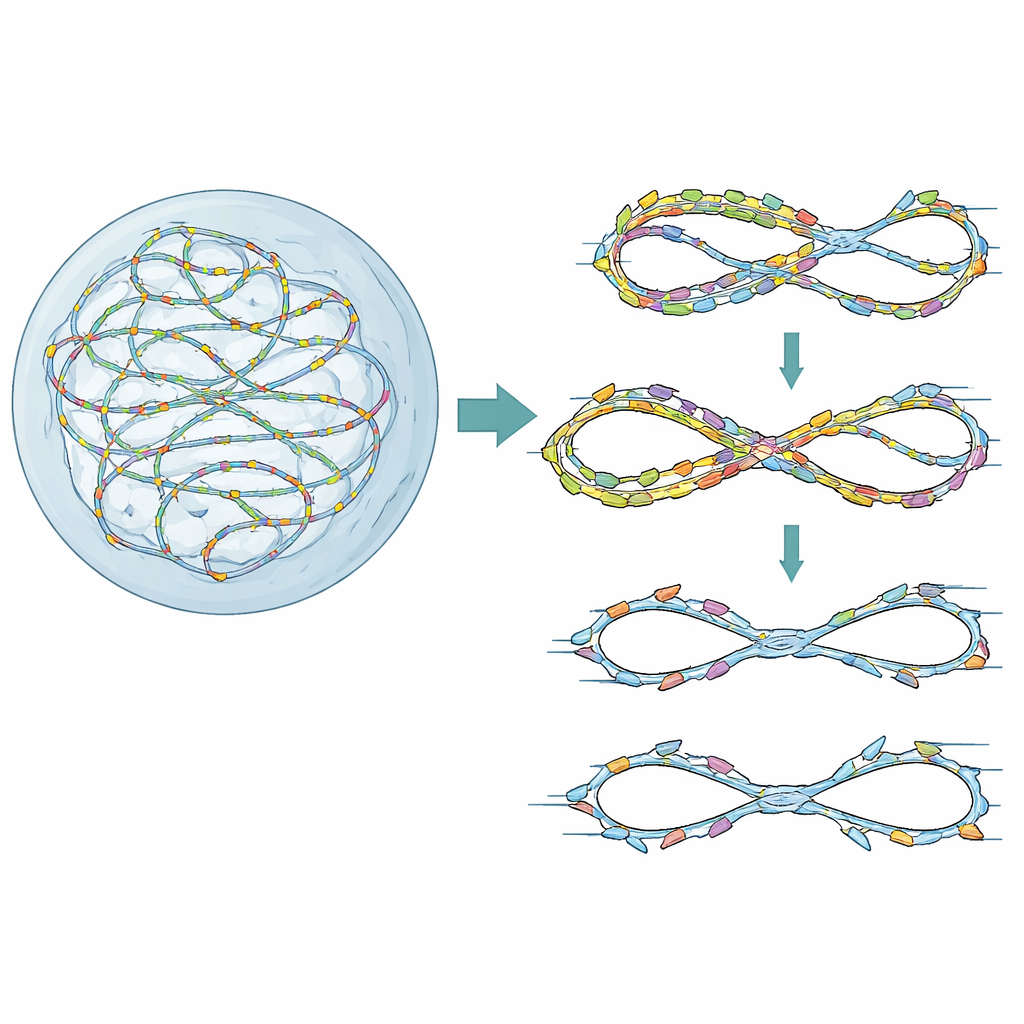
Barierki dla jednokrotnego kopiowania
Nasze chromosomy są dublowane z tysięcy punktów startowych, czyli „originów”, które są aktywowane i zapalane w precyzyjnie zaplanowanym porządku. Małe białko o nazwie Geminin zwykle pomaga zapewnić, że każdy origin zostaje uruchomiony tylko raz w cyklu komórkowym. Gdy Geminin zostaje utracony lub osłabiony, niektóre originy mogą zostać ponownie uruchomione na już skopiowanym DNA — zjawisko znane jako re-replikacja. Komórki nowotworowe, które często nadmiernie wytwarzają czynniki licencjonujące, są szczególnie podatne na ten problem. Autorzy najpierw przeprowadzili wysokowydajny ekran genetyczny w komórkach ludzkich przygotowanych do niskiego poziomu re-replikacji przez deplecję Gemininy. Zbadali, które geny naprawcze DNA i checkpointowe stają się krytyczne w tym stanie stresu i odkryli, że FANCD2, znane głównie z naprawy sprzężeń DNA w zespole Fanconiego, wyłania się jako kluczowy strażnik przeżycia komórek i integralności genomu.
Pierwsza odpowiedź przy przeciążonych „maszynach” kopiujących
Zespół następnie śledził, gdzie i kiedy FANCD2 pojawia się w komórkach przechodzących re-replikację. Krótko po usunięciu Gemininy FANCD2 szybko gromadzi się na chromatynie i tworzy jasne ogniska jądrowe, na długo zanim da się wykryć masowe pęknięcia DNA. Dzięki znakowaniu nowo syntetyzowanego DNA i testom bliskości wykazano, że FANCD2 jest rekrutowany bezpośrednio do aktywnych maszyn replikacyjnych, szczególnie w komórkach, których DNA jest już kopiowane po raz drugi. W synchronizowanych komórkach uwolnionych do następnego cyklu podziałowego pojawiła się odrębna populacja z rozproszonym, wzorcem nadreplikacji DNA. Komórki te wykazywały silne sygnały FANCD2 i RPA, świadczące o trwającym stresie replikacyjnym, i były zatrzymywane przed mitozą przez aktywny checkpoint, co sugeruje, że FANCD2 jest częścią wczesnej odpowiedzi stabilizującej przeciążone widełki, a nie jedynie reakcji na już złamane DNA.
Powstrzymywanie wymykających się widełek i ukrytych szczelin
Aby sprawdzić, jak FANCD2 kształtuje kopiowanie DNA, badacze połączyli utratę Gemininy z deplecją FANCD2. Ku zaskoczeniu, usunięcie FANCD2 nie zwiększyło odsetka komórek z widocznie zreplikowanym genomem. Zamiast tego testy pojedynczych włókien DNA wykazały, że widełki replikacyjne przemieszczały się dalej i stawały się bardziej asymetryczne, co jest oznaką nierównomiernego i niestabilnego postępu. Te szybsze widełki pozostawiały po sobie więcej jednoniciowych szczelin w nowo powstałym DNA, widocznych jako intensywne ogniska RPA i natywnego BrdU oraz potwierdzone wrażliwością znakowanych pasm na enzymy tnące fragmenty jednoniciowe. Komórki pozbawione jednocześnie Gemininy i FANCD2 wykazywały wzrost pęknięć chromosomów, fragmentów, ciałek jądrowych i mikrojadreczek — wszystkie cechy ciężkiej niestabilności genomu. Zablokowanie PARP, czynnika, który normalnie pomaga radzić sobie z takimi szczelinami, naśladowało i pogarszało te defekty, podkreślając, że niekontrolowane tworzenie szczelin jest kluczowe dla powstawania uszkodzeń.
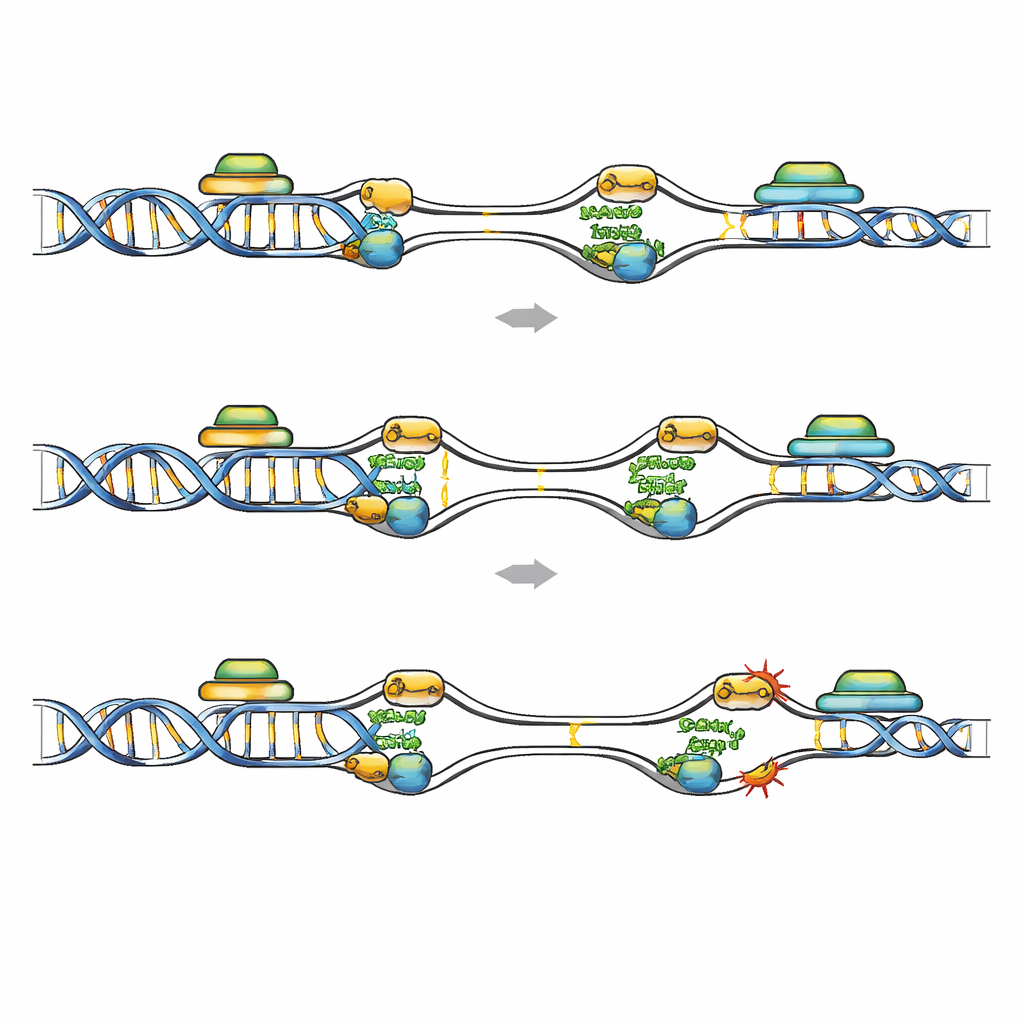
Kruchość w gorących punktach, gdzie kopiowanie zderza się z transkrypcją
Mapowanie wiązania FANCD2 w skali genomowej pokazało, gdzie re-replikacja jest najbardziej niebezpieczna. W komórkach białaczkowych pozbawionych Gemininy FANCD2 przesunęło się z klasycznych wspólnych miejsc kruchości (common fragile sites) na wczesne originy replikacyjne osadzone w krótkich, GC‑bogatych, intensywnie transkrybowanych genach. Te regiony noszą ślady aktywnej transkrypcji i są podatne na formowanie R‑pętli, w których nowo powstający RNA hybrydyzuje z matrycowym DNA, potencjalnie blokując replikację. Publicznie dostępne zbiory danych wykazały więcej uszkodzeń DNA i podwyższone sygnały hybryd RNA–DNA w genach wzbogaconych w FANCD2 po utracie Gemininy, a te regiony pokrywały się z tzw. wczesnymi replikującymi się miejscami kruchości. Gdy transkrypcję ogólnie stłumiono lekiem lub usunięto R‑pętle przez nadekspresję RNazy H1, liczba ognisk FANCD2, RPA i uszkodzeń DNA w komórkach pozbawionych Gemininy znacząco spadła. Wskazuje to, że kolizje między ponownie uruchamianymi originami a aktywnymi jednostkami transkrypcyjnymi, wzmacniane przez R‑pętle, tworzą podatne na uszkodzenia miejsca, które FANCD2 musi chronić.
Dostrajanie ochrony przez chemiczne znaczniki
FANCD2 jest aktywowany częściowo przez przyłączenie małego markera podobnego do ubikwityny. Poprzez deplecję FANCA, rdzennego składnika machinerii znakującej, oraz użycie komórek wyrażających mutant FANCD2 oporny na tę modyfikację, autorzy pokazali, że mono‑ubikwitynacja poprawia przeżywalność komórek re‑replikujących się, ale nie jest absolutnie konieczna. Nawet nieoznakowany FANCD2 zapewniał częściową ochronę, co jest zgodne z odrębnymi rolami w wykrywaniu i stabilizowaniu przeciążonych widełek. Ogólny obraz przedstawia FANCD2 jako czynnik, który spowalnia i organizuje replikację przy wrażliwych wczesnych originach oraz ogranicza liczbę i rozmiar jednoniciowych szczelin.
Dlaczego to ma znaczenie dla leczenia nowotworów
Dla osób niebędących specjalistami kluczowy wniosek jest taki, że nie wszystkie błędy replikacji od razu są katastrofalne. Łagodna re‑replikacja, jak ma to miejsce w niektórych nowotworach, może być tolerowana, jeśli systemy ochronne, takie jak FANCD2, utrzymują wymykające się kopiowanie pod kontrolą i zapobiegają przemianie podatnych szczelin w złamane chromosomy. Gdy ta osłona zostaje usunięta lub przeciążona, te same niskopoziomowe błędy licencjonowania szybko eskalują do rozpadu genomu. Ponieważ utrata Gemininy i defekty licencjonowania replikacji są wzbogacone w komórkach nowotworowych, a wiele guzów ma już osłabioną sieć Fanconi/BRCA, ujawnione tu podatności sugerują strategie terapeutyczne: łączenie inhibitorów skłaniających komórki nowotworowe ku re‑replikacji z lekami nasilającymi akumulację szczelin, np. inhibitorami PARP, mogłoby selektywnie zepchnąć komórki złośliwe za granicę tolerancji, oszczędzając normalne komórki z nienaruszoną ochroną.
Cytowanie: Badra-Fajardo, N., Karydi, E., Bayona-Feliu, A. et al. FANCD2 restrains fork progression and prevents fragility at early origins upon re-replication. Nat Commun 17, 2478 (2026). https://doi.org/10.1038/s41467-026-68966-4
Słowa kluczowe: Stres podczas replikacji DNA, FANCD2, Geminin, re-replikacja, niestabilność genomu