Clear Sky Science · pl
Składanie indukowane asocjacją kontroluje montaż zastępczej łańcuchu lekkiego i rdzenia receptora pre-B
Jak nasze ciało testuje nowe przeciwciała
Zanim młody limfocyt B w szpiku kostnym zostanie dopuszczony do układu odpornościowego, musi przejść surowy test: czy potrafi zbudować działające jądro przeciwciała? Artykuł bada, jak specjalna „próbna” wersja części przeciwciała, zwana zastępczym łańcuchem lekkim, pomaga przeprowadzić ten test. Śledząc, jak te białka się fałdują i dopasowują, autorzy ujawniają ukryty system kontroli jakości, który decyduje, które przyszłe przeciwciała są wystarczająco dobre, by je zatrzymać — a które należy odrzucić.
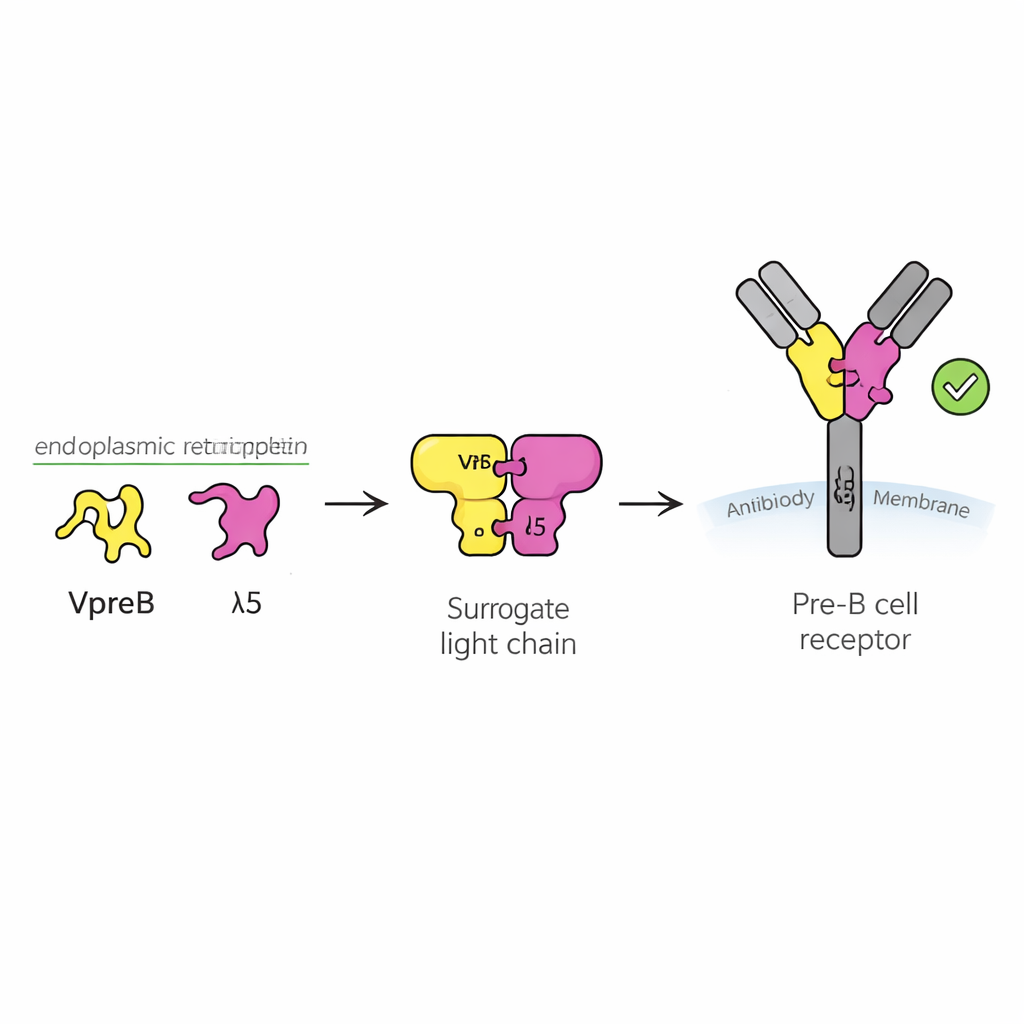
Checkpoint bezpieczeństwa dla młodych komórek odpornościowych
Przeciwciała to białka w kształcie litery Y, które rozpoznają napastników. Składają się z dwóch głównych części: łańcuchów ciężkich i lekkich. Podczas rozwoju limfocytu B najpierw powstaje łańcuch ciężki i komórka musi ocenić, czy ten nowy łańcuch ciężki jest użyteczny, zanim zainwestuje energię w produkcję dopasowanego łańcucha lekkiego. W tym celu komórka używa tymczasowego substytutu zwanego zastępczym łańcuchem lekkim, złożonego z dwóch białek: VpreB i λ5. Razem z łańcuchem ciężkim tworzą receptor pre-B na powierzchni komórki, który wysyła sygnał „idź” lub „stop”. Około połowa nowo zrekonfigurowanych łańcuchów ciężkich nie przechodzi tego testu, więc zrozumienie działania zastępczego łańcucha lekkiego jest kluczowe dla poznania, jak powstaje zdrowy repertuar przeciwciał.
Fałdowanie przez asocjację: pomoc niestabilnemu partnerowi
Autorzy wykazali, że jeden z komponentów, VpreB, w izolacji jest w dużej mierze niefałdowany i niestabilny. Przy użyciu technik biofizycznych pokazali, że przyjmuje właściwą trójwymiarową formę dopiero po związaniu się z λ5. Krótki fragment λ5, ukształtowany jak pasmo beta, wsuwa się w VpreB i dopełnia jego strukturę, niczym brakujący ząb w przekładni. To „fałdowanie indukowane asocjacją” nie tylko stabilizuje VpreB, lecz także tworzy bardzo mocne partnerstwo między tymi dwoma białkami, o powinowactwie w zakresie niskich nanomoli. W komórkach dopiero gdy VpreB i λ5 zmontują się w zastępczy łańcuch lekki, unikają zatrzymania w retikulum endoplazmatycznym i mogą być wydzielane lub transportowane dalej, co podkreśla ścisłe sprzężenie między fałdowaniem a kontrolą jakości.
Wykończenie łańcucha ciężkiego i zdanie inspekcji
Historia nie kończy się na VpreB i λ5. Kluczowy fragment łańcucha ciężkiego, zwany CH1, początkowo jest nieuporządkowany i utrzymywany wewnątrz komórki. Badacze wykazali, że λ5, działając częściowo jak czaperon, może wywołać fałdowanie CH1 w momencie ich związania. Ten drugi etap fałdowania indukowanego asocjacją jest niezbędny do zbudowania pełnego receptora pre-B i umożliwienia mu opuszczenia retikulum endoplazmatycznego oraz dotarcia na powierzchnię komórki. Co interesujące, obie części zastępczego łańcucha lekkiego — VpreB i λ5 — mogą kontaktować się z łańcuchem ciężkim, lecz tylko λ5 jest zdolne przeprowadzić CH1 do jego gotowego, zdolnego do fałdowania stanu. Jeśli to się nie zdarzy, częściowy receptor zostaje zatrzymany, a komórka w praktyce odrzuca dany łańcuch ciężki.
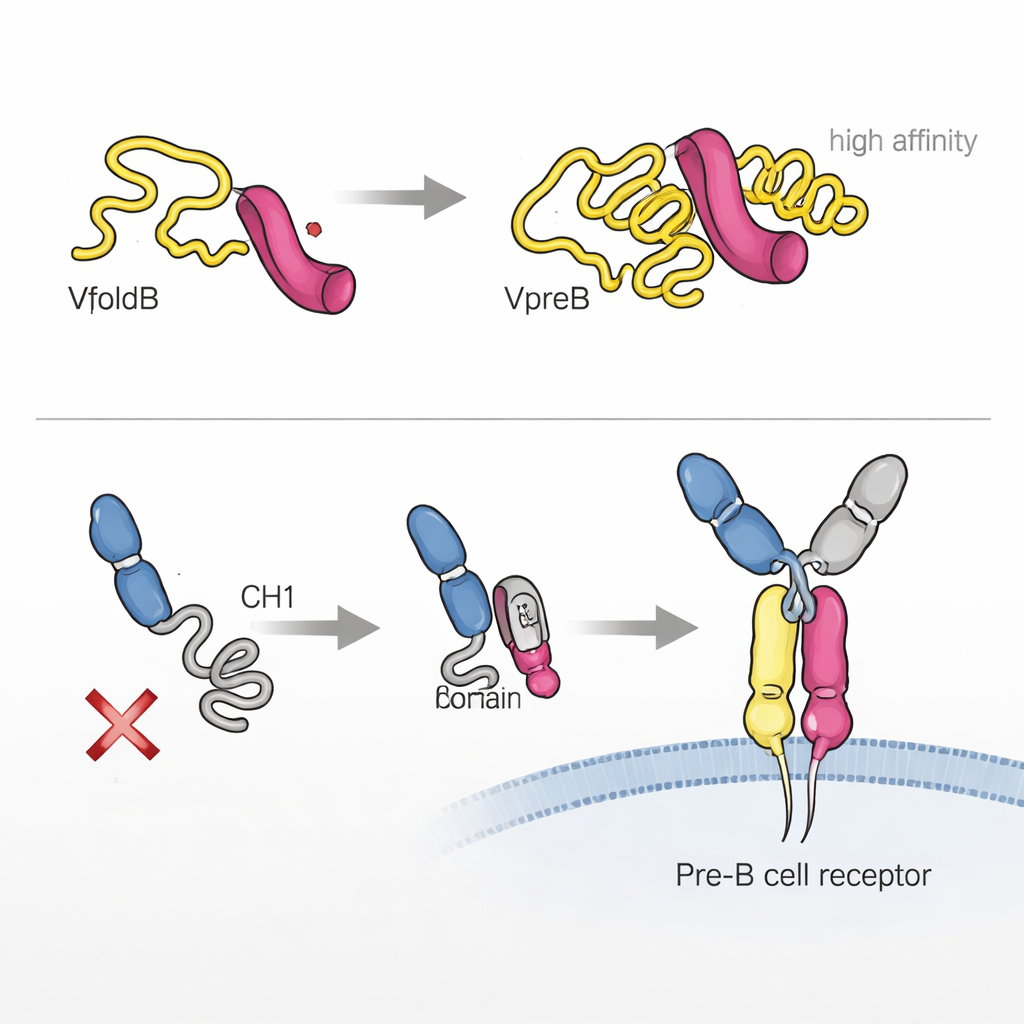
Elastyczne ogony, które dopracowują wiązanie i sygnalizację
Zarówno VpreB, jak i λ5 mają luźne, nieuporządkowane fragmenty zwane regionami unikalnymi, które nie przypominają żadnych znanych sekwencji białkowych. Chociaż te „ogona” nie są bezwzględnie potrzebne do złożenia białek w probówce, zespół odkrył, że silnie wpływają na tempo tworzenia zastępczego łańcucha lekkiego, jego stabilność oraz na to, jak dobrze wiąże się z fragmentami łańcucha ciężkiego. W komórkach usunięcie tych regionów zmniejszało efektywność wydzielania złożonych kompleksów. Szczególnie ogon λ5 okazał się wielozadaniowy: przyspiesza montaż, jest niezbędny do pewnych kontaktów z zmiennym regionem łańcucha ciężkiego i znacząco wpływa na to, jak receptor pre-B angażuje antygeny i inne ligandów. W niektórych przypadkach siła wiązania kombinacji zastępczego łańcucha lekkiego i łańcucha ciężkiego zbliżała się do tej obserwowanej dla normalnego fragmentu przeciwciała.
Dlaczego to ma znaczenie dla różnorodności przeciwciał
Mapując te etapowe zdarzenia fałdowania i montażu, autorzy proponują, że zastępczy łańcuch lekki robi więcej niż tylko podtrzymywać łańcuch ciężki. Działa jak dynamiczny inspektor, używając swojej ustrukturyzowanej części i elastycznych ogonów, by wyczuć, czy łańcuch ciężki potrafi się poprawnie złożyć i produktywnie wchodzić w interakcje z potencjalnymi celami. Udane kombinacje są fałdowane, stabilizowane i dopuszczane do dotarcia na powierzchnię komórki, gdzie wysyłają sygnały pozwalające limfocytowi B kontynuować dojrzewanie. Wadliwe kombinacje zostają uwięzione i ostatecznie eliminowane. Dla laika sedno sprawy jest takie: twój układ odpornościowy uruchamia wyrafinowany „stanowisko testowe” dla przyszłych przeciwciał, zbudowane z białek, które dosłownie składają się nawzajem, zapewniając, że tylko dobrze zachowujące się rdzenie przeciwciał przejdą dalej, by cię chronić.
Cytowanie: König, J., Sarmiento Alam, N.C., He, R. et al. Association-induced folding governs surrogate light chain and pre-B cell receptor core assembly. Nat Commun 17, 1202 (2026). https://doi.org/10.1038/s41467-026-68965-5
Słowa kluczowe: Rozwój limfocytów B, fałdowanie przeciwciał, zastępczy łańcuch lekki, kontrola jakości białek, receptor pre-B