Clear Sky Science · pl
Odblokowanie enzymatycznej deracemizacji strukturalnie zróżnicowanych allenów przez zaprojektowane fotoenzymy
Dlaczego dobieranie i łączenie cząsteczek ma znaczenie
Wiele leków działa tylko wtedy, gdy ich atomy są ułożone w bardzo specyficzny, trójwymiarowy sposób — podobnie jak lewa dłoń pasuje do lewej rękawiczki, a nie do prawej. Chemicy potrafią często wytwarzać takie „jednoręczne” cząsteczki, ale trudniej zrobić to czysto, gdy cegiełki są złożone. Artykuł podejmuje to wyzwanie dla trudnej klasy skręconych struktur zwanych allenami, wykorzystując zaprojektowane enzymy napędzane światłem. Praca pokazuje, jak biologia i fotochemia mogą współpracować, aby wyodrębnić pożądaną „rękę” cząsteczki z pomieszaniny, obiecując szybsze i czystsze ścieżki do przyszłych leków i materiałów.
Skręcone cegiełki z dużym zwrotem korzyści
Alleny to liniowe łańcuchy trzech atomów węgla z dwoma sąsiednimi wiązaniami podwójnymi, lecz ta prosta konfiguracja powoduje skręcenie przestrzeni, które nadaje cząsteczce chiralność. Ten osiowy skręt pojawia się w produktach naturalnych, środkach ochrony roślin i zaawansowanych katalizatorach. Niestety tradycyjne metody wytwarzania chiralnych allenów mają tendencję do dużej specjalizacji: katalizator, który doskonale działa dla jednego allenu, często zawodzi dla innego przy niewielkiej zmianie budowy. Nawet niedawno opracowane chemiczne katalizatory aktywowane światłem zmagają się z tym problemem. W rezultacie chemicy muszą wielokrotnie projektować katalizatory od podstaw, gdy chcą badać nowe alleny, co spowalnia odkrycia i zwiększa odpady.
Zap借�anie selektywności natury i dodanie światła
Enzymy w systemach żywych doskonale rozpoznają i przekształcają specyficzne kształty z niezwykłą precyzją, ale ewoluowały do naturalnych celów, a nie do syntetycznych allenów. Autorzy postawili sobie za cel stworzenie „fotoenzymu”, który łączy selektywność przypominającą enzymy z możliwością pozyskiwania światła jako źródła energii. Zaczęli od rusztowania białkowego nazwanego CTB10 i genetycznie przebudowali je tak, aby zawierało nienaturalny aminokwas działający jak maleńka wbudowana antena świetlna. Gdy ten specjalny składnik pochłania ultrafiolet, może przekazać energię pobliskiemu allenowi, tymczasowo go wzbudzając i umożliwiając przemieszanie jego skrętu. Poprzez powtarzanie tego procesu wielokrotnie enzym może selektywnie usunąć jedną „rękę” z mieszaniny 50:50 i pozostawić głównie tę drugą. 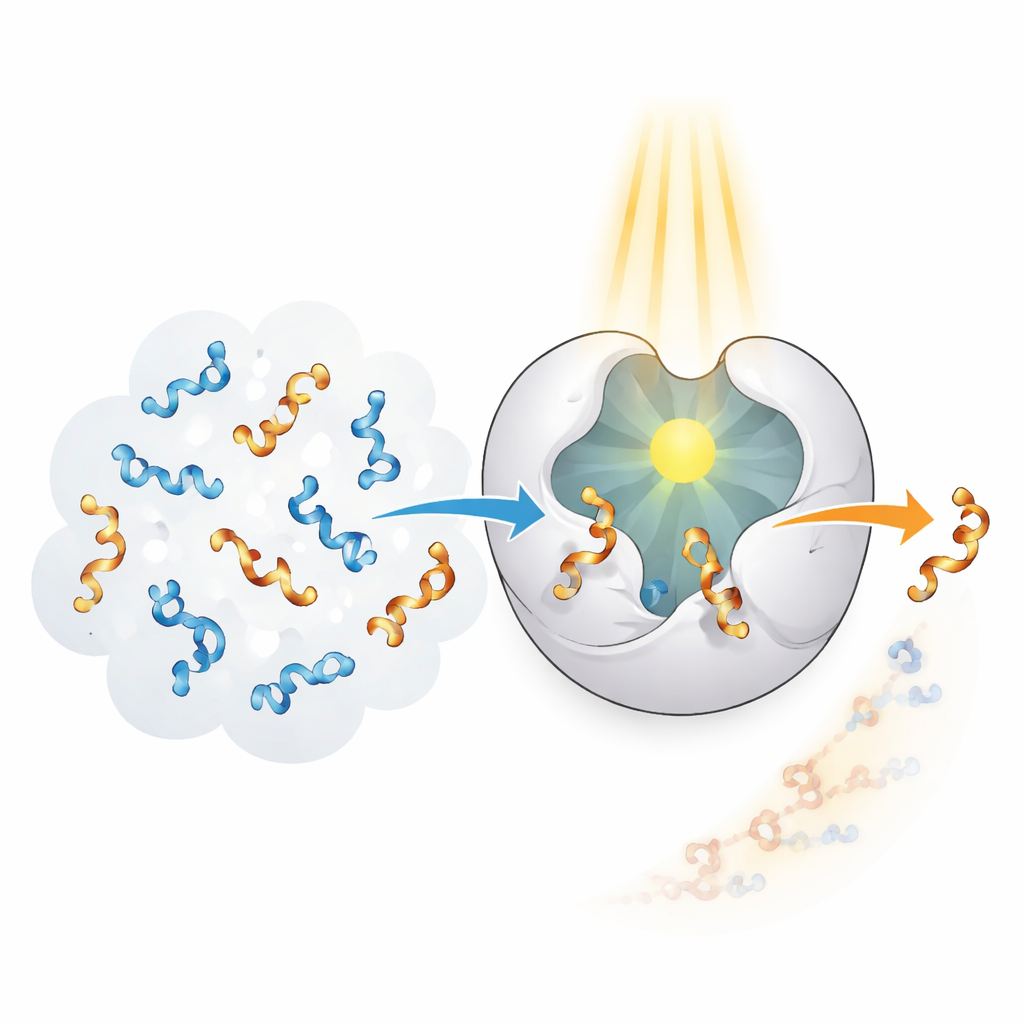
Wyrzeźbienie dopasowanych kieszeni dla różnych gości
Zaplanowanie takiego systemu nie sprowadza się do prostego naświetlania białka. Zespół użył modelowania komputerowego, strategicznych mutacji i zdjęć rentgenowskich, aby wyrzeźbić kilka wersji fotoenzymu, z których każda miała nieco inną wewnętrzną kieszeń. Te kieszenie utrzymują alleny w określonej pozie obok anteny świetlnej i stabilizują kluczowe części cząsteczki przez wiązania wodorowe oraz subtelne oddziaływania upakowania. Krok po kroku badacze poprawili zarówno siłę wiązania, jak i wyrównanie między enzymem a allenem, co jest kluczowe dla wydajnego transferu energii. Ostateczne warianty wykazały imponującą wydajność, przekształcając kwasy allenowe, estry i amidy w produkty o jednej preferowanej „ręce” z bardzo wysoką czystością, często powyżej 99% jednego enancjomeru, i to w warunkach powietrza bez potrzeby delikatnych procedur.
Obserwacja mechanizmu w rozdzielczości atomowej
Aby zrozumieć, dlaczego nowe fotoenzymy preferują jedną „rękę” nad drugą, autorzy krystalizowali pary enzym‑substrat i badali je w rozdzielczości atomowej. Stwierdzili, że preferowana konfiguracja allenowa leży bliżej grupy pochłaniającej światło i może przyjmować kilka nieco różnych kształtów, wszystkie zgodne z wydajnym transferem energii. Niepreferowana konfiguracja albo wiąże się słabo, albo znajduje się dalej, co znacznie zmniejsza prawdopodobieństwo jej wzbudzenia. Dodatkowe eksperymenty z czystymi praworęcznymi i leworęcznymi materiałami wyjściowymi potwierdziły tę przewagę: enzym szybko przekształca preferowaną „rękę” w reaktywny pośrednik, który następnie w roztworze relaksuje do mieszaniny, w której akumuluje się przeciwna „ręka”. W istocie białko zachowuje się jak molekularna bramka, wielokrotnie wzbudzając i zużywając jedną „rękę”, podczas gdy druga się gromadzi. 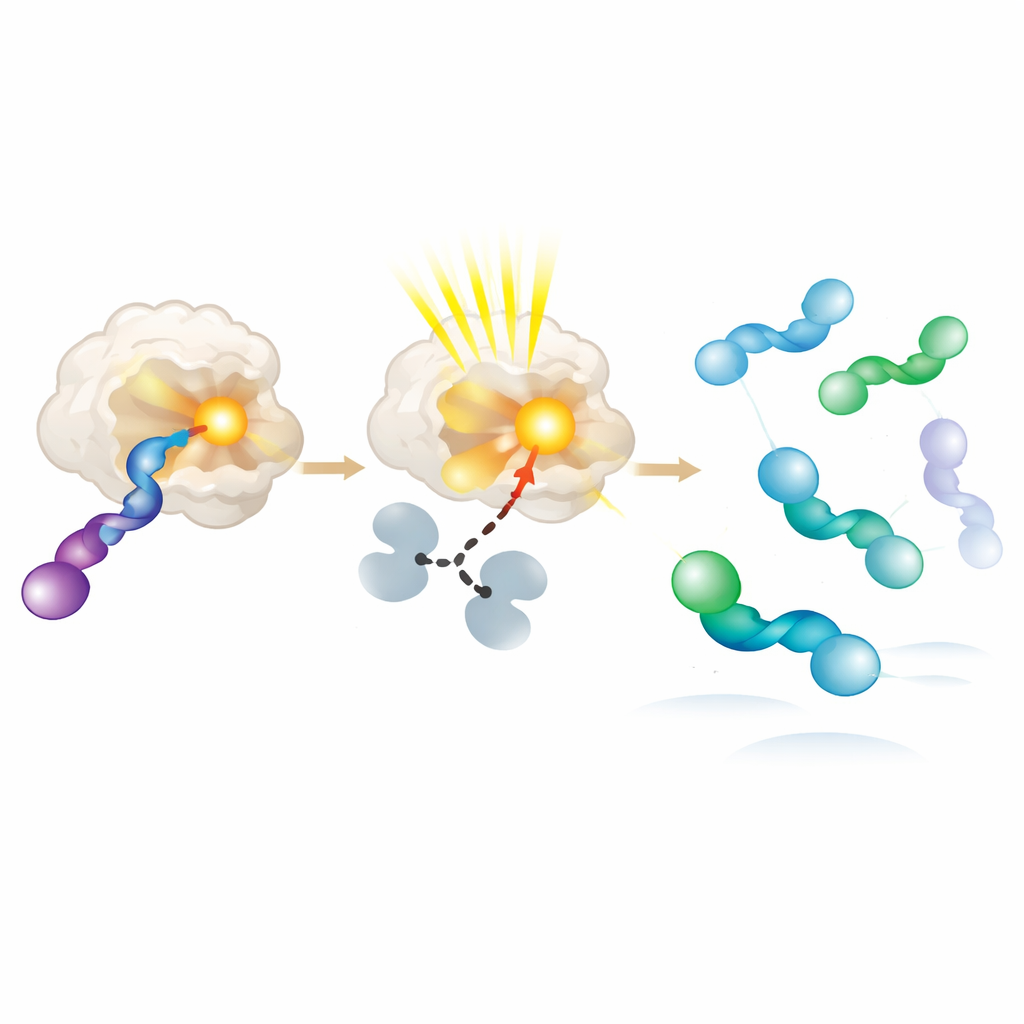
Co to oznacza dla przyszłej chemii
Dla osób niebędących specjalistami główne przesłanie jest takie, że zespół stworzył programowalną maszynę białkową, która używa światła do sortowania i udoskonalania skręconych cząsteczek z niespotykaną wszechstronnością. Zamiast projektować zupełnie nowy chemiczny katalizator dla każdego celu, badacze mogą teraz startować od tej platformy fotoenzymu i dostrajać jej wewnętrzną kieszeń, aby przyjmowała wiele różnych allenów. Podejście to zmniejsza przepaść między wyrafinowaną kontrolą natury a potrzebą przemysłu chemicznego na szerokie, solidne metody. W dłuższej perspektywie takie enzymy zasilane światłem mogą pomóc chemikom w przygotowywaniu złożonych, jednoręcznych cegiełek do leków i materiałów efektywniej, przy mniejszej liczbie etapów i mniejszej ilości odpadów.
Cytowanie: Fu, K., Li, M., Deng, Z. et al. Unlocking enzymatic deracemization of structurally diverse allenes by designed photoenzymes. Nat Commun 17, 2082 (2026). https://doi.org/10.1038/s41467-026-68964-6
Słowa kluczowe: fotoenzym, deracemizacja, chiralny allen, biokataliza, transfer energii tripletowej