Clear Sky Science · pl
Infekcja HCMV zaburza funkcje bariery i sprzyja przejściu nabłonkowo-mezenchymalnemu w modelu organoidu cholangiocytów
Dlaczego ta historia o wirusie w wątrobie ma znaczenie
Ludzki cytomegalowirus jest bardzo powszechnym wirusem, który większość z nas nosi bez wiedzy o tym. Jednak u noworodków i osób z osłabionym układem odpornościowym może wiązać się z poważnymi problemami w obrębie wątroby i dróg żółciowych, w tym z rzadką, ale wyniszczającą chorobą dziecięcą zwaną atrezją dróg żółciowych. W badaniu użyto miniaturowych, hodowanych w laboratorium ludzkich dróg żółciowych, aby pokazać, jak wirus może bezpośrednio uszkadzać te delikatne przewody i wywoływać zmiany bliznowate, które mogą pomóc wyjaśnić długo dyskutowane związki między infekcją a przewlekłą chorobą wątroby.
Bliższe spojrzenie na powszechny, lecz skryty wirus
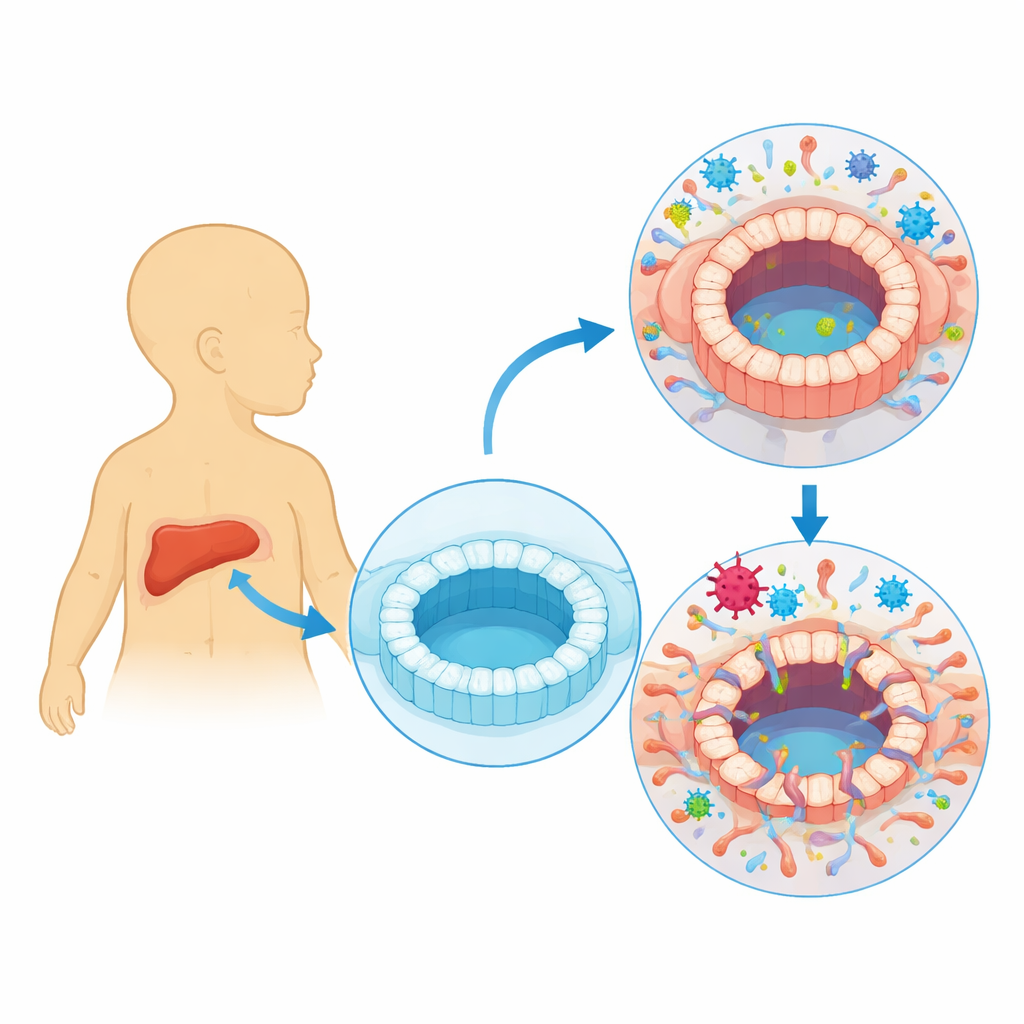
Ludzki cytomegalowirus (HCMV) zwykle bytuje w naszych organizmach w sposób ukryty, przechodząc między fazą aktywną, gdy produkuje nowe cząstki wirusa, a fazą utajenia, gdy ukrywa się w niektórych komórkach krwi. Lekarze od dawna obserwują, że osoby z aktywną infekcją HCMV mogą rozwijać uszkodzenia dróg żółciowych i cholestazę, w której żółć nie odpływa prawidłowo. Wiele niemowląt z atrezją dróg żółciowych — stanem, w którym przewody żółciowe zostają zablokowane i zbliznowacone wkrótce po urodzeniu — wykazuje również oznaki niedawnej infekcji HCMV. Nie było jednak jasne, czy wirus faktycznie zakaża komórki wyściełające przewody żółciowe, czy też pojawia się jedynie jako towarzysz choroby.
Budowanie małych przewodów żółciowych w probówce
Aby to sprawdzić, naukowcy stworzyli trójwymiarowe „organoidy” naśladujące ludzkie przewody żółciowe. Rozpoczęli od indukowanych pluripotentnych komórek macierzystych, przeprogramowanych z ludzkiej krwi, i ukierunkowali je, by różnicowały się w komórki podobne do cholangiocytów — typu komórek wyściełających przewody żółciowe. Komórki te samoorganizowały się w puste kule z centralną jamą i ścisłymi połączeniami międzykomórkowymi, przypominając zminiaturyzowany przewód żółciowy. Zespół następnie narażał te organoidy na szczep HCMV opatrzony fluorescencyjnym znacznikiem, który świeci, gdy wirus aktywnie replikuje się. Pozwoliło to śledzić zakażone komórki i mierzyć zmiany w organoidach w czasie.
Jak infekcja deformuje strukturę i osłabia barierę
Po zakażeniu organoidy przestały rosnąć normalnie i stały się zdeformowane, z pogrubionymi i nieregularnymi ścianami. Niektóre komórki jasno świeciły, co wskazywało na pełną aktywność wirusa i produkcję nowych cząstek; inne zawierały materiał genetyczny wirusa na niższym poziomie, sugerując bardziej utajony stan przypominający latencję. Testy funkcjonalne wykazały, że zakażone organoidy utraciły kluczowe zdolności przewodów żółciowych. Przestały prawidłowo pęcznieć w odpowiedzi na bodziec zależny od kanałów transportu jonów i wykazywały większe przecieki w teście oporu elektrycznego mierzącym szczelność bariery. Białka zwykle uszczelniające przestrzenie między komórkami, takie jak składniki zamków szczelnych, były zmniejszone, a transport próbnego barwnika do wnętrza i z jamy centralnej stał się nieprawidłowy. Razem te zmiany pokazują, że HCMV może bezpośrednio osłabić ścianę przewodu żółciowego, czyniąc ją nieszczelną i dysfunkcyjną.
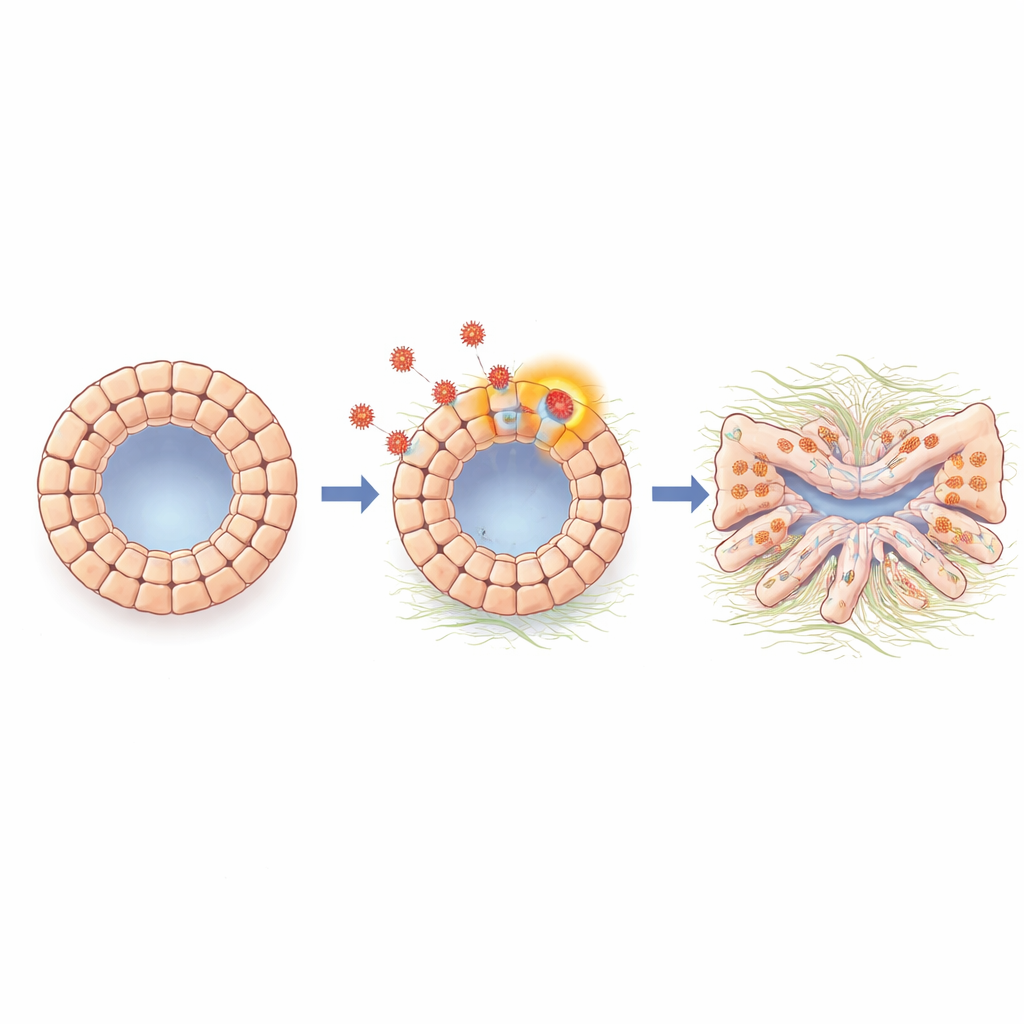
Komórki zmieniają tożsamość w kierunku stanu bliznowacenia
Wnikliwsze analizy aktywności genów w organoidach, przeprowadzone metodami grupowymi i na poziomie pojedynczej komórki, wykazały silną aktywację programu przypominającego przejście nabłonkowo-mezenchymalne (EMT). To proces, w którym ciasno powiązane komórki powierzchniowe rozluźniają więzi, przyjmują bardziej ruchliwy, włóknisty charakter i zaczynają produkować cząsteczki związane z bliznowaceniem tkanki. Zakażone organoidy wykazywały podwyższone poziomy N-kadheryny i innych markerów związanych z tą zmianą, a także genów uczestniczących w tworzeniu włóknienia i macierzy pozakomórkowej. Cząsteczka sygnałowa zwana TGF-beta, dobrze znana z napędzania bliznowacenia w wielu narządach, była nasilona podczas infekcji. Gdy zespół zablokował sygnalizację TGF-beta za pomocą małocząsteczkowego inhibitora lub przeciwciała, organoidy odzyskały bardziej normalny kształt, a wiele genów związanych ze stanuem przejścia i bliznowaceniem wróciło w kierunku wartości wyjściowych, co wskazuje, że TGF-beta jest kluczowym pośrednikiem łączącym obecność wirusa ze szkodliwymi zmianami komórkowymi.
Z probówek do chorych dzieci
Aby sprawdzić, czy te obserwacje z laboratorium odnoszą się do rzeczywistej choroby, badacze przeanalizowali tkankę wątrobową dzieci z atrezją dróg żółciowych i z innymi pediatrycznymi schorzeniami wątroby. Przy użyciu czułych sond wykryli DNA HCMV w cholangiocytach — komórkach przewodów żółciowych — w około dwóch trzecich próbek od pacjentów z atrezją, ale znacznie rzadziej w wątrobach bez atrezji. W tych samych obszarach, gdzie znaleziono DNA wirusa, komórki przewodów żółciowych miały wyższe poziomy TGF-beta i N-kadheryny, odpowiadające wzorcowi przejścia i bliznowacenia widzianemu w organoidach. Sugeruje to, że przynajmniej u części dzieci HCMV zakaża bezpośrednio komórki przewodów żółciowych i przesuwa je w kierunku stanu włóknienia poprzez aktywację dróg zależnych od TGF-beta.
Co to oznacza dla rozumienia i leczenia chorób dróg żółciowych
Mówiąc prosto, ta praca pokazuje, że powszechny wirus może zainwadować komórki wyściełające przewody żółciowe, rozluźnić ich ścisłe połączenia i pchnąć je w stronę bliznowaciałego, mniej wyspecjalizowanego stanu poprzez sygnał oparty na TGF-beta. Zmiany te osłabiają funkcje bariery i transportu przewodów i mogą przyczyniać się do zatkanych, zbliznowaciałych przewodów obserwowanych w chorobach takich jak atrezja dróg żółciowych. Chociaż nie każdy przypadek choroby przewodów żółciowych będzie spowodowany HCMV, badanie wzmacnia hipotezę, że u podatnych niemowląt infekcja wirusowa może być istotnym elementem układanki — oraz że celowanie w szlaki związane z TGF-beta mogłoby pewnego dnia pomóc chronić lub przywracać wrażliwe przewody żółciowe.
Cytowanie: Ye, Z., Hu, X., Rahaman, S.M. et al. HCMV infection disrupts barrier functions and promotes epithelial–mesenchymal transition in a cholangiocyte organoid model. Nat Commun 17, 2273 (2026). https://doi.org/10.1038/s41467-026-68962-8
Słowa kluczowe: cytomegalowirus, atresia dróg żółciowych, organoidy przewodów żółciowych, przejście nabłonkowo-mezenchymalne, szlak TGF-beta