Clear Sky Science · pl
Dywergentna fotochemiczna wymiana pierścienia izoksazoli
Światło skierowane na bloki konstrukcyjne leków
Wiele współczesnych leków zbudowanych jest z małych, pierścieniowych fragmentów, które decydują o zachowaniu cząsteczki w organizmie. Chemicy często chcą wymienić jeden taki pierścień na pokrewny, aby dopracować aktywność, lecz zazwyczaj wiąże się to z koniecznością odbudowy całej cząsteczki od podstaw. Badanie to pokazuje, że starannie dobrane promieniowanie ultrafioletowe może bezpośrednio przekształcić powszechny pierścień zwany izoksazolem w kilka innych przydatnych pierścieni, co może zaoszczędzić czas, koszty i nakład pracy w odkrywaniu leków.
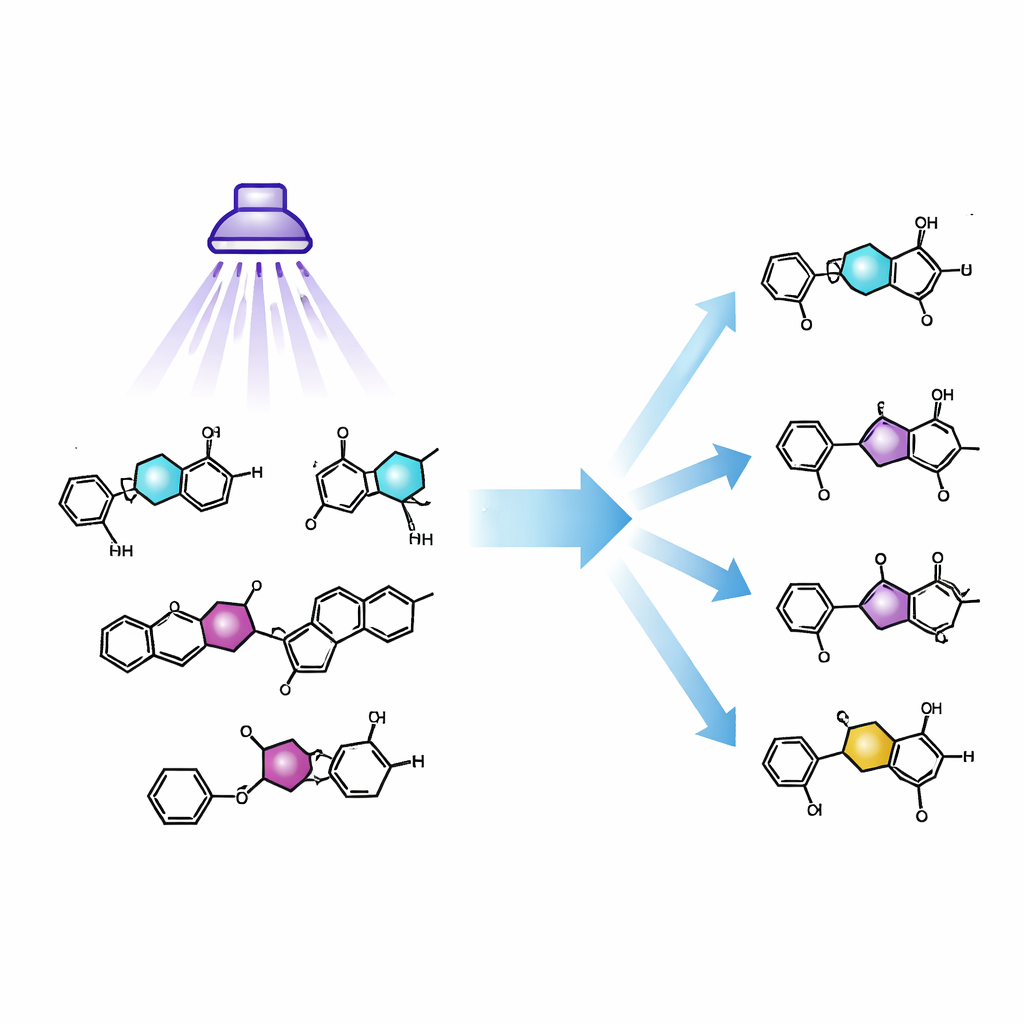
Dlaczego te małe pierścienie mają znaczenie
Pierścienie pięcioczłonowe zawierające atomy tlenu, azotu lub siarki są powszechne w farmaceutykach i środkach ochrony roślin. Izoksazole i oksazole szczególnie często zastępują typowe elementy jak ketony czy estry, często poprawiając stabilność i aktywność leku. Kiedy badacze sprawdzają, jak zmiana pierścienia wpływa na aktywność biologiczną, zwykle przygotowują oddzielną wersję cząsteczki dla każdego typu pierścienia — pracochłonny proces zwany syntezą de novo. Metoda, która pozwoliłaby zacząć od pojedynczego leada opartego na izoksazolu i bezpośrednio przekształcić jego pierścień w kilka bliskich krewnych, znacznie przyspieszyłaby eksplorację przestrzeni chemicznej.
Wykorzystanie światła jako narzędzia precyzyjnego
Autorzy odkryli, że naświetlanie izoksazolów światłem ultrafioletowym może uruchomić wysoce selektywne przearanżowania, o ile „ozdoby” cząsteczki i otaczający rozpuszczalnik zostaną dobrane ostrożnie. Z prostego izoksazolu znaleźli warunki, w których światło przekształca go w oksazol, albo alternatywnie rozrywa pierścień, tworząc pośrednik zwany alfa-ketonitrylem. Wcześniejsze prace sygnalizowały podobne zachowanie, lecz cierpiały na niskie wydajności i nieczyste mieszaniny produktów. Tutaj zespół systematycznie zmieniał podstawienia pierścienia i rozpuszczalnik, mapując, kiedy dochodzi do czystej wymiany pierścienia, a kiedy cząsteczka rozpada się lub pozostaje niezmieniona.
Zajrzeć pod maskę dzięki teorii
Aby zrozumieć, dlaczego niewielkie zmiany strukturalne prowadzą do tak różnych rezultatów, badacze sięgnęli po obliczenia kwantowo-chemiczne. Studia komputerowe pokazują, że po absorpcji światła izoksazol chwilowo przechodzi do stanu wzbudzonego, w którym pęka kluczowe wiązanie, tworząc wysokoenergetyczny pośrednik. Stamtąd układ może albo ponownie się zamknąć do pierwotnego pierścienia, skurczyć się do trójczłonowego „azirynu”, albo ulec dalszemu przearanżowaniu. Czy proces przejdzie dalej w stronę nowego pierścienia, czy zgaśnie w rozkładzie, zależy wrażliwie od położenia podstawników na pierścieniu i tego, na ile poszczególne pośrednie formy pochłaniają dodatkowe światło. Analiza ta wykazała, że izoksazole z określonymi grupami w specyficznym położeniu pierścienia są szczególnie dobrze predysponowane do kontrolowanej wymiany pierścienia.
Z jednego pierścienia w wiele
Wyposażeni w te obserwacje, autorzy skupili się na rodzinie izoksazoli, które reagują na światło w sposób powtarzalny. W rozpuszczalnikach alkoholowych te substraty płynnie przeobrażają się w oksazole w łagodnych warunkach i tolerują szeroki zakres dodatkowych grup funkcyjnych, w tym delikatne fragmenty często spotykane w kandydatach na leki. W mniej polarnym rozpuszczalniku to samo naświetlanie prowadzi natomiast do powstania pośrednika alfa-ketonitrylu, który w jednej probówce można przekształcić w kilka innych pierścieni — pyrazole, pirolowe pierścienie, amino-podstawione izoksazole oraz izotiazole — przy użyciu prostych reakcji następczych. Rozpoczynając od zaledwie siedmiu dostępnych komercyjnie izoksazoli, autorzy zbudowali bibliotekę 34 różnych produktów heterocyklicznych bez konieczności odbudowy żadnej cząsteczki od podstaw.
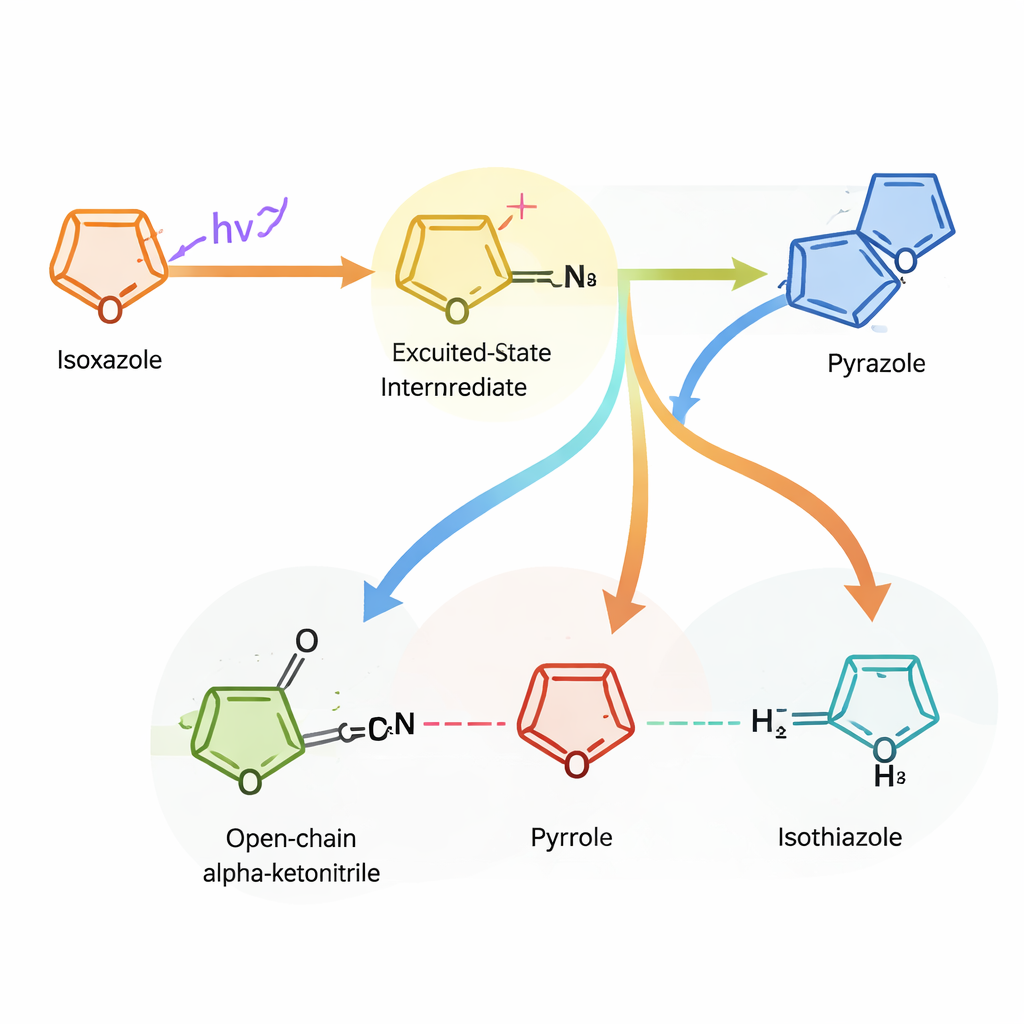
Implikacje dla przyszłych leków
Praca ta wprowadza praktyczny sposób „edycji” rdzenia pierścienia złożonych cząsteczek późno w syntezie, zamiast ich odbudowywania z prostszych elementów. Dzięki użyciu światła do wywołania selektywnego przebudowania pierścienia chemicy mogą szybko wygenerować rodziny blisko spokrewnionych struktur i przetestować, jak każda z nich zachowuje się w układach biologicznych. Łagodne warunki metody i zgodność z rzeczywistymi cząsteczkami leków wskazują, że może się ona stać cennym narzędziem dla chemików medycznych poszukujących lepszych terapii przy mniejszej liczbie etapów syntezy.
Cytowanie: Xu, Y., Poletti, L., Arpa, E.M. et al. Divergent photochemical ring-replacement of isoxazoles. Nat Commun 17, 2141 (2026). https://doi.org/10.1038/s41467-026-68960-w
Słowa kluczowe: fotochemiczne edytowanie pierścieni, remodelowanie izoksazoli, dywersyfikacja heterocykli, metody chemii medycznej, skok szkieletowy