Clear Sky Science · pl
Zrozumienie wpływu metali alkalicznych na katalizę hydrogenacji poprzez Silną Interakcję Metal–Zasada
Dlaczego dopracowywanie katalizatorów ma znaczenie w codziennym życiu
Przekształcanie prostych cząsteczek, takich jak dwutlenek węgla i wodór, w użyteczne paliwa i chemikalia jest kluczowe dla czystszej energii i bardziej ekologicznego przemysłu. Wiele metalicznych katalizatorów stosowanych w tych reakcjach zawiera niewielkie ilości metali alkalicznych, takich jak sód czy potas, pełniących rolę „promotorów”, lecz ich rzeczywista rola była dotąd zaskakująco niejasna. Niniejsze badanie ujawnia zjednoczoną zasadę działania tych dodatków, oferując sposób na projektowanie inteligentniejszych katalizatorów, które mogą skierować reakcje w stronę pożądanych produktów i zmniejszyć ilość odpadów.
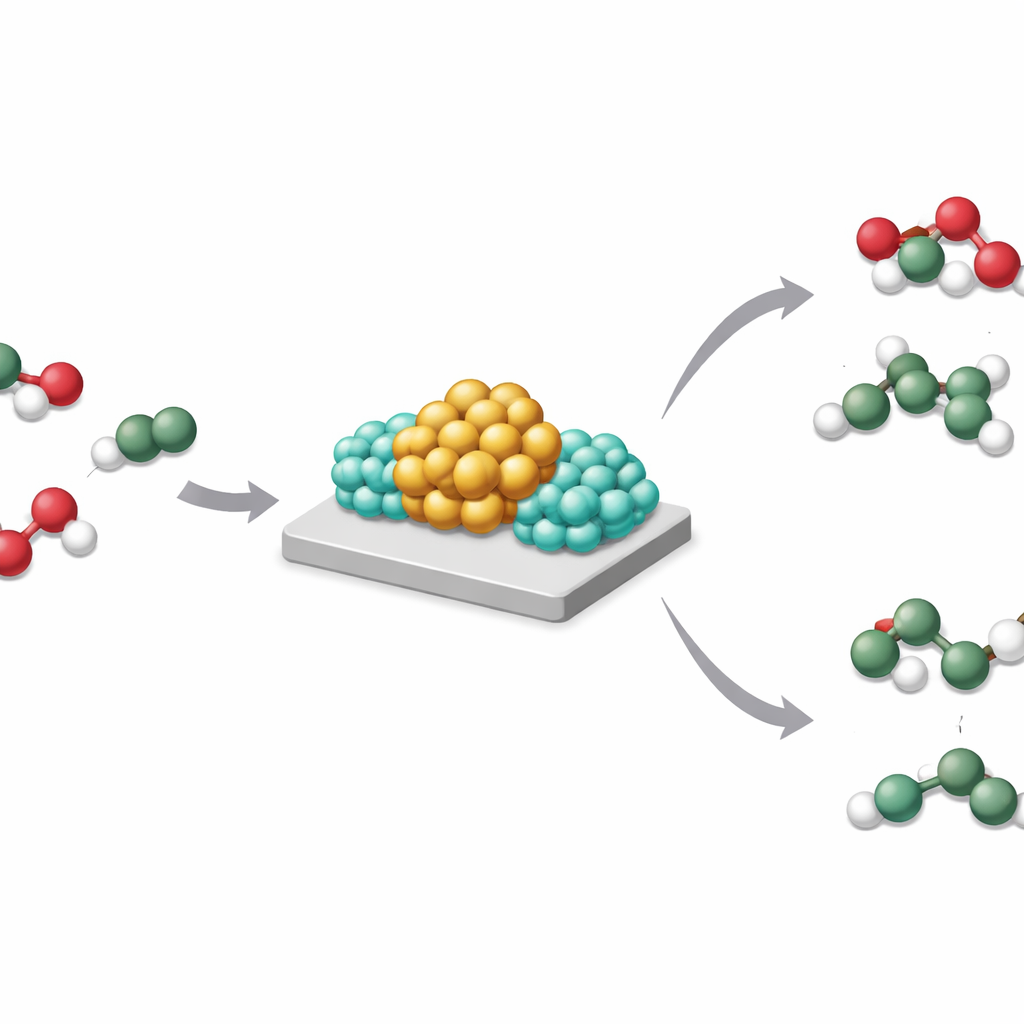
Bliższe spojrzenie na wzmacniane katalizatory metaliczne
Katalizatory oparte na metalach przejściowych, takich jak rod czy nikiel, osadzone na stałych nośnikach pomagają przełamywać i tworzyć wiązania chemiczne. Przez dziesięciolecia przemysł dodawał metale alkaliczne, aby uczynić te katalizatory bardziej aktywnymi, selektywnymi lub trwalszymi. Standardowe wyjaśnienia koncentrowały się na prostych efektach geometrycznych (zmiana kształtu i rozmiaru cząstek) lub bezpośrednim oddawaniu elektronów przez metal alkaliczny do metalu aktywnego. Jednak w rzeczywistych warunkach pracy te promotory występują głównie jako tlenki, a nie jako nagie atomy metalu, co sprawia, że proste przekazywanie elektronów jest niepełnym opisem.
Odkrycie silnego partnerstwa na powierzchni
Autorzy badali układ modelowy: nanocząstki rodu na dwutlenku tytanu, z dodatkiem sodu i bez niego. Wykorzystując zaawansowaną mikroskopię elektronową, spektroskopię rentgenowską i symulacje komputerowe, stwierdzili, że sód występuje jako tlenek, Na2O, bezpośrednio na krawędzi styku cząstek rodu z nośnikiem. Pod wpływem wodoru takie rozmieszczenie tworzy to, co nazwali Silną Interakcją Metal–Zasada (SMBI). W tych szczególnych punktach styku cząsteczki wodoru rozpadają się niejednakowo: bardziej zasadowy Na2O przyciąga część podobną do protonu, podczas gdy rod utrzymuje partnera bogatego w elektrony. Ten „heterolityczny” rozpad powoduje, że powierzchnia rodu staje się wyjątkowo bogata w elektrony i zapobiega „przelewaniu się” wodoru na nośnik z dwutlenku tytanu.
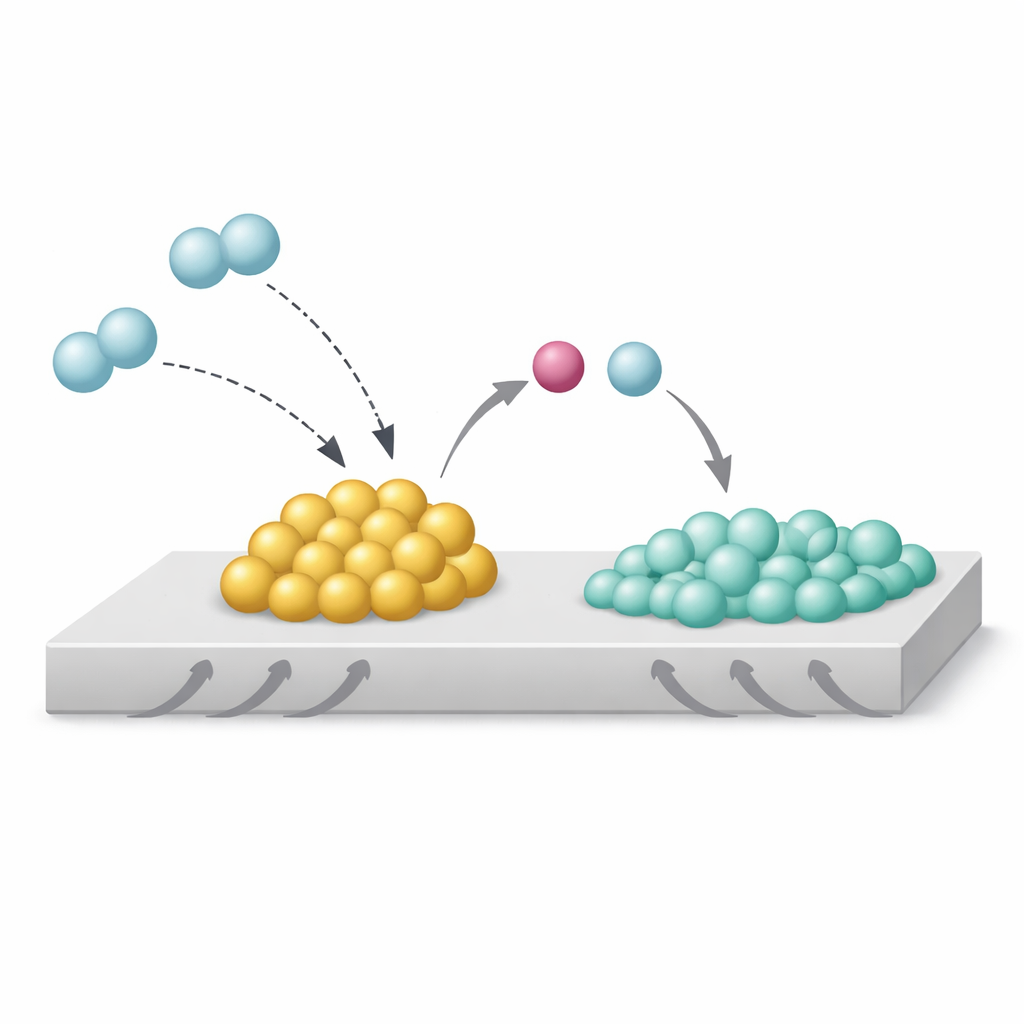
Jak ten ukryty efekt kieruje przebiegiem reakcji
To subtelne przemieszczenie wodoru i elektronów ma daleko idące konsekwencje. W hydrogenacji dwutlenku węgla czysty rod na dwutlenku tytanu sprzyja pełnej hydrogenacji aż do metanu. Po dodaniu sodu ten sam katalizator zamiast tego produkuje głównie tlenek węgla, wartościowy surowiec, przy znacznie mniejszej ilości metanu. Podobne zachowanie obserwuje się przy zastosowaniu litu lub potasu, albo gdy rod zastąpiono niklem. Autorzy pokazują, że kiedy wodór może swobodnie przelewać się na nośnik, dominuje głęboka hydrogenacja; kiedy SMBI utrzymuje wodór skoncentrowany na granicy metal–zasada i z dala od nośnika, przeważają łagodniejsze produkty.
Różne wiązania podwójne — różne rezultaty
Zespół następnie sprawdził, jak SMBI wpływa na typowe reakcje hydrogenacji organicznej obejmujące wiązania podwójne C–C, C–O i N–O. Dla wiązania podwójnego C–C w winylowym acetacie promocja sodem przyspiesza reakcję, prawdopodobnie dlatego, że elektronowo wzbogacony rod osłabia to wiązanie, podczas gdy słabiej związany wodór dodaje się do niego wydajnie. W przeciwieństwie do tego, dla związków takich jak acetofenon i nitrobenzen, których reaktywne grupy preferują osadzenie na tlenkowym nośniku, to samo dodanie sodu spowalnia reakcję. Tutaj zahamowane przelewanie wodoru oznacza, że nośnik nie otrzymuje wystarczającej ilości wodoru do przeprowadzenia tych przekształceń, co pokazuje, że nie wszystkie wiązania podwójne korzystają jednakowo z tego samego efektu promocyjnego.
Projektowanie katalizatorów z zamierzoną kontrolą
Łącząc eksperymenty i teorię, autorzy twierdzą, że SMBI dostarcza zunifikowanego sposobu rozumienia, jak promotory metali alkalicznych przeobrażają powierzchnie katalityczne. Zamiast działać jako proste dawcy elektronów, tlenki alkaliczne pełnią rolę silnych pułapek protonów, wymuszając spolaryzowany rozpad wodoru i ograniczając reaktywny wodór w pobliżu interfejsu metal–zasada. To spostrzeżenie wyjaśnia zagadkowe trendy obserwowane w wielu reakcjach hydrogenacji i różnych metalach oraz wskazuje praktyczną zasadę projektowania: poprzez dostrojenie ilości i rozmieszczenia tlenków alkalicznych wokół cząstek metalu chemicy mogą celowo kierować reakcjami ku określonym produktom, jednocześnie optymalizując aktywność i stabilność dla czyściejszych procesów chemicznych.
Cytowanie: Jung, M., Dickieson, M.P., Chen, P. et al. Understanding alkali metal promotion in hydrogenation catalysis through Strong Metal–Base Interaction. Nat Commun 17, 2465 (2026). https://doi.org/10.1038/s41467-026-68952-w
Słowa kluczowe: kataliza hydrogenacji, promotory metali alkalicznych, konwersja CO2, katalizatory heterogeniczne, interfejsy metal–tlenek