Clear Sky Science · pl
RiboBright ujawnia różnice w organizacji i ruchu rybosomów zależne od typu komórki
Widząc, jak zapalają się fabryki białek komórki
Każda z naszych komórek co sekundę wytwarza tysiące nowych białek przy pomocy maleńkich maszyn zwanych rybosomami. Dotychczas obserwowanie, gdzie te maszyny się znajdują i jak się poruszają wewnątrz żywych komórek, było zaskakująco trudne. W tym badaniu wprowadzono RiboBright, małą cząsteczkę fluorescencyjną, która przyczepia się do rybosomów i je rozświetla, pozwalając naukowcom śledzić te fabryki białek komórka po komórce. Praca ujawnia, że rybosomy są organizowane i używane bardzo różnie w zależności od typu komórki, zwłaszcza gdy komórki macierzyste wybierają swoją przyszłą drogę rozwojową.
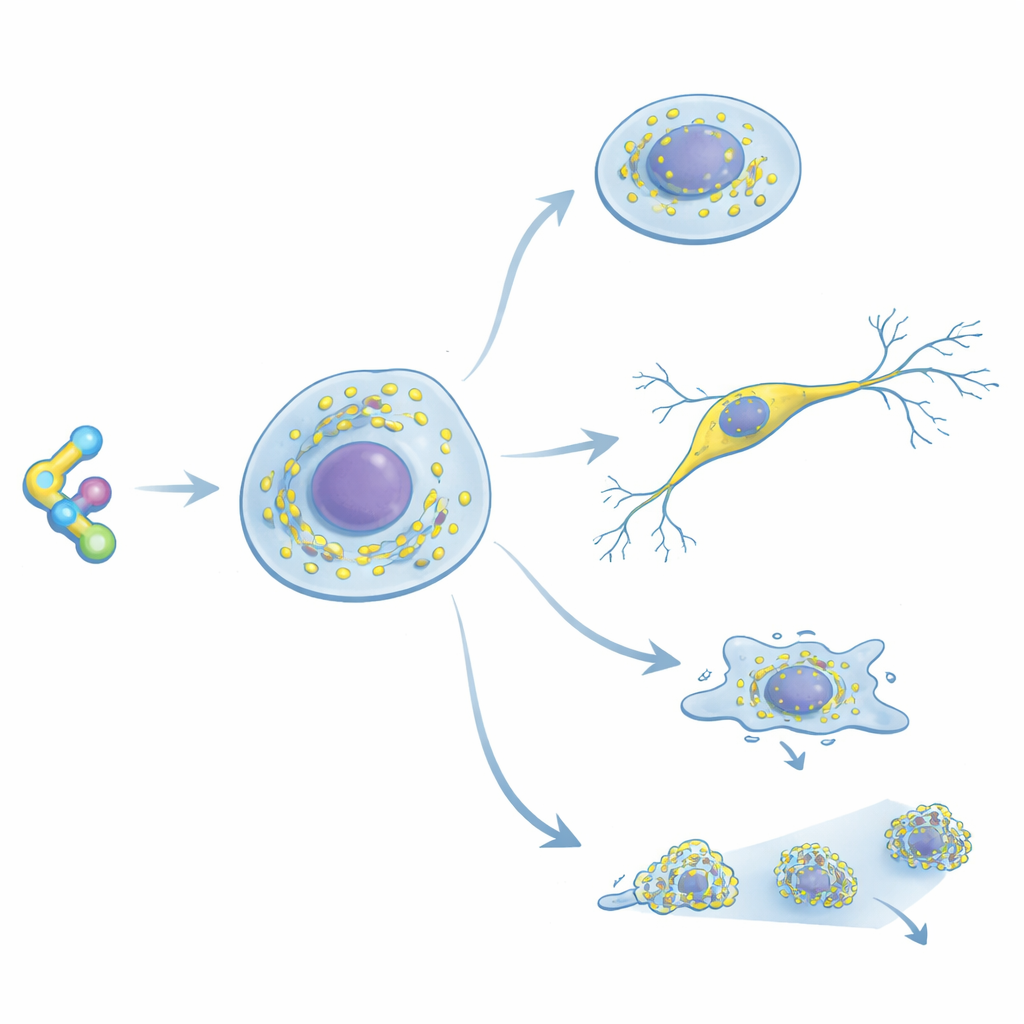
Nowy sposób na uwydatnienie rybosomów
Naukowcy stworzyli RiboBright modyfikując cykloheksymid, klasyczny lek znany z silnego i selektywnego wiązania z rybosomami zwierząt i ludzi. Do cząsteczki przymocowali specjalny barwnik będący „molekularnym rotorem” w pozycji na leku, która nie osłabia jego przyczepności do rybosomu. Barwnik słabo świeci, gdy swobodnie się obraca w roztworze, ale staje się jasny, gdy jego ruch jest ograniczony — na przykład gdy sonda wsuwa się do rybosomu. Testy w probówkach wykazały, że zmodyfikowane cząsteczki nadal hamują produkcję białek przy dawkach zbliżonych do oryginalnego leku, co potwierdza dobre wiązanie. W żywych komórkach jedna z wersji dała szczególnie ostre, jasne plamki, wskazując na właściwą równowagę między silnym wiązaniem z rybosomem a wydajnym emitowaniem światła; zoptymalizowaną sondę nazwano RiboBright.
Dowody, że sonda celuje w prawdziwe rybosomy
Aby upewnić się, że RiboBright rzeczywiście oznacza rybosomy, zespół zastosował kilka komplementarnych podejść. Gdy komórki były wstępnie traktowane albo samym cykloheksymidem, albo innym, niezwiązanym związkiem blokującym rybosomy, sygnał RiboBright niemal zanikał, co sugeruje, że wszystkie trzy konkurują o to samo miejsce wiązania. Chemiczne badanie RNA rybosomalnego wykazało dodatkowo, że RiboBright chroni ten sam nukleotyd, który chroni cykloheksymid, zgodnie z identycznym miejscem dokowania. Mikroskopia o wysokiej rozdzielczości pokazała silne nakładanie się sygnału RiboBright z markerami dużej podjednostki rybosomu oraz ze strukturami takimi jak siateczka śródplazmatyczna i mitochondria — miejscami, gdzie znajduje się wiele rybosomów. Jednocześnie niektóre jasne plamki dryfowały swobodnie w cytoplazmie, prawdopodobnie reprezentując ruchome rybosomy nieprzyczepione do błon.
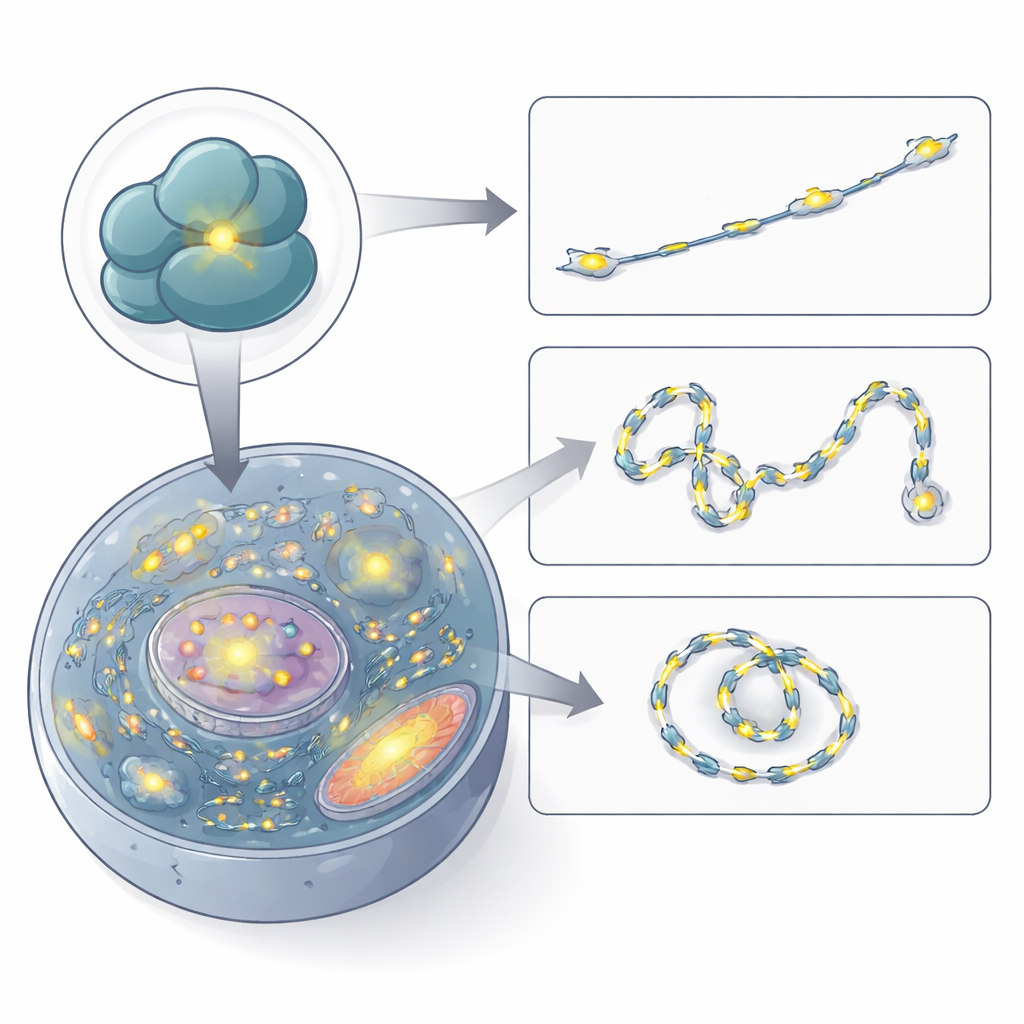
Obserwowanie ruchu rybosomów w żywych komórkach
Z ufnością co do specyfiki autorzy użyli RiboBright do filmowania rybosomów w akcji. Rejestrując obrazy co kilkaset milisekund, śledzili trajektorie pojedynczych fluorescencyjnych punkcików w komórce. Wiele plamek poruszało się minimalnie lub pozostawało ograniczonych do małych obszarów, co sugeruje, że rybosomy tłumaczą białka w miejscu, na unieruchomionych mRNA lub na siateczce śródplazmatycznej. Inne wędrowały w sposób losowy, dyfuzyjny, a mniejsza frakcja wykazywała wyraźny kierunkowy ruch, sugerując aktywny transport po szlakach komórkowych. Zmierzone prędkości odpowiadają wcześniejszym oszacowaniom dla mRNA i klastrów rybosomów, potwierdzając, że RiboBright potrafi uchwycić realistyczne dynamiczne zachowanie rybosomów w czasie rzeczywistym.
Różne typy komórek, różne strategie rybosomów
RiboBright ujawnił również, jak bardzo zawartość i organizacja rybosomów zależą od tożsamości komórki. W dziesięciu liniach komórkowych ludzkich i mysich, w tym komórkach macierzystych, komórkach nowotworowych i niekancerogennych, wzór i jasność plamek rybosomowych różniły się dramatycznie. Niektóre komórki zawierały duże, jasne klastry, które mogą odpowiadać obszarom intensywnej produkcji białek, podczas gdy inne miały głównie małe, rozproszone punkciki. Zaskakująco, sama liczba rybosomów w komórce nie przewidywała wiarygodnie ilości wytwarzanych białek: w większości typów komórek produkcja białek i zawartość rybosomów wykazywały niewielką korelację. Komórki macierzyste embrionalne wyróżniały się niską produktywnością na rybosom i stosunkowo równomiernym tłumaczeniem między poszczególnymi komórkami, co sugeruje, że utrzymują duże rezerwy niewykorzystanych rybosomów, jednocześnie ograniczając szumy w produkcji białek.
Rybosomy podczas wczesnych decyzji o losie komórki
Zespół następnie śledził mysie komórki macierzyste embrionalne, gdy zaczynały różnicować się w dwa wczesne powiązania: gałąź przypominającą ektodermę oraz gałąź przypominającą pozazarodkowy endoderma (XEN). Używając RiboBright wraz z markerami powierzchniowymi komórek, odkryli, że obie wyłaniające się linie uzyskały nieco większą całkowitą zawartość rybosomów niż komórki niezróżnicowane, ale organizowały te rybosomy w różny sposób. Komórki podobne do XEN, które rozwijają długie wypustki, wykazywały wolniejszy i bardziej ograniczony ruch rybosomów, zgodny z lokalizowaną syntezą białek w wyspecjalizowanych regionach. W przeciwieństwie do tego komórki przypominające ektodermę miały bardziej ruchome rybosomy i po około dwóch dniach rozwinęły uderzające „huby translacyjne”, gdzie zarówno sygnał rybosomów, jak i nowa synteza białek osiągały szczyt. W ciągu pierwszych 72 godzin różnicowania ogólna produkcja białek i poziomy rybosomów nieznacznie się obniżyły, ale pozostałe rybosomy stały się nieco wydajniejsze, szczególnie w komórkach różnicujących się.
Co to oznacza dla zrozumienia komórek
Razem te wyniki malują bogatszy obraz rybosomów jako dynamicznych, zależnych od kontekstu maszyn, a nie jednorodnych sił roboczych. RiboBright daje badaczom praktyczne narzędzie do wizualizacji i zliczania rybosomów w wielu typach komórek, zarówno w próbkach utrwalonych, jak i żywych, oraz do powiązania położenia i ruchu rybosomów z tym, ile białka komórka rzeczywiście produkuje. Dla laików kluczowy wniosek jest taki, że komórki regulują nie tylko ile fabryk białek budują, ale też gdzie je umieszczają i jak intensywnie je uruchamiają — w sposób zależny od typu komórki i stanu rozwojowego. Ta nowa sonda fluorescencyjna uwidacznia tę ukrytą logistykę, otwierając drogę do badania, jak zachowanie rybosomów przyczynia się do rozwoju, chorób i reakcji na terapię.
Cytowanie: Poulladofonou, G., Grandi, C., Hu, X. et al. RiboBright reveals cell-type-specific differences in ribosome organization and movement. Nat Commun 17, 2734 (2026). https://doi.org/10.1038/s41467-026-68947-7
Słowa kluczowe: rybosomy, sondy fluorescencyjne, obrazowanie pojedynczych komórek, różnicowanie komórek macierzystych, synteza białek