Clear Sky Science · pl
Allosteryczny inhibitor proteazy NS2B-NS3 wirusa Zika o skuteczności po podaniu doustnym w modelach mysich
Nowy sposób na przechytrzenie groźnego wirusa
Wirus Zika trafił na pierwsze strony gazet dekadę temu, gdy zakażenia u ciężarnych kobiet powiązano z urodzeniami dzieci z nietypowo małymi głowami i uszkodzeniami mózgu. Do dziś nie ma zatwierdzonego leku do leczenia ani zapobiegania Zika. W tym badaniu opisano obiecujący związek przypominający tabletkę, który wyłącza kluczowy enzym wirusowy w nieoczekiwany sposób i chroni myszy przed ciężkim zakażeniem Zika, wskazując drogę do przyszłego leku, który mógłby chronić osoby wrażliwe, szczególnie podczas epidemii.
Dlaczego Zika wciąż ma znaczenie
Wirus Zika przenoszony jest głównie przez komary Aedes i należy do tej samej rodziny co wirusy dengi i Zachodniego Nilu. Większość zakażonych odczuwa niewielkie objawy lub w ogóle nie choruje, jednak około jedna na pięć osób rozwija problemy od gorączki i wysypki po poważne powikłania, takie jak uszkodzenia oczu, niewydolność narządów i zaburzenia układu nerwowego. Największe zagrożenie dotyczy płodów: zakażenie w trakcie ciąży może prowadzić do mikrocefalii i trwałego kalectwa. Ponieważ nie ma zatwierdzonej szczepionki ani terapii przeciwwirusowej, lekarze mogą jedynie zapewniać leczenie wspomagające. Naukowcy traktują więc Zikę jako priorytet w przygotowaniach na pandemie i poszukują leków, które mogłyby zarówno chronić populacje zagrożone, jak i powstrzymywać nowe ogniska.
Polowanie na ukryte słabe punkty
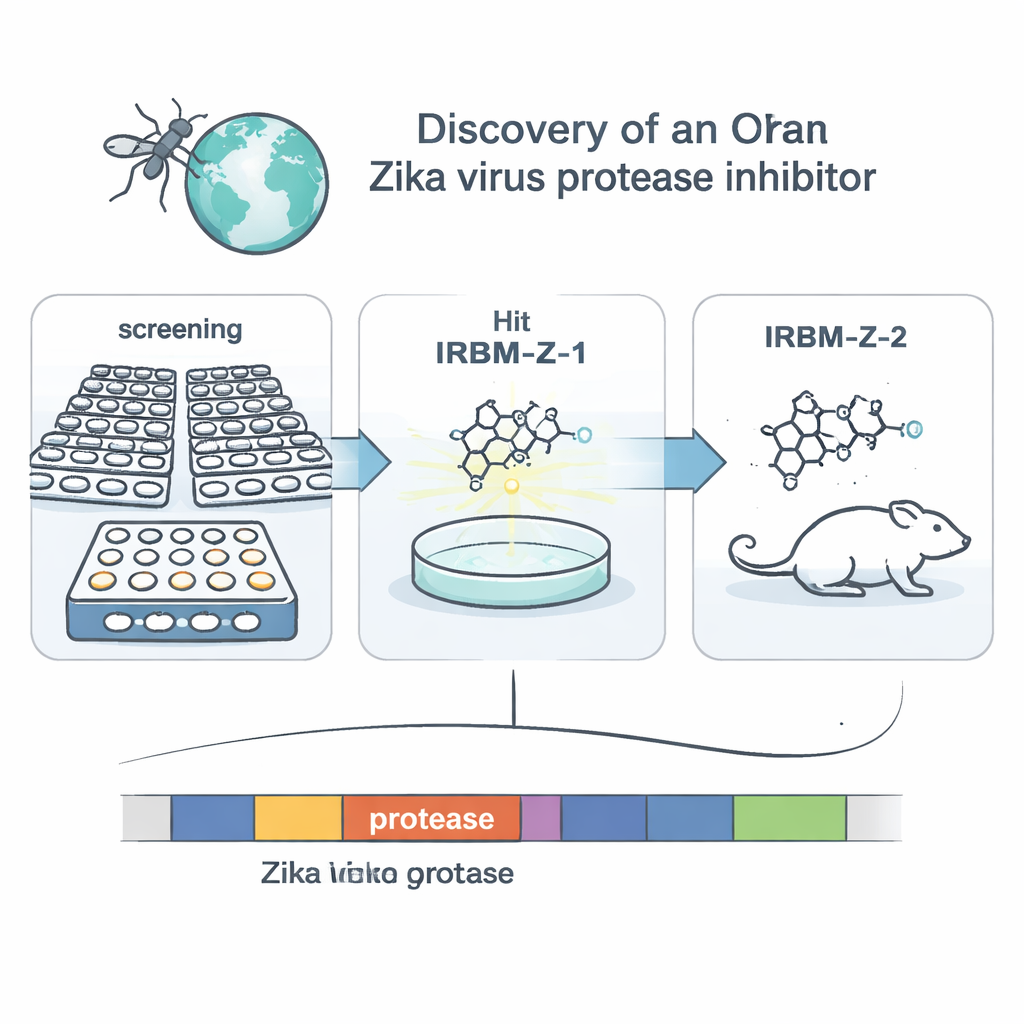
Badacze skupili się na enzymie wirusowym zwanym proteazą NS2B–NS3. Te „nożyczki” molekularne przecinają duży początkowy białkowy polipeptyd wirusa na fragmenty potrzebne do skompletowania nowych wirionów, co czyni je atrakcyjnym celem terapeutycznym. Zamiast projektować lek skierowany na oczywiste miejsce cięcia, zespół zastosował system przesiewowy oparty na komórkach, który naśladuje replikację Zika w komórkach nerkowych małp. Zbudowali zmodyfikowany genom Zika, tzw. replicon, pozbawiony genów strukturalnych, ale zawierający reporter lucyferazowy, tak że emisja światła odzwierciedla kopiowanie wirusa. Przesiewając ponad 120 000 małych cząsteczek z krajowej biblioteki chemicznej, wybrali te, które silnie zmniejszały sygnał świetlny bez uszkadzania komórek, a następnie wyhodowali replicony wirusa, które stały się oporne na każde z trafień. To genetyczne dochodzenie wskazało proteazę jako kluczowy cel dla jednej rodziny związków, związaną z początkową cząsteczką o nazwie IRBM-Z-1.
Zamrażanie enzymu w niewłaściwym kształcie
Testy biochemiczne wykazały, że IRBM-Z-1 nie konkurował z typowym substratem w miejscu cięcia. Zamiast tego działał jako inhibitor niekonkurencyjny, czyli allosteryczny — wiązał się w oddzielnej kieszeni i uniemożliwiał enzymowi przyjęcie aktywnej konformacji. Krystalografia rentgenowska o wysokiej rozdzielczości ujawniła, że związek wkłada się w wcześniej nieznaną kieszeń daleko od centrum katalitycznego. Tam jego nietypowe jądro „N-acylsydnonowy iminowy” tworzy sieć wiązań wodorowych i interakcji układania, które wypychają kluczowy region proteazy do otwartej, nieaktywnej konformacji. Pojedyncza zmiana aminokwasu w tym regionie, w pozycji 156, czyni wirusa opornym, co podkreśla, jak precyzyjnie związek wykorzystuje to ukryte miejsce. Ta kieszeń różni się też od allosterycznych miejsc opisanych u pokrewnych flawiwirusów, oferując prawdziwie nową pozycję startową dla projektowania leków.
Od trafienia do ochronnego leku u myszy
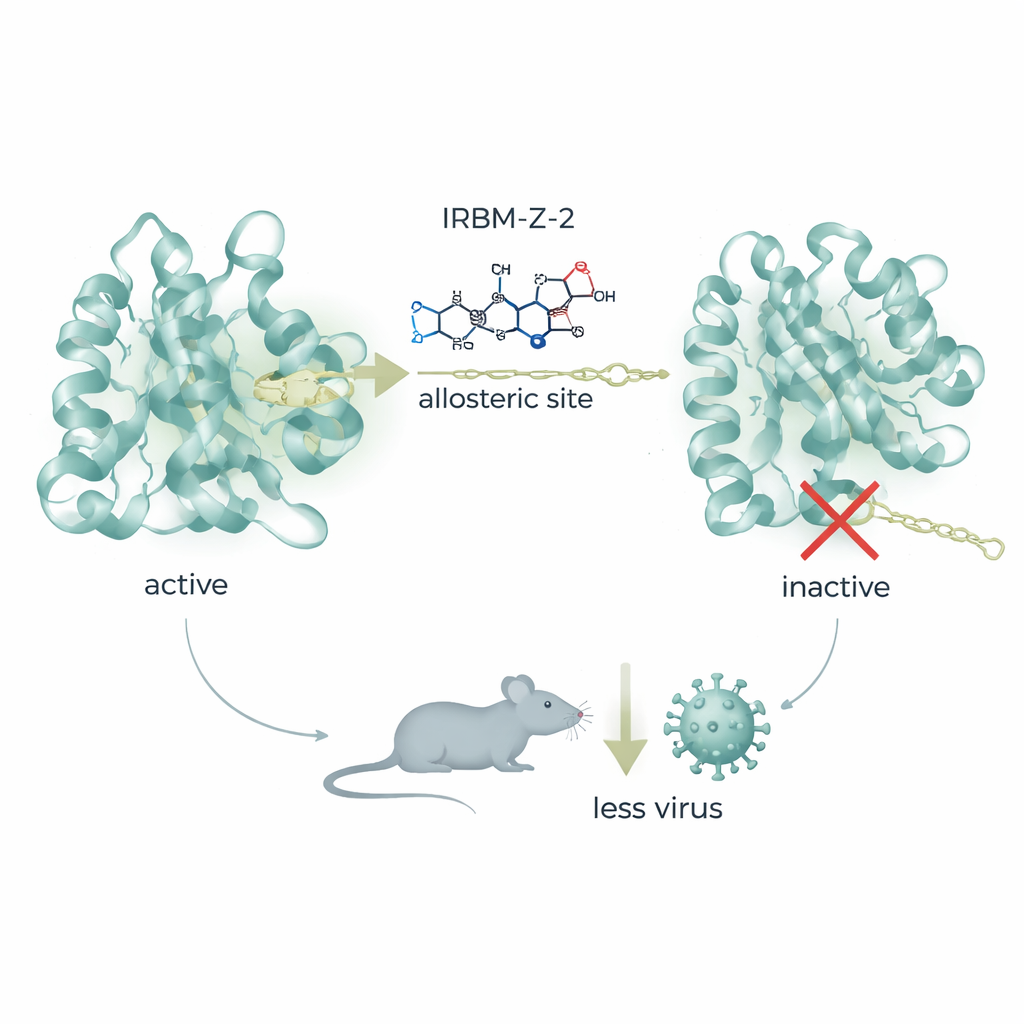
Kierując się wglądem strukturalnym, zespół udoskonalił IRBM-Z-1 do silniejszej cząsteczki nazwanej IRBM-Z-2. Ulepszony związek blokuje proteazę Zika w stężeniach nanomolowych, silnie hamuje replikację wirusa w kilku typach komórek i wykazuje aktywność przeciwko pokrewnym proteazom dengi i Zachodniego Nilu, oszczędzając przy tym enzymy ludzkie. W badaniach na zwierzętach IRBM-Z-2 wykazał korzystne właściwości „lekopodobne”: był stabilny w organizmie, dobrze wchłaniał się po podaniu doustnym i utrzymywał stężenia we krwi znacznie przewyższające te potrzebne do zahamowania wirusa, bez wyraźnych oznak toksyczności. U wysoce podatnych myszy AG129 zakażonych Zika codzienne leczenie — zarówno przez wstrzyknięcie, jak i doustnie — dramatycznie obniżyło ilość wirusowego RNA w krwi, zapobiegło utracie masy i objawom choroby oraz pozwoliło wszystkim leczonym zwierzętom przeżyć, podczas gdy nieleczone kontrolne myszy zmarły w wyniku zakażenia.
Co to może oznaczać dla przyszłych ognisk
W całości te ustalenia przedstawiają nową klasę leków przeciwwirusowych przeciw Zika, które działają przez „zamrożenie” krytycznego enzymu wirusowego w nieaktywnej pozycji, zamiast bezpośrednio blokować jego miejsce aktywne. Ponieważ IRBM-Z-2 można podawać doustnie, wykazuje silną ochronę w surowych modelach mysich i jak dotąd ma dobre właściwości bezpieczeństwa, wyróżnia się jako obiecujący kandydat do dalszego rozwoju jako lek zapobiegawczy — potencjalnie do ochrony kobiet w ciąży, pracowników służby zdrowia i podróżnych w przypadku ponownego pojawienia się Zika. Szerzej rzecz biorąc, nowo odkryta kieszeń allosteryczna może zainspirować podobne leki przeciw pokrewnym wirusom, otwierając nowy front w walce z chorobami przenoszonymi przez komary.
Cytowanie: Ontoria, J.M., Torrente, E., Missineo, A. et al. An allosteric inhibitor of the Zika virus NS2B-NS3 protease with oral efficacy in mouse models. Nat Commun 17, 1439 (2026). https://doi.org/10.1038/s41467-026-68943-x
Słowa kluczowe: wirus Zika, lek przeciwwirusowy, inhibitor proteazy, modulacja allosteryczna, choroba przenoszona przez komary