Clear Sky Science · pl
FCHo2, a nie talin, umożliwia aktywację integryny ɑvβ5 od strony wewnętrznej w zakrzywionych adhezjach
Jak komórki wyczuwają kształt otoczenia
Nasze ciała zbudowane są z komórek, które nieustannie chwytają otaczające je środowisko, pociągając i popychając, by się poruszać, dzielić lub utrzymać pozycję. W pracy tej wykazano, że komórki nie tylko odczytują sztywność otoczenia — analizują też jego kształt. Odkrycie specjalnego systemu adhezyjnego, który włącza się wyłącznie tam, gdzie błona komórkowa jest silnie zakrzywiona, pokazuje, że komórki stosują różne „uchwyty” wewnętrzne w zależności od tego, czy otoczenie jest płaskie, czy włókniste, co ma istotne znaczenie dla formowania tkanek i rozprzestrzeniania się nowotworów.
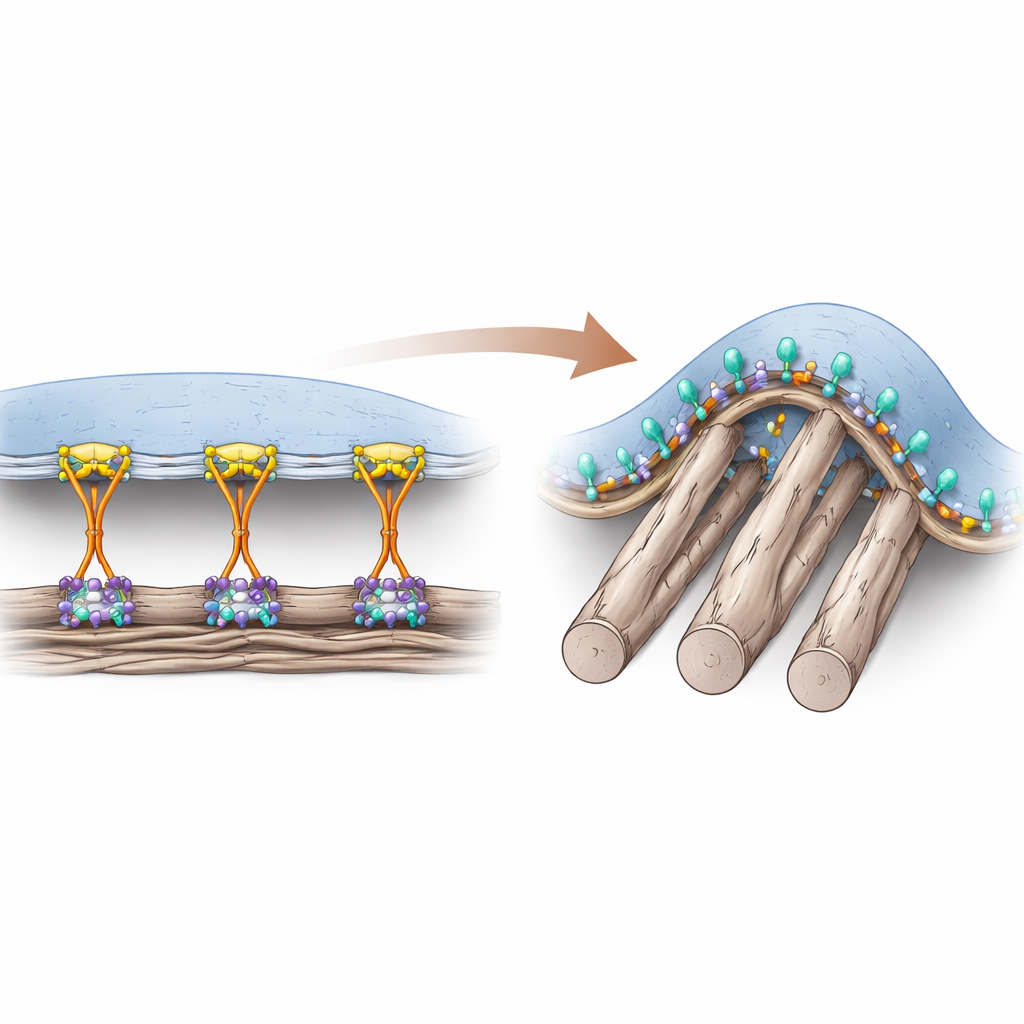
Dwa sposoby, w jaki komórki się trzymają
Komórki przyczepiają się do białkowej macierzy otaczającej je przestrzeń za pomocą receptorów powierzchniowych zwanych integrynami. Przez lata badacze uważali, że białko pomocnicze o nazwie talin jest absolutnie niezbędne do „włączenia” integryn od strony wewnętrznej komórki, co pozwala na silne wiązanie w klasycznych miejscach kotwiczenia znanych jako ogniskowe adhezje. Te adhezje powstają głównie na płaskich, sztywnych powierzchniach i przenoszą duże siły pociągające przez szkielet komórkowy. Jednak w tkankach żywych wiele otaczających włókien jest miękkich i cylindrycznych, tworząc zakrzywione punkty kontaktu, które nie sprzyjają strukturom przenoszącym duże siły. Autorzy wcześniej opisali inny typ struktur adhezyjnych, zwany zakrzywioną adhezją, która pojawia się tam, gdzie błona owija się wokół cienkich włókien i opiera się na specyficznej integrynie αvβ5.
Zakrzewione uchwyty korzystają z innego pomocnika
W nowym badaniu zespół wykazuje, że talin, choć obecny, nie jest kluczowym aktywatorem integryny αvβ5 w zakrzywionych adhezjach. Zamiast niego tę rolę przejmuje białko wyczuwające krzywiznę o nazwie FCHo2. Korzystając z precyzyjnie zaprojektowanych nano-prętów i słupków do kontrolowanego wyginania błon komórkowych, zaobserwowano, że αvβ5 silnie gromadzi się w obszarach zakrzywionych, ale tylko wtedy, gdy FCHo2 może związać bardzo krótki motyw — sekwencję HDRRE — tuż po wewnętrznej stronie ogonka β5. Gdy ten motyw jest zaburzony, integryna nadal działa w ogniskowych adhezjach, lecz nie może tworzyć zakrzywionych adhezji. Redukcja ekspresji FCHo2 pozostawia klasyczne ogniskowe adhezje w dużej mierze nienaruszone, zaś eliminuje zakrzywione adhezje; natomiast usunięcie taliny znacząco osłabia ogniskowe adhezje, pozostawiając zakrzywione adhezje w dużej mierze nietknięte.
Pojedynczy aminokwas jako selektor kształtu
Jedną z zagadek było to, dlaczego blisko spokrewniona integryna αvβ3 nie tworzy zakrzywionych adhezji, mimo że jej wewnętrzny ogonek jest bardzo podobny do ogonka β5. Poprzez wymianę domen między tymi dwiema integrynami oraz wprowadzanie mutacji punktowych autorzy zidentyfikowali pojedyncze kluczowe miejsce w sąsiedztwie miejsca wiążącego talinę: większość integryn β ma tryptofan (W), natomiast β5 wyjątkowo posiada tyrozynę (Y766). Gdy tyrozyna w β5 została zastąpiona tryptofanem, integryna utraciła zdolność uczestniczenia w zakrzywionych adhezjach i zaczęła zachowywać się bardziej jak β3, preferując jedynie ogniskowe adhezje. Zmiana odwrotna — wprowadzenie tyrozyny do chimery o charakterze β3 — przywróciła wrażliwość na krzywiznę. Dalsze eksperymenty z wariantami imitującymi stany ufosforylowane lub nieufosforylowane tej tyrozyny sugerują, że modyfikacja chemiczna tego miejsca może przesunąć równowagę integryny w stronę płaskich, silnie obciążonych ogniskowych adhezji lub zakrzywionych, niskoobciążeniowych adhezji.
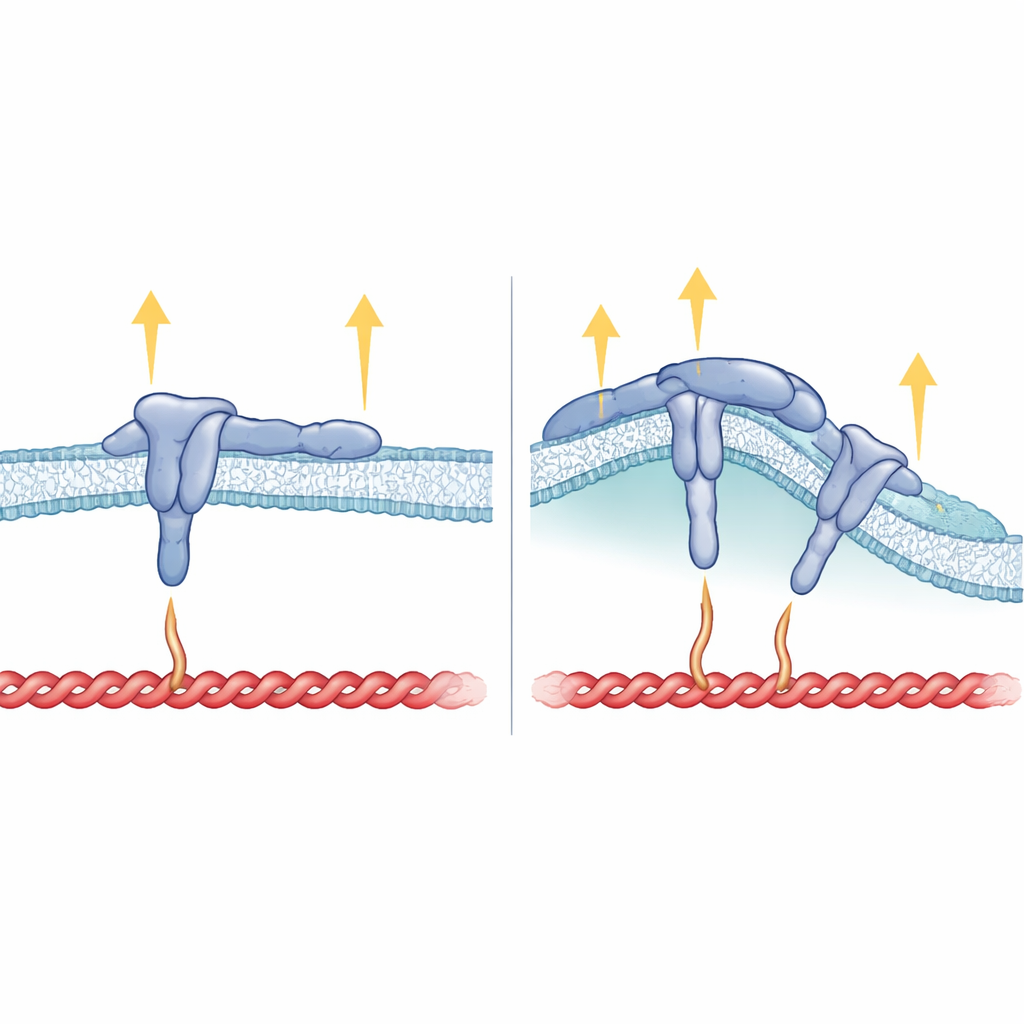
Jak kształt błony, struktura integryny i siła do siebie pasują
Poza wewnętrznym ogonkiem istotny okazał się również fragment β5 przebiegający przez błonę. Kiedy badacze zastąpili segment transmembranowy β5 tym z β3, powstała integryna nadal potrafiła tworzyć ogniskowe adhezje, lecz przestała preferować zakrzywione miejsca i nie współpracowała z FCHo2. Sugeruje to, że sposób osadzenia integryny w błonie pomaga zorientować motyw HDRRE tak, by FCHo2 mogło się przyczepić w obszarach zakrzywionych i stabilizować ligandozależną, aktywną αvβ5. W zakrzywionych adhezjach talin wydaje się mieć kontakt tylko z dalszą częścią ogonka integryny i nie jest pod dużym napięciem, co wyjaśnia, dlaczego inne elementy pragnące siły, takie jak winkulina, tensyna i kindlina, są tam w dużej mierze nieobecne. W przeciwieństwie do tego, w ogniskowych adhezjach talin chwyta zarówno bliższe, jak i dalsze miejsca na ogonku i błonie, wspierając silne siły pociągające, jednocześnie blokując FCHo2 przed dostępem do tego samego rejonu.
Co to znaczy dla zachowania komórek
Dla laika przesłanie tej pracy jest takie, że komórki dysponują dwoma odrębnymi „trybami chwytu” do przyczepiania się do otoczenia. Na płaskich, sztywnych obszarach używają talinowo-zależnych ogniskowych adhezji zbudowanych do silnego ciągnięcia. Na miękkich, włóknistych i zakrzywionych strukturach przełączają się na FCHo2-zależne zakrzywione adhezje, które stabilizują integrynę αvβ5 przy znacznie niższym obciążeniu. Drobna zmiana w sekwencji integryny — i to, czy to miejsce jest chemicznie zmodyfikowane — pomaga zdecydować, który tryb zostanie użyty. Ten podwójny system pozwala komórkom interpretować zarówno sztywność, jak i kształt w środowiskach trójwymiarowych, wpływając na ich migrację, organizację tkanek i potencjalnie na zdolność do inwazji w przebiegu choroby.
Cytowanie: Lu, CH., Lee, C.E., Zhang, W. et al. FCHo2, not talin, enables inside-out activation of integrin ɑvβ5 in curved adhesions. Nat Commun 17, 2419 (2026). https://doi.org/10.1038/s41467-026-68942-y
Słowa kluczowe: integryny, adhezja komórkowa, krzywizna błony, FCHo2, cytoszkielet