Clear Sky Science · pl
Postępy i wyzwania w przechodzeniu od hitów do kandydatów w odkrywaniu leków metodą opartą na fragmentach
Przekształcanie małych chemicznych elementów w przyszłe leki
Współczesne leki często odkrywane są poprzez przeszukiwanie ogromnych kolekcji cząsteczek — proces powolny, kosztowny i coraz mniej efektywny. Ten artykuł opisuje nowsze podejście zwane odkrywaniem leków opartym na fragmentach, które zaczyna się od bardzo małych fragmentów chemicznych i krok po kroku buduje z nich obiecujących kandydatów na leki. Dla czytelników daje to wgląd w to, jak inteligentniejsze projektowanie, automatyzacja i sztuczna inteligencja mogą przyspieszyć znalezienie przyszłych terapii i uczynić je powszechniejszymi.
Dlaczego zaczynać od małych fragmentów zamiast przesiewać wszystko
Tradycyjne odkrywanie leków często polega na testowaniu milionów stosunkowo dużych cząsteczek, aby sprawdzić, które z nich wiążą się z białkiem związanym z chorobą. Metody oparte na fragmentach idą odwrotną drogą: przesiewają znacznie mniejszą kolekcję drobnych cząsteczek, czyli „fragmentów”, z których każdy reprezentuje prosty kształt chemiczny. Te fragmenty wiążą się tylko słabo, ale ponieważ są tak małe i różnorodne, efektywniej eksplorują przestrzeń chemiczną. Wyzwanie polega na tym, że słabe sygnały są trudne do wykrycia i interpretacji, więc badacze potrzebują bardzo czułych eksperymentów i rygorystycznych weryfikacji, by mieć pewność, że fragment rzeczywiście wiąże się, a nie jest artefaktem testu. Techniki strukturalne, takie jak krystalografia rentgenowska i kriomikroskopia elektronowa, mogą pokazać dokładnie, jak fragment osiada w kieszeni białka, podczas gdy metody w roztworze, takie jak NMR, kalorymetria i powierzchniowy rezonans plazmonowy, mierzą, jak mocno i jak szybko się wiąże.
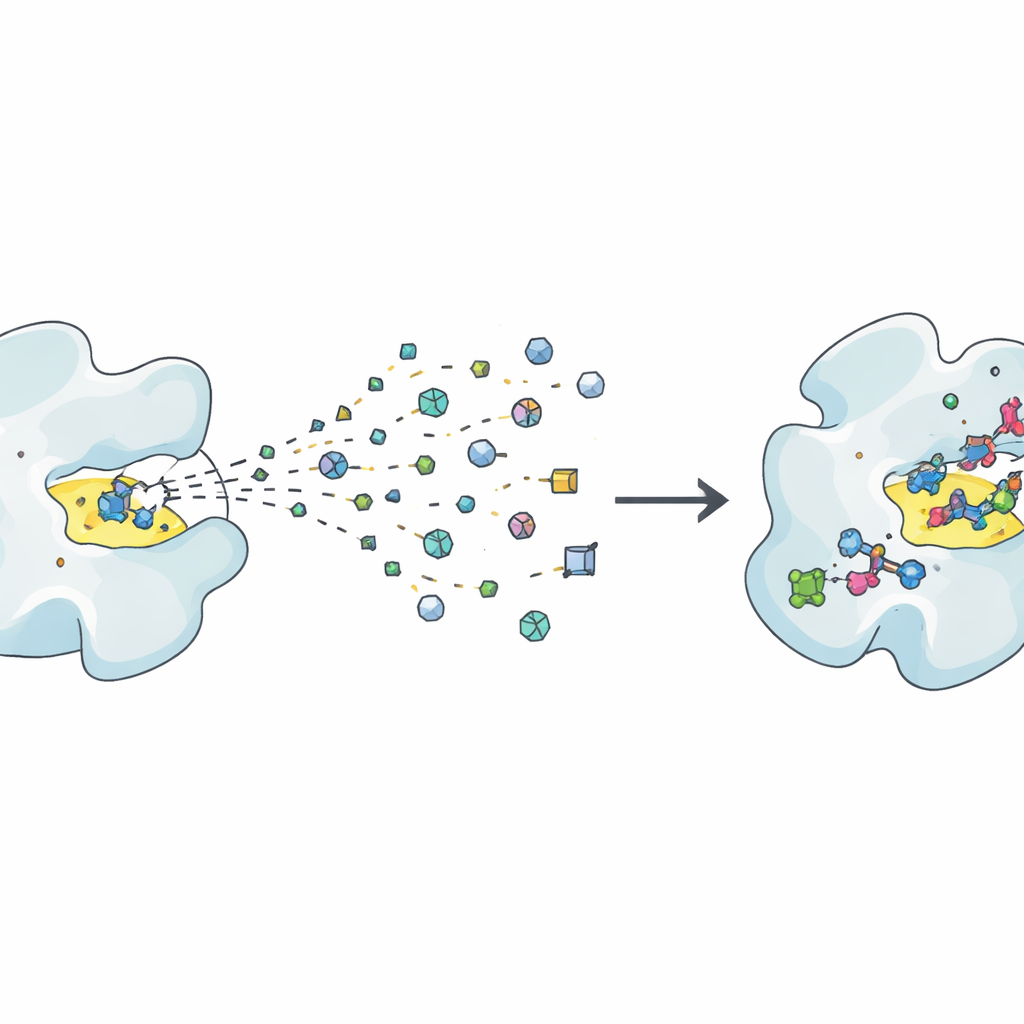
Od pierwszych hitów do obiecujących leadów
Gdy zostaną znalezione użyteczne fragmenty, zaczyna się prawdziwa praca: przekształcenie tych słabych „hitów” w silne, selektywne związki „lead”. Artykuł przedstawia tę drogę jako powtarzające się cykle „Projektuj, Wytwarzaj, Testuj”. W kroku Projektowania chemicy i systemy komputerowe proponują sposoby rozrastania, łączenia lub łączenia fragmentów tak, aby lepiej wypełniały kieszeń białka, unikały niepożądanej reaktywności i zachowywały dobre właściwości fizyczne, np. rozpuszczalność. W kroku Wytwarzania te projekty są syntetyzowane, coraz częściej przy pomocy robotów, chemii wysokoprzepustowej i inteligentnego oprogramowania do planowania dróg syntezy. Krok Testowania mierzy, czy nowe cząsteczki rzeczywiście wiążą się mocniej, działają na zamierzony efekt biologiczny i unikają częstych pułapek, takich jak związki dające fałszywe sygnały we wszystkich testach (PAINS). Ponieważ fragmenty zaczynają od słabego wiązania, często potrzeba kilku rund tego cyklu, zanim związki staną się wystarczająco silne, by przypominać prawdziwych kandydatów na leki.
Nowe narzędzia: automatyzacja, SI i inteligentne biblioteki
Przegląd podkreśla, jak nowa generacja narzędzi przekształca każdy etap tego cyklu. Biblioteki fragmentów projektuje się dziś nie tylko pod kątem różnorodności, ale również jako „sintetycznie towarzyskie”, co oznacza, że można je łatwo rozszerzać w wielu kierunkach przy użyciu odpornych reakcji. Specjalistyczne zestawy fragmentów celują w konkretne rodziny białek, miejsca zawierające metale, a nawet tworzą wiązania kowalencyjne z określonymi aminokwasami, co pomaga zaatakować wcześniej „niedostępne” cele. Po stronie cyfrowej modele sztucznej inteligencji i symulacje oparte na fizyce pomagają sugerować, które zmiany chemiczne mogą poprawić wiązanie lub zmniejszyć toksyczność, oraz mogą przesiewać ultra-wielkie wirtualne przestrzenie miliardów możliwych cząsteczek. Przewidywania te coraz częściej łączy się z pętlami aktywnego uczenia, gdzie niewielka liczba kosztownych symulacji lub eksperymentów trenuje szybsze modele, które z kolei kierują kolejną falą projektów.
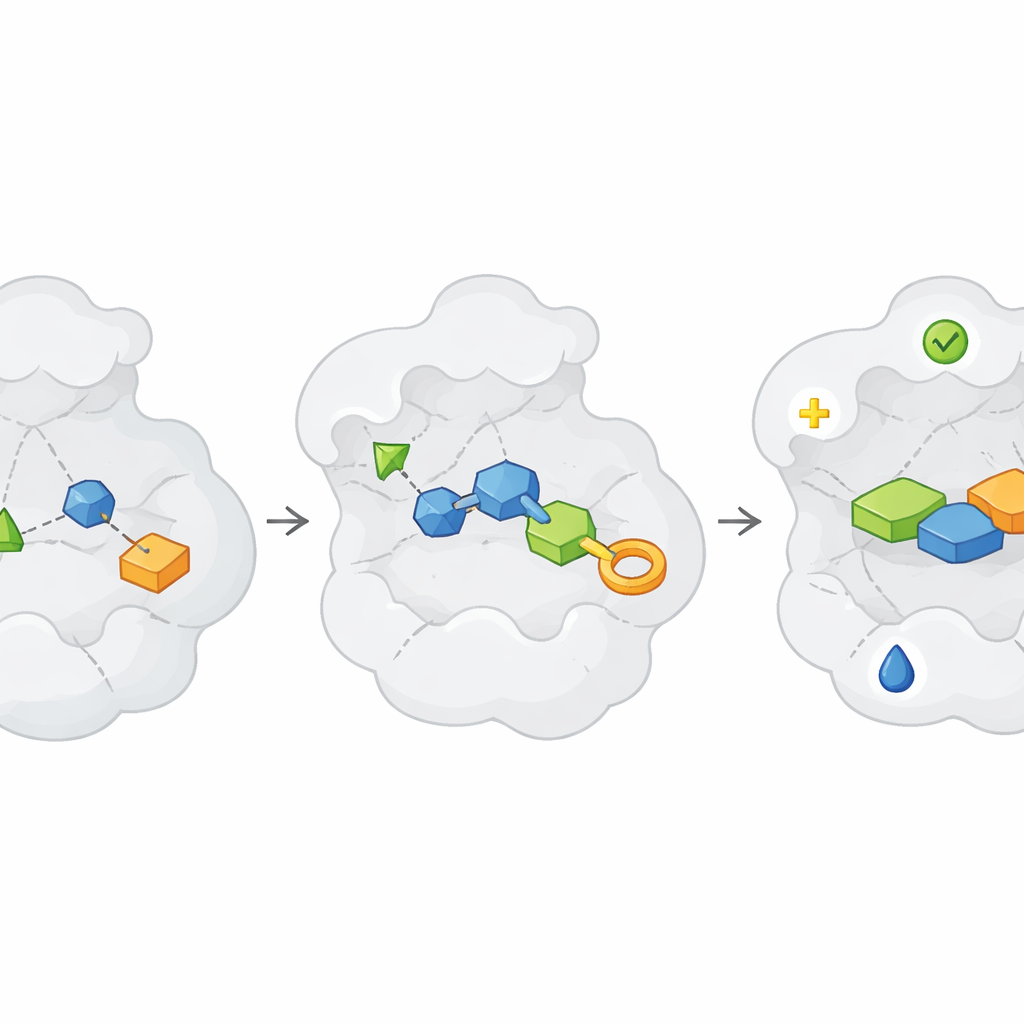
Wytwarzanie i testowanie na dużą skalę bez spowolnienia
Głównym wąskim gardłem w odkrywaniu leków jest po prostu wytworzenie i oczyszczenie wystarczającej liczby związków do przetestowania. Artykuł opisuje, jak roboty do syntezy wysokoprzepustowej, chemia przepływowa i nowe metody ekstrakcji mogą produkować setki lub tysiące pokrewnych cząsteczek wokół fragmentu-hitu. Niektóre podejścia pomijają na początku pełne oczyszczanie: surowe mieszaniny reakcyjne są testowane bezpośrednio w czułych testach, takich jak krystalografia, pomiary kinetyczne czy NMR — podejście zwane czasem „bezpośrednio do biologii”. Kontrole jakości, np. spektrometria mas, są używane równolegle, by śledzić, które mieszaniny rzeczywiście zawierają zamierzony produkt. Chociaż dane mogą być zaszumione, łączenie tych szybkich testów z inteligentną analizą i późniejszą czystą syntezą pozwala badaczom znacznie szybciej mapować związki struktura–aktywność niż przy tradycyjnej chemii jeden po drugim.
Co to oznacza dla przyszłych terapii
Podsumowując, artykuł wnioskuje, że odkrywanie leków oparte na fragmentach dojrzało do roli potężnej i elastycznej strategii znajdowania nowych leków, szczególnie w połączeniu z nowoczesną automatyzacją i SI. Zaczynanie od małych, efektywnych bloków budulcowych pozwala naukowcom bardziej przemyślanie eksplorować przestrzeń chemiczną, ale wymaga starannej walidacji, ponieważ początkowe sygnały są bardzo słabe. Autorzy twierdzą, że największe korzyści przyniesie ścisła integracja projektowania, syntezy i testowania w półautomatyczne, oparte na danych przepływy pracy, przy jednoczesnym otwartym dzieleniu się danymi o fragmentach i metodach, tak aby nawet zespoły o ograniczonych zasobach mogły z nich korzystać. Jeśli te kierunki się utrzymają, podejścia oparte na fragmentach mogą pomóc odwrócić długoterminowy spadek wydajności badań i przyspieszyć pojawienie się bezpieczniejszych, bardziej skutecznych leków na szeroką gamę chorób.
Cytowanie: Grosjean, H., Biggin, P.C. Developments and challenges in hit progression within fragment-based drug discovery. Nat Commun 17, 2226 (2026). https://doi.org/10.1038/s41467-026-68941-z
Słowa kluczowe: odkrywanie leków oparte na fragmentach, optymalizacja hit-to-lead, cykl projektuj-wytwarzaj-testuj, badania przesiewowe o dużej przepustowości, obliczeniowe projektowanie leków