Clear Sky Science · pl
Model polimerowy oparty na danych eksperymentalnych ujawnia wysokorozdzielczą organizację loci genomowych
Jak składanie DNA kształtuje tożsamość komórki
Każda komórka w twoim ciele nosi w zasadzie te same instrukcje DNA, a mimo to komórki mózgowe, skórne i macierzyste zachowują się bardzo różnie. Jednym z kluczowych powodów jest sposób, w jaki to DNA jest składane i upakowane w jądrze. W tym badaniu przedstawiono nowy sposób „oglądania” tego składania z niezwykłą szczegółowością, łącząc fizyczne rozmieszczenie DNA z tym, czy ważne geny są włączone czy wyłączone. Poprzez połączenie eksperymentów z symulacjami opartymi na zasadach fizyki, autorzy ujawniają ukryte skupiska materiału genetycznego, które wydają się działać jako podstawowe cegiełki organizacji genomu.
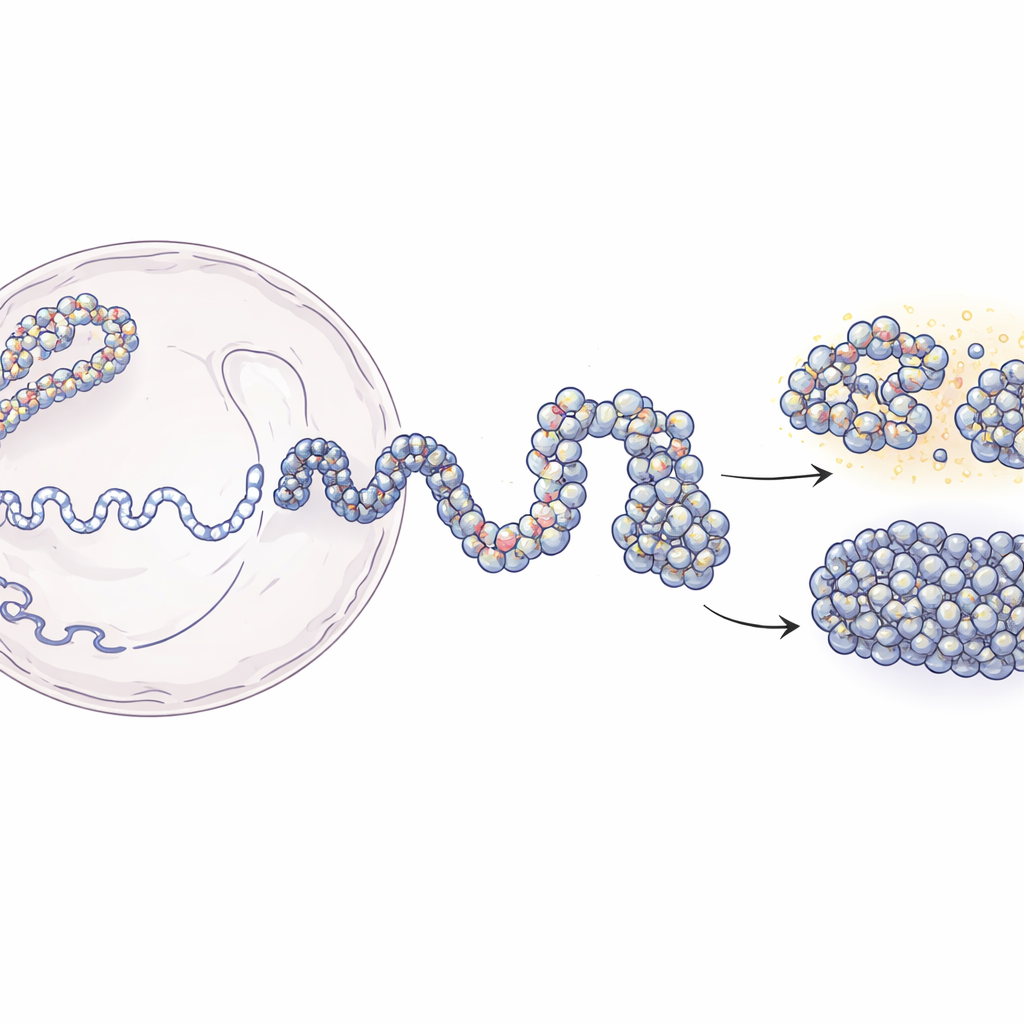
Od długich nici DNA do trójwymiarowych map genomu
W jądrze DNA owija się wokół białkowych wrzecion zwanych nukleosomami, tworząc strukturę koralików na nici znaną jako chromatyna. Nowoczesne techniki, takie jak Hi-C i Micro-C, informują nas, które fragmenty DNA leżą blisko siebie w 3D, ale zwykle dają rozmyte, uśrednione po populacji obrazy. Z kolei eksperymenty lokalizujące pojedyncze nukleosomy dostarczają ostrego, lokalnego szczegółu, ale mało mówią o większej strukturze. Ta praca wypełnia tę lukę. Autorzy zaczynają od niskorozdzielczych map kontaktów, które raportują, jak często odległe segmenty DNA stykają się ze sobą, a następnie łączą je z eksperymentalnymi mapami pozycji nukleosomów. Wykorzystując zasady fizyki polimerów, konstruują symulowane zespoły 3D chromatyny, które zgadzają się z danymi eksperymentalnymi, a jednocześnie rozdzielczością sięgają kilku dziesiątek par zasad DNA.
Strategia dwuetapowa rekonstrukcji chromatyny
Podejście modelowe rozwija się w dwóch głównych etapach. Najpierw zespół wykorzystuje dane Hi-C do wygenerowania wielu możliwych kształtów na dużą skalę dla fragmentu DNA o długości 200 000 zasad, traktując chromatynę jako elastyczny łańcuch, w którym segmenty po 5 000 zasad są delikatnie kierowane do nawiązywania lub unikania kontaktów obserwowanych w eksperymentach. Te zgrubne struktury odwzorowują ogólny wzorzec składania, który wspomagają białka komórkowe. W drugim etapie każda duża kula zostaje zastąpiona dużo drobniejszym łańcuchem złożonym z pojedynczych nukleosomów i krótkich łączników DNA między nimi. Pozycje tych nukleosomów pochodzą z enzymatycznej metody mapowania (MNase-seq), która ujawnia, gdzie przeważnie się lokują wzdłuż genomu. Następnie pozwala się drobnoziarnistym łańcuchom zwinąć, jednocześnie respektując szerszą architekturę. Gdy badacze „rozmywają” swoje wysokorozdzielcze modele z powrotem do rozdzielczości eksperymentalnych, odwzorowują zarówno mapy kontaktów Hi-C, jak i Micro-C z wysoką dokładnością.
Odkrycie skupisk nukleosomów jako jednostek strukturalnych
Gdy autorzy przyjrzeli się zbliżeniom swoich symulowanych struktur, wyłonił się uderzający wzorzec: nukleosomy nie były ułożone równomiernie, lecz grupowały się w nieregularne klastry, które autorzy nazywają skupiskami nukleosomów. Te skupiska przypominają grudkowate struktury widziane wcześniej w obrazach z mikroskopii super-rozdzielczej prawdziwych komórek. Analizując tysiące symulowanych migawkowych struktur, zespół wykazał, że te skupiska są wydłużone, a nie kuliste, i zazwyczaj zawierają kilka zwartych nukleosomów. Co ważne, kontakty wewnątrz tych skupisk odpowiadają ściśle blokom oddziaływań o charakterze domenowym obserwowanym w danych eksperymentalnych, co wskazuje, że skupiska nie są przypadkowe, lecz stanowią fundamentalne jednostki 3D organizacji chromatyny. Symulacje nawet przewidują dodatkowe subtelne granice domen, które trudno wykryć eksperymentalnie, sugerując, że ten model fizyczny potrafi ujawnić drobnoziarniste cechy ukryte w zaszumionych danych.
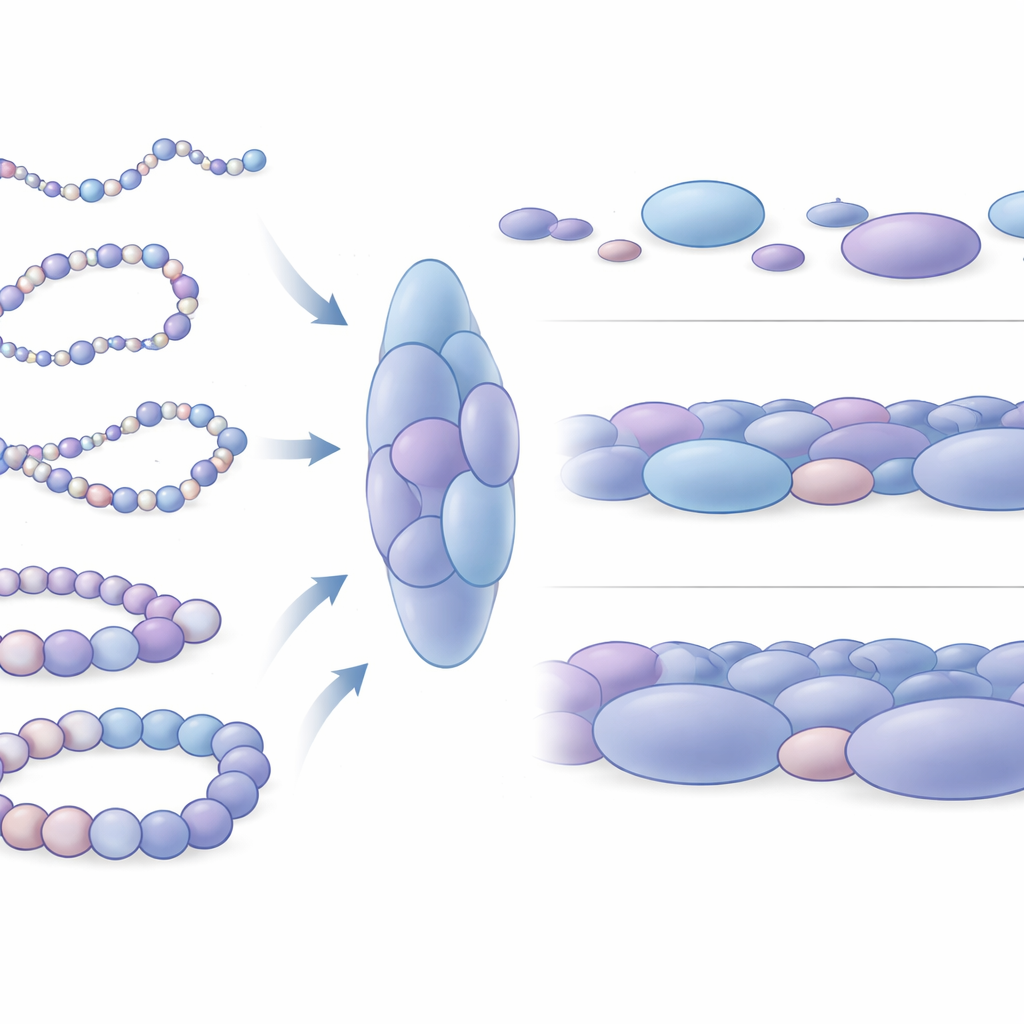
Jak różnice w upakowaniu odzwierciedlają aktywność genów
Następnie badacze zbadali, jak te skupiska różnią się wokół genów aktywnych w porównaniu z genami uśpionymi. Skoncentrowali się na czterech dobrze poznanych fragmentach ludzkiego DNA, w tym na dwóch genach utrzymujących komórki macierzyste w plastycznym, niezróżnicowanym stanie (Nanog i Lin28A) oraz na dwóch genach kontroli rozwoju (HoxB4 i HoxA13), które są wyłączone w tych samych komórkach. Wokół nieaktywnych genów skupiska były średnio większe i bardziej ciasno upakowane, z nukleosomami tworzącymi bardziej zamknięte lokalne układy. W przeciwieństwie do tego skupiska w pobliżu genów aktywnych były mniejsze, nieco luźniejsze i bardziej zróżnicowane. W szerszej skali DNA wokół genów aktywnych przyjmował znacznie więcej różnych kształtów i był mechanicznie bardziej podatny na zginanie, podczas gdy regiony wokół genów uśpionych zachowywały się jak sztywniejsze segmenty chromatyny. Ta mechaniczna różnica prawdopodobnie wpływa na to, jak łatwo odległe elementy regulacyjne DNA mogą się spotykać i współpracować z włącznikami genów.
Dlaczego to ma znaczenie dla zrozumienia kontroli genów
W sumie wyniki malują obraz genomu zbudowanego z dynamicznych skupisk nukleosomów, których rozmiar, kształt i rozstaw decydują o tym, czy pobliskie geny są dostępne, czy zablokowane. Nowy model łączy dane kontaktowe z eksperymentów, mapy nukleosomów i zasady fizyczne w jedną ramę wyjaśniającą, jak geny komórek macierzystych mogą pozostać elastyczne i interaktywne, podczas gdy geny rozwojowe zostają uwięzione w sztywniejszych, bardziej zwartch sąsiedztwach. Dla czytelników niebędących specjalistami kluczowa idea jest taka, że aktywność genów nie jest rządzona wyłącznie sekwencją DNA; zależy także od tego, jak to DNA jest złożone w trójwymiarowe struktury. Ujawniając skupiska nukleosomów jako podstawowe cegiełki tego składania, praca ta oferuje potężną drogę do powiązania mikroskopowej architektury genomu z procesami na dużą skalę, takimi jak rozwój, tożsamość komórkowa i choroba.
Cytowanie: Mittal, R., Heermann, D.W. & Bhattacherjee, A. An experimentally-informed polymer model reveals high resolution organization of genomic loci. Nat Commun 17, 2338 (2026). https://doi.org/10.1038/s41467-026-68928-w
Słowa kluczowe: składanie chromatyny, skupiska nukleosomów, trójwymiarowa organizacja genomu, regulacja genów, modelowanie polimerów