Clear Sky Science · pl
Klonalna ekspansja cytotoksycznych limfocytów CD8⁺ w przebiegu ARIA związanego z leczeniem lekanemabem
Dlaczego to ma znaczenie dla osób z chorobą Alzheimera
Lekanemab jest jednym z pierwszych leków, które potrafią usunąć amyloid z mózgu i w umiarkowanym stopniu spowalniać utratę pamięci w chorobie Alzheimera. Jednak niektórzy pacjenci otrzymujący tę terapię rozwijają obrzęk mózgu lub drobne krwawienia mózgowe — zmiany widoczne w badaniach MRI, grupowane pod pojęciem amyloid‑related imaging abnormalities (ARIA). Badanie stawia kluczowe pytanie dla pacjentów i rodzin: co się dzieje w układzie odpornościowym, gdy pojawia się ARIA, i czy prosty test krwi mógłby kiedyś pomóc przewidzieć, kto jest najbardziej narażony?
Obietnica i ryzyko nowej terapii przeciwko Alzheimerowi
Lekanemab to przeciwciało podawane w infuzji, które celuje w złogi białka zwanego beta‑amyloidem — cechę charakterystyczną choroby Alzheimera. Pomagając organizmowi usuwać amyloid, może ono w umiarkowanym stopniu spowalniać pogorszenie funkcji poznawczych. Ten zysk wiąże się jednak z ryzykiem: u niektórych osób rozwija się ARIA, obejmująca obszary obrzęku mózgu lub drobne ogniskowe krwawienia. Te działania niepożądane wymagają częstego monitorowania za pomocą MRI i mogą ograniczać, kto otrzyma lek. Nie wszyscy są jednakowo podatni — nosiciele wariantu genetycznego APOE4 są bardziej narażeni — ale same geny nie wyjaśniają, dlaczego ARIA pojawia się, zwłaszcza wcześnie po rozpoczęciu leczenia. Ponieważ lekanemab podawany jest do krwiobiegu, autorzy założyli, że uważna analiza komórek odpornościowych w krwi może ujawnić wczesne znaki ostrzegawcze lub mechanizmy łączące terapię z urazem naczyń mózgowych. 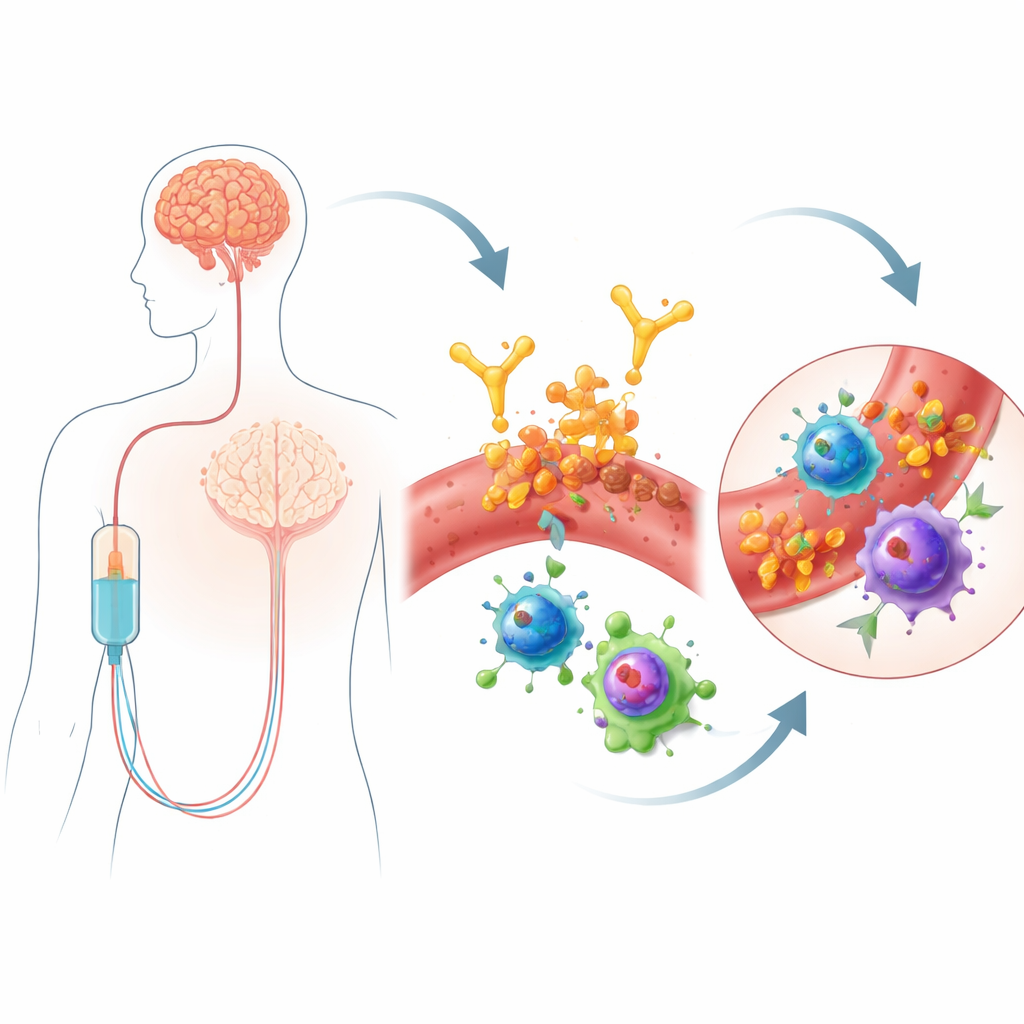
Śledzenie komórek odpornościowych u pacjentów, którzy rozwijali ARIA i którzy nie rozwijali
Naukowcy przebadali sześć osób z chorobą Alzheimera leczonych lekanemabem w regionalnej poradni pamięci. U trzech rozwinęły się różne formy ARIA, a trzech dopasowanych pacjentów (pod względem wieku, płci, genotypu APOE i liczby infuzji) nie wykazało takich zmian. Krew pobierano tuż przed infuzjami, a zespół zastosował intensywne podejście „multi‑omiczne”: sekwencjonowanie RNA pojedynczych komórek, by odczytać, które geny są aktywne w tysiącach indywidualnych komórek odpornościowych; znaczniki oparte na przeciwciałach do definiowania typów komórek; sekwencjonowanie receptorów T‑komórkowych do śledzenia klonów; oraz ukierunkowaną metabolomikę do pomiaru setek małych cząsteczek uczestniczących w metabolizmie komórek. Pozwoliło to zbadać nie tylko, jakie typy komórek występowały, ale jak były aktywne, jakiego paliwa używały oraz czy konkretne rodziny limfocytów T rozszerzały się w odpowiedzi na jakiś bodziec.
Ekspansja silnie uzbrojonych zabójczych limfocytów T
U pacjentów, u których pojawiła się ARIA, wyłonił się wyraźny wzorzec. W porównaniu z grupą kontrolną mieli wyższy odsetek limfocytów CD8 „zabójców” i mniej limfocytów CD4 pomocniczych. W obrębie populacji CD8 wyróżniły się dwie podgrupy: komórki pamięci efektorowej oraz terminalnie zróżnicowana forma znana jako komórki TEMRA. Komórki TEMRA przypominają weteranów — wysoce wyspecjalizowane do ataku, z silnym aparatem do zabijania komórek docelowych. U pacjentów z ARIA komórek TEMRA było więcej, wykazywały większą ekspansję klonalną (co oznacza, że konkretne rodziny limfocytów T się namnożyły) i niosły programy genowe związane z cytotoksycznością, migracją przez naczynia krwionośne oraz oznakami przewlekłej stymulacji. Podobne stany limfocytów T obserwowano w starzeniu się, przewlekłych zakażeniach, stwardnieniu rozsianym oraz w płynie mózgowo‑rdzeniowym osób z chorobą Alzheimera, gdzie mogą gromadzić się w pobliżu naczyń krwionośnych i powierzchni mózgu.
Przestawienie metabolizmu i komunikacja z innymi komórkami odpornościowymi
Zespół odkrył również, że te efektorowe komórki CD8 zmieniły swój metabolizm. Zamiast polegać głównie na efektywnej produkcji energii w mitochondriach, przestawiły się na glikolizę — szybszy, lecz mniej wydajny sposób wytwarzania energii, który wspiera krótkotrwałą, intensywną aktywność. Pomiary metabolitów w komórkach krwi potwierdziły to: poziomy mleczanu i pirogronianu były podwyższone, podczas gdy kluczowe składniki cyklu kwasu cytrynowego były zredukowane — wzorzec typowy dla zapalnych komórek odpornościowych. Monocyty, inny typ krwinek białych, wykazywały zmiany komplementarne. U pacjentów z ARIA monocyty włączały geny związane z prezentowaniem antygenów, adhezją do innych komórek i produkcją chemokin — sygnałów chemicznych przyciągających limfocyty T. Modelowanie komputerowe par ligand‑receptor sugerowało, że monocyty wysyłają silniejsze sygnały aktywujące i kierunkujące do efektorowych komórek CD8, tworząc środowisko sprzyjające angażowaniu ścian naczyń krwionośnych przez te komórki zabójcze.
Kody adresowe kierujące limfocyty T ku naczyniom mózgu
Ponieważ badanie obejmowało jedynie próbki krwi, autorzy sięgnęli do niezależnego zestawu danych pojedynczych komórek z mózgów pacjentów leczonych lekanemabem, aby sprawdzić, czy te same programy limfocytów T łączą się z niszami naczyniowymi w mózgu. Po rzutowaniu swoich podzbiorów CD8 na tę mapę mózgową, komórki TEMRA i pamięci efektorowej od pacjentów z ARIA wykazały transkrypcyjne „kody adresowe” — kombinacje molekuł adhezyjnych i receptorów chemokin — które odpowiadały komórkom śródbłonka (naczyniowym) w chorym mózgu. Te sygnatury sugerują, że rozszerzone komórki zabójcze są nie tylko silnie uzbrojone i metabolicznie pobudzone, ale także ukierunkowane do przemieszczania się i interakcji ze zestresowanymi naczyniami mózgowymi w miejscach oczyszczania amyloidu. 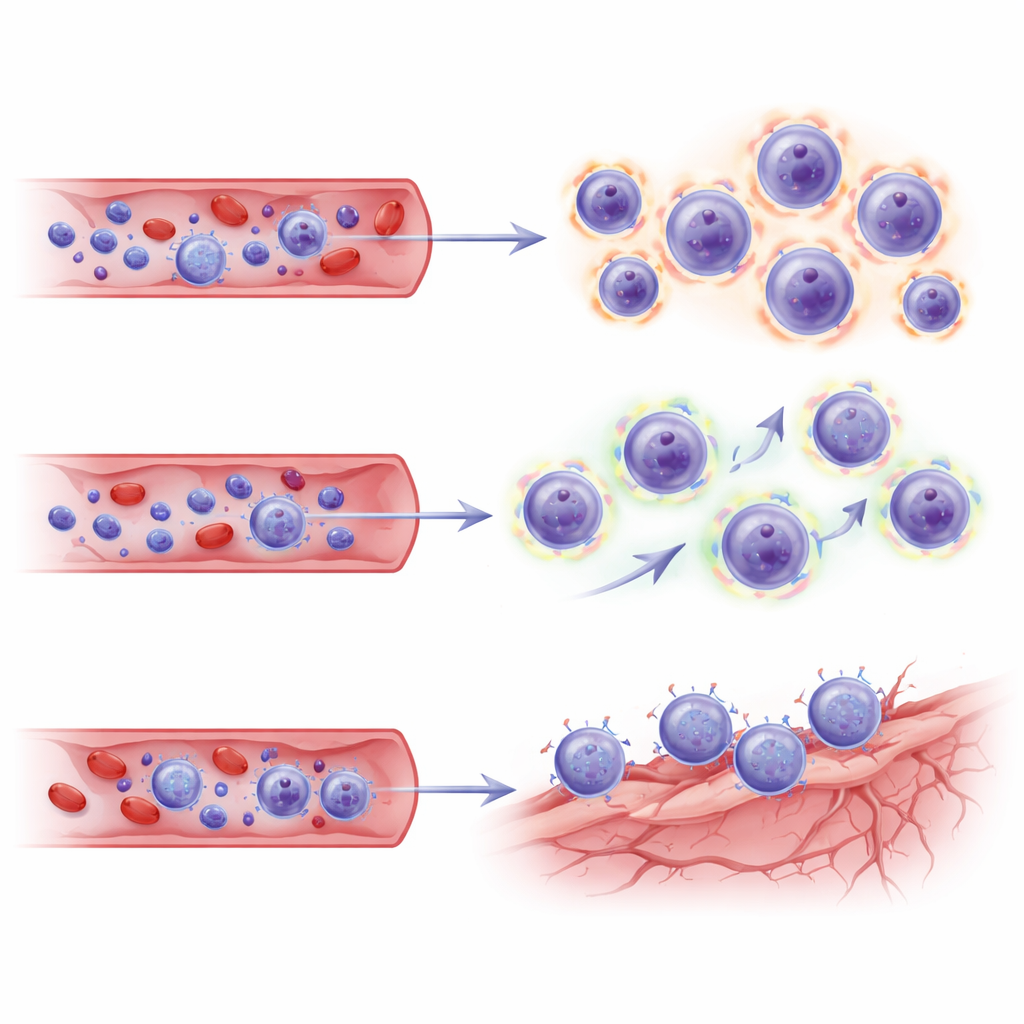
Co to może znaczyć dla pacjentów i przyszłej opieki
Podsumowując, to niewielkie, ale szczegółowe badanie przedstawia ARIA jako coś więcej niż bierne działanie niepożądane usuwania amyloidu. Wygląda na to, że jest powiązane ze skoordynowaną odpowiedzią immunologiczną w krwi: ekspansją i metaboliczną aktywacją konkretnych klonów zabójczych limfocytów T, wzmocnionym sygnalizowaniem ze strony monocytów oraz cechami molekularnymi sprzyjającymi interakcji z naczyniami mózgowymi. Praca ta nie dowodzi, że te komórki powodują ARIA — zmiany immunologiczne mogą być reakcją na uszkodzenie naczyń, a nie jego źródłem — ale dostarcza testowalnych hipotez i planu działania dla biomarkerów opartych na krwi. W przyszłości pomiar liczebności i stanu metabolicznego komórek CD8 TEMRA wraz z kluczowymi cząsteczkami sygnalizacyjnymi może pomóc zidentyfikować pacjentów o najwyższym ryzyku ARIA, dostosować harmonogramy monitorowania lub nawet zainspirować ukierunkowane strategie czasowego stłumienia tej odpowiedzi immunologicznej przy zachowaniu korzyści terapii usuwających amyloid.
Cytowanie: Johnson, L.A., Saito, K., Pallerla, A.V. et al. Clonal expansion of cytotoxic CD8⁺ T cells in lecanemab-associated ARIA. Nat Commun 17, 2180 (2026). https://doi.org/10.1038/s41467-026-68921-3
Słowa kluczowe: Choroba Alzheimera, lekanemab, komórki układu odpornościowego, naczynia krwionośne mózgu, skutki uboczne leczenia