Clear Sky Science · pl
Proteiny TMEM63 działają jako mechanicznie aktywowane, cholesterolowi podlegające ślamaczki lipidów, przyczyniając się do mechanoodporności błony
Jak komórki pozostają nienaruszone pod wpływem naprężeń mechanicznych
Komórki naszego ciała są nieustannie ściskane, rozciągane i potrącane — czy to w bijącym sercu, pracujących mięśniach, czy w guzie przeciskającym się przez tkankę. To badanie ujawnia, jak rodzina białek błonowych, zwana OSCA/TMEM63, pomaga komórkom przetrwać takie silne siły mechaniczne, przestawiając lipidy w ich zewnętrznej powłoce. Zrozumienie tego wbudowanego systemu amortyzacji może odsłonić nowe spojrzenia na zaburzenia słuchu, izolacji nerwów, a nawet rozsiew nowotworów.
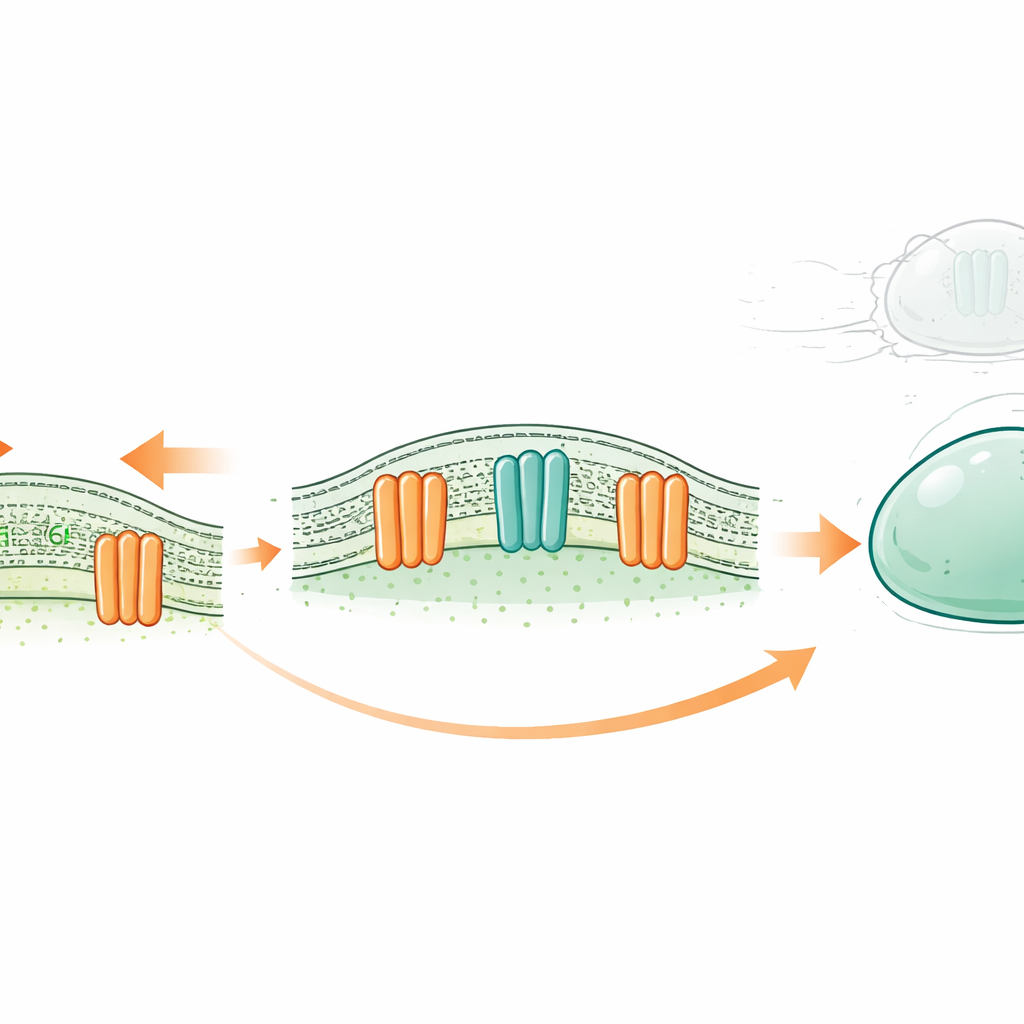
Nowy rodzaj komórkowego amortyzatora
Każda komórka jest otoczona cienką, oleistą błoną zbudowaną z dwóch warstw cząsteczek tłuszczopodobnych zwanych lipidami. Tradycyjnie pewne białka błonowe uważano za wyłącznie kanały jonowe — maleńkie zawory przepuszczające naładowane cząstki w odpowiedzi na bodźce, takie jak rozciąganie. Rodzina OSCA/TMEM63, obecna od roślin po ludzi, jest znana z otwierania się w odpowiedzi na napięcie błony. Wcześniejsze prace strukturalne zasugerowały, że w przeciwieństwie do klasycznych kanałów ich pory są częściowo wyłożone samymi lipidami. To rodzi prowokującą możliwość: czy te kanały mogą również działać jako „scramblazy”, przewracając lipidy między wewnętrzną a zewnętrzną warstwą błony, gdy komórka jest pod obciążeniem?
Obserwowanie przewracania lipidów przez błonę
Aby przetestować ten pomysł, autorzy połączyli symulacje komputerowe z redukcjonistycznymi systemami laboratoryjnymi złożonymi z oczyszczonych składników. W symulacjach otwarte formy kilku białek OSCA i TMEM63 osadzono w modelowych błonach. Molekuły lipidów spontanicznie przemieszczały się przez rowek w tych białkach z jednej strony dwuwarstwy na drugą, tworząc pas łączący obie monowarstwy, pozostawiając jednocześnie wypełnioną wodą ścieżkę dla jonów. W równoległych eksperymentach zespół zbudował olbrzymie sztuczne „bańki” (pęcherzyki) zawierające fluorescencyjne lipidy i konkretne białka. Gdy czynnik zewnętrzny tłumił fluorescencję na powierzchni zewnętrznej, każdy dalszy spadek sygnału mógł być wyjaśniony tylko przez przewrócenie lipidów z warstwy wewnętrznej na zewnątrz. Pęcherzyki zawierające OSCA1.1, OSCA1.2, OSCA2.2 lub TMEM63A/B wykazywały taki dodatkowy ubytek fluorescencji, co wskazywało na aktywne przestawianie, podczas gdy kanały kontrolne, które nie przestawiają lipidów, tego efektu nie miały.
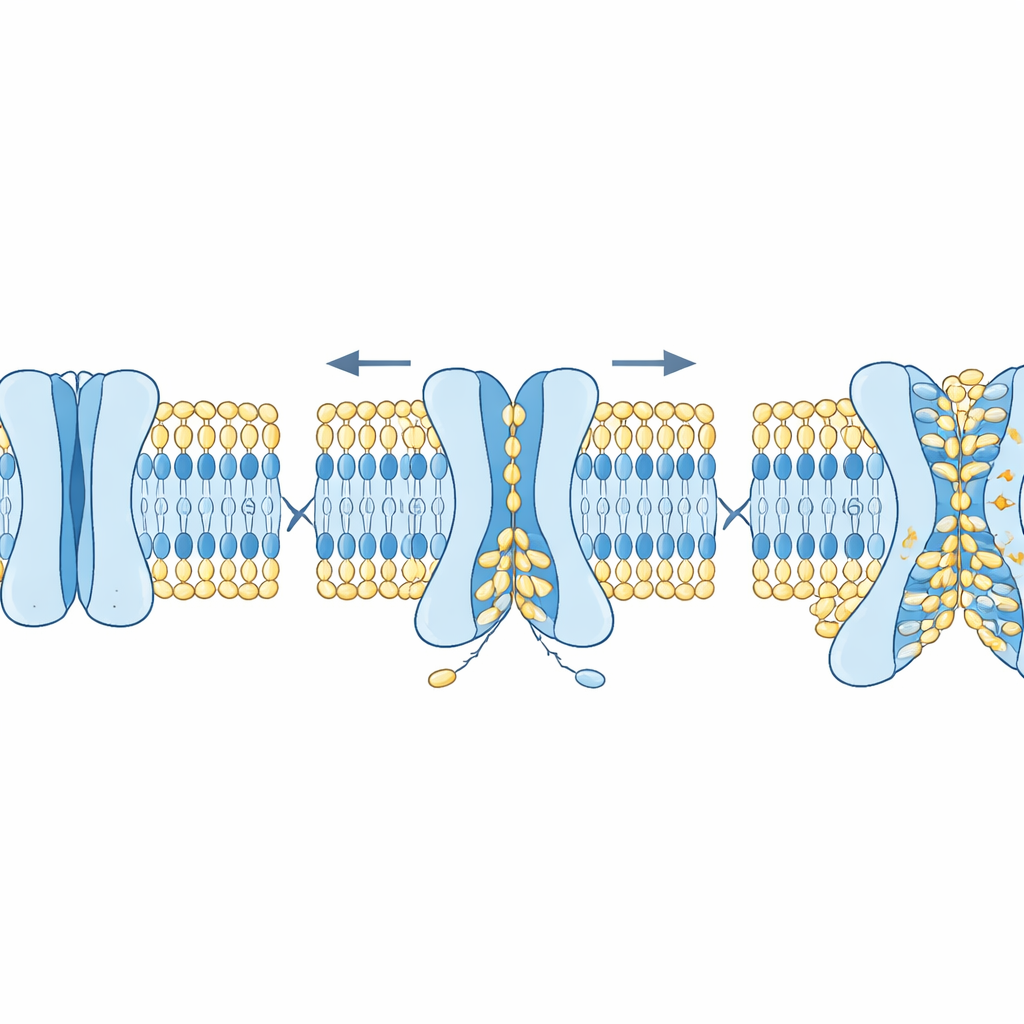
Jak struktura i cholesterol regulują ten proces
Naukowcy zapytali następnie, które cechy białek TMEM63 kontrolują to podwójne zachowanie. Korzystając z AlphaFold2, wygenerowali wiele prawdopodobnych kształtów ludzkich TMEM63, od zamkniętych po coraz bardziej otwarte. Symulacje ujawniły, że garstka masywnych aminokwasów działa jak „wąskie gardła” w rowku. Jeden reszt ogranicza głównie przepływ jonów, podczas gdy inne blokują ruch lipidów. Zmiana (mutacja) w bariery jonowej zwiększała przewodnictwo elektryczne bez istotnej zmiany przestawiania lipidów, natomiast zmiana w „zaporze” lipidowej powodowała łatwiejsze przewracanie lipidów, a nawet sprawiała, że komórki wystawiały sygnały „zjedz mnie” na swojej powierzchni bez dodatkowego bodźca. Kolejnym kluczowym regulatorem był cholesterol — element usztywniający błony komórkowe. Dodanie cholesterolu do modelowych błon znacząco spowalniało przestawianie lipidów i stabilizowało stan zamknięty TMEM63A, zarówno w symulacjach, jak i w strukturach uzyskanych metodą krio‑elektronowej mikroskopii, gdzie cholesterol osadzał się w określonych miejscach na białku.
Siła mechaniczna jako przełącznik
Jeśli cholesterol zwykle powstrzymuje przestawianie w komórkach, co je wtedy uruchamia we właściwym momencie? Zespół użył pierścieniowych cukrów zwanych cyklodekstrynami, aby selektywnie usuwać lipidy z błon i w ten sposób zwiększać napięcie bez usuwania cholesterolu. W pęcherzykach wielkości komórkowej dodanie cyklodekstryny aktywowało przestawianie lipidów przez TMEM63A tylko wtedy, gdy białko było obecne, co dowodzi, że sam stres mechaniczny może wyzwolić przewracanie. Podobne podejścia w żywych komórkach pokazały, że łagodne usunięcie cholesterolu samo w sobie nie wystarcza; konieczne było następnie mechaniczne wyzwanie, by zaobserwować silne przestawianie. Gdy komórki zaprojektowane do ekspresji TMEM63A były wielokrotnie rozciągane, szybko eksponowały pewne lipidy na powierzchni zewnętrznej — znak przestawiania — podczas gdy komórki pozbawione tych białek wykazywały znacznie mniejsze zmiany.
Ochrona komórek przed pęknięciem
Poza przewracaniem lipidów, mechanicznie aktywowane przestawianie zmieniało zachowanie fizyczne błon pod ekstremalnym stresem. W sztucznych pęcherzykach narażonych na duże siły te pozbawione scramblazów miały tendencję do pękania, podczas gdy pęcherzyki zawierające TMEM63A lub znaną scramblazę kurczyły się, tworzyły cienkie rurki i w dużej mierze pozostawały nienaruszone. W ludzkiej linii komórek raka mózgu, która naturalnie wyraża TMEM63A i TMEM63B, obniżenie poziomu któregokolwiek z tych białek zwiększało prawdopodobieństwo pęknięcia komórek pod silnym stresem mechanicznym. Razem te obserwacje wspierają model, w którym białka OSCA/TMEM63 działają jak zawory otwierające się pod napięciem i tymczasowo rozmazujące zwykłe różnice między wewnętrzną a zewnętrzną stroną błony. Pozwalając lipidom szybko się przemieszcząć, pomagają wyrównać naprężenia i zapobiec katastrofalnym rozdarciom.
Co to oznacza dla zdrowia i chorób
Mówiąc wprost, ta praca pokazuje, że niektóre kanały wrażliwe na rozciąganie robią więcej niż przewodzą sygnały elektryczne: reorganizują także zewnętrzną „skórę” komórki, pomagając jej przetrwać ściskanie. Białka TMEM63 wyłaniają się jako mechanicznie aktywowane scramblazy lipidów, których aktywność jest precyzyjnie regulowana przez skład błony, w szczególności przez cholesterol. Ten mechanizm mechanoodporności może być ważny wszędzie tam, gdzie komórki są narażone na duże siły — od izolacji włókien nerwowych i komórek słuchowych po komórki nowotworowe przemieszczające się przez gęste tkanki. Zrozumienie i ostatecznie modulowanie tej podwójnej funkcji kanału jonowego i scramblazy może otworzyć nowe drogi do ochrony wrażliwych tkanek — lub przeciwnie, do uczynienia trudnych do zabicia komórek nowotworowych bardziej podatnymi na zniszczenie.
Cytowanie: Lin, Y., Zhou, Z., Han, Y. et al. TMEM63 proteins act as mechanically activated cholesterol modulated lipid scramblases contributing to membrane mechano-resilience. Nat Commun 17, 2717 (2026). https://doi.org/10.1038/s41467-026-68919-x
Słowa kluczowe: mechanoczułe kanały jonowe, przestawianie lipidów, mechanika błony komórkowej, regulacja cholesterolem, białka TMEM63 OSCA