Clear Sky Science · pl
Toksyczny kryptopetyd powstający w wyniku zależnego od TDP-43 kryptycznego składania PKN1
Ukryte zagrożenia wewnątrz komórek mózgu
Wiele chorób mózgu, w tym stwardnienie zanikowe boczne (SLA) i choroba Alzheimera, wiąże się z agregatami białka zwanego TDP-43. Naukowcy wiedzą, że kiedy to białko przestaje działać poprawnie, komórki nerwowe tracą kluczowe komunikaty i z czasem obumierają. W tej pracy odkryto zaskakujący zwrot akcji: utrata funkcji TDP-43 może także powodować, że komórki mózgu wytwarzają wcześniej nieznany, toksyczny mini‑białek, który z kolei uszkadza obwody pamięciowe. Zrozumienie tej ukrytej postaci może otworzyć nowe drogi diagnostyki i leczenia w niszczycielskich otępieniach.
Jak komórkowy korektor pilnuje porządku w RNA
W neuronach TDP-43 działa jak korektor dla RNA — pośrednich komunikatów między DNA a białkami. Wiąże się z określonymi krótkimi sekwencjami i blokuje wstawianie zbędnych „dodatków” do tych komunikatów. Gdy TDP-43 zostaje utracony lub źle ulokowany, jak w SLA i wielu przypadkach choroby Alzheimera, do RNA mogą wsuwać się te dodatkowe fragmenty — nazywane kryptycznymi eksonami. Do tej pory większość znanych kryptycznych eksonów powodowała jedynie utratę normalnego białka przez destabilizację i szybkie zniszczenie komunikatu. Nie było jasne, czy takie zdarzenia mogą też generować nowe, szkodliwe białka.
Kryptyczne składanie tworzy toksyczny fragment
Autorzy skupili się na genie PKN1, który pomaga utrzymać wewnętrzny szkielet i przepływ sygnałów w neuronach. W modelach komórkowych z obniżonym poziomem TDP-43 odkryli wcześniej nieznany kryptyczny ekson, nazwany PKN1‑5a1, wstawiony między dwa normalne odcinki RNA PKN1. To wstawienie wprowadza wczesny sygnał stop, tworząc skrócony RNA. Co godne uwagi, część tej wadliwej informacji omija system kontroli jakości komórki i jest translokowana na stabilny fragment białka PKN1 zawierający jedynie pierwsze 207 aminokwasów. Zespół nazwał ten skrócony produkt PKN207. Pokazali, że TDP-43 normalnie zapobiega temu błędowi, wiążąc się z kilkoma regionami bogatymi w UG otaczającymi kryptyczny ekson; gdy to wiązanie zostaje utracone, ekson jest włączany i powstaje PKN207.
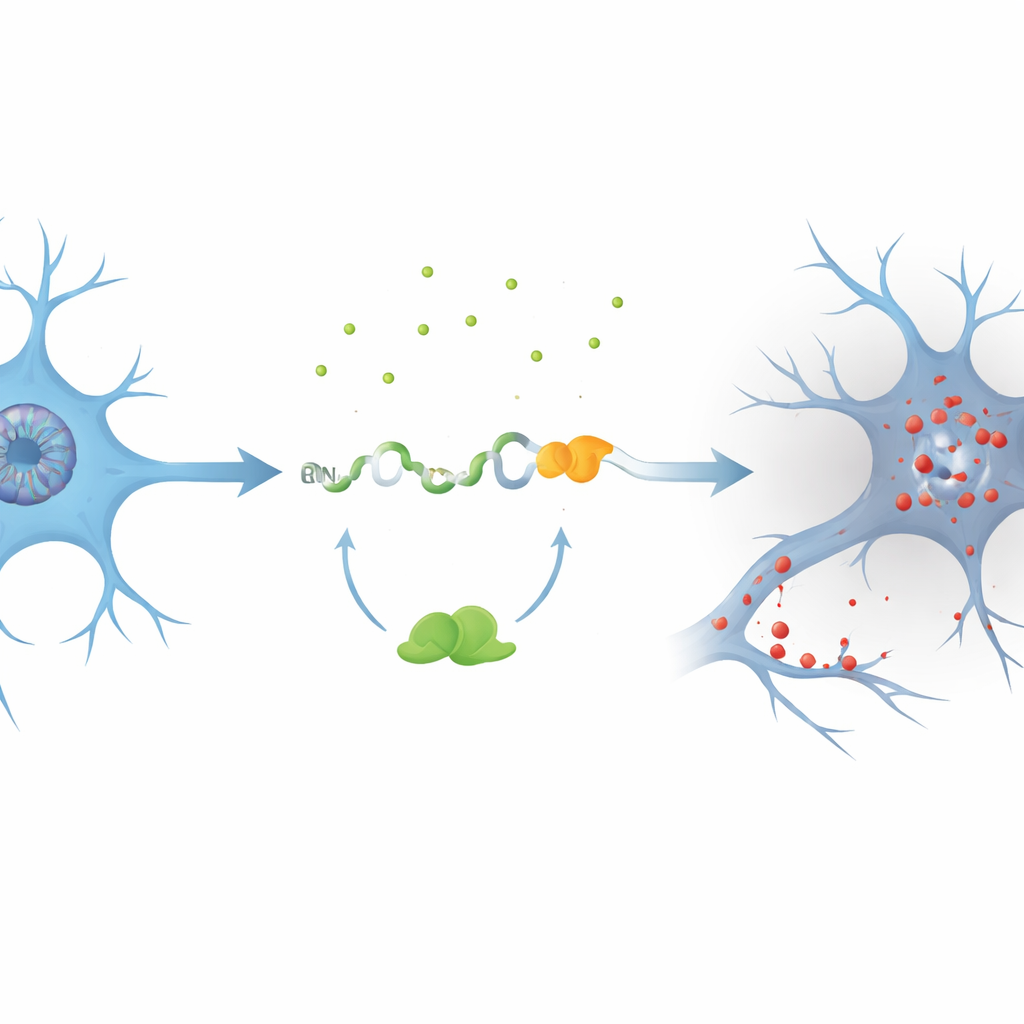
Dane z mózgów pacjentów i dużych zbiorów
Aby sprawdzić, czy to zdarzenie występuje w ludzkiej chorobie, badacze przeanalizowali dane sekwencjonowania RNA z setek próbek mózgu i rdzenia kręgowego od chorych na SLA. Stwierdzili powszechną aktywację kryptycznego eksonu PKN1‑5a1 w regionach znanych z patologii TDP-43, takich jak kora ruchowa i rdzeń kręgowy, ale nie w stosunkowo oszczędzonym móżdżku. Następnie wytworzyli wysoce specyficzne przeciwciała rozpoznające tylko unikalny ogon PKN207, a nie białko PKN1 w pełnej długości. W tkance hipokampa od pacjentów z Alzheimerem, którzy także wykazywali nieprawidłowe, fosforylowane TDP-43, przeciwciała te wykryły wyraźny pas odpowiadający PKN207, podczas gdy taki pas był nieobecny w mózgach kontrolnych. Dodatkowe zbiory danych z choroby Alzheimera potwierdziły, że kryptyczny ekson jest aktywowany nawet we wczesnych stadiach choroby, co sugeruje, że ten błąd molekularny może rozpoczynać się na długo przed pojawieniem się oczywistych objawów.
Mini‑białko o dużym wpływie na pamięć
Obecność PKN207 w chorym ludzkim mózgu postawiła kluczowe pytanie: czy jest ono szkodliwe? Aby to sprawdzić, zespół użył wirusów do wymuszenia produkcji albo normalnego PKN1, albo PKN207 specyficznie w hipokampie — obszarze mózgu kluczowym dla pamięci — młodych myszy. Po kilku miesiącach obie grupy myszy wykazały upośledzenie uczenia się w teście Morris water maze, pływając dłużej, by znaleźć ukrytą platformę. Płyn mózgowo‑rdzeniowy zawierał podwyższone poziomy lekkiego łańcucha neurofilamentów, markera uszkodzenia aksonów. W hodowanych neuronach zwiększenie poziomu PKN207 wywołało uszkodzenie komórek, mierzone przez wypływ enzymu wskazującego na uszkodzenie błony. Szczegółowy profil białkowy hipokampa ujawnił szerokie zmiany w szlakach związanych z siłą synaptyczną (długotrwałe wzmocnienie) i dobrze znanymi chorobami neurodegeneracyjnymi, z szczególnie silnym zaburzeniem cząsteczek wspierających efektywne przekazywanie sygnału i zdrowy szkielet włókien nerwowych.
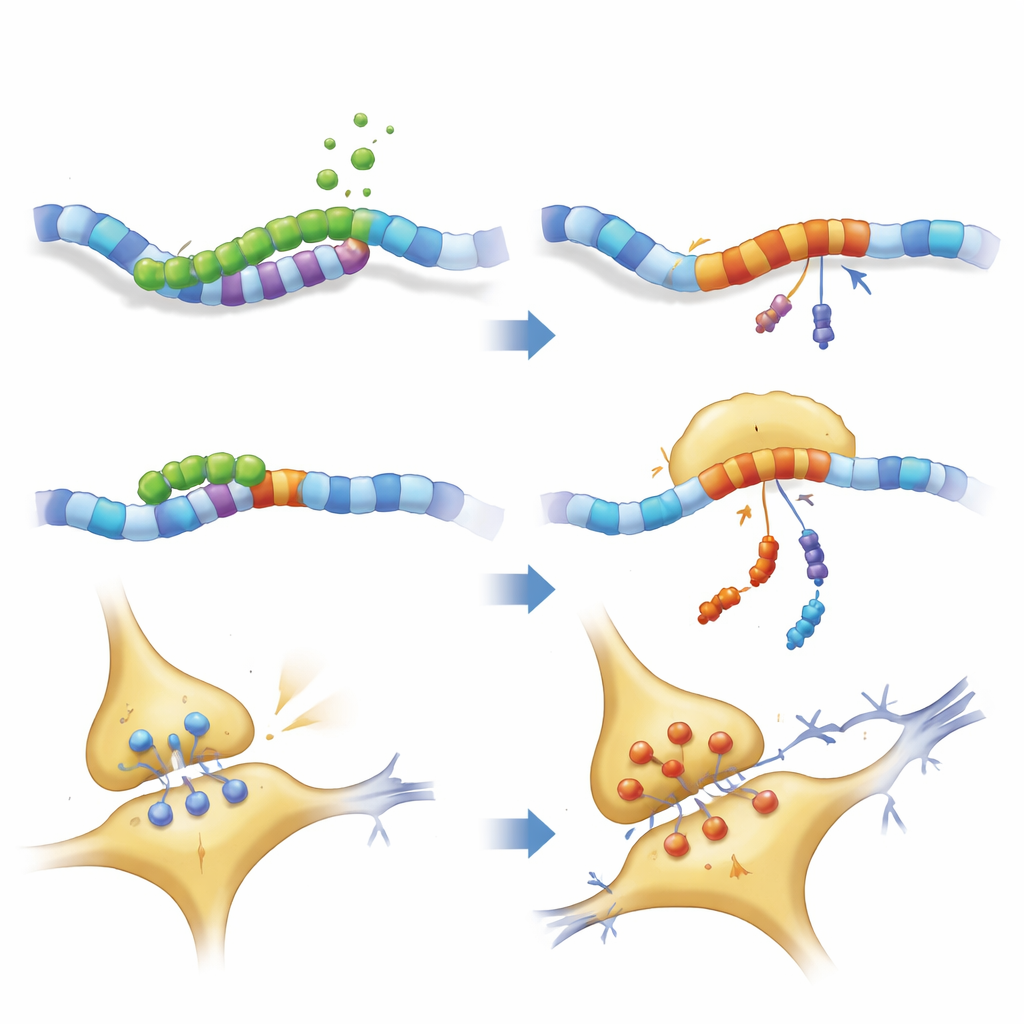
Jak fragment zaburza okablowanie mózgu
Bardziej szczegółowe badanie struktury neuronów wykazało, że zarówno PKN1 w pełnej długości, jak i PKN207 zaburzały sieć neurofilamentów, która nadaje aksonom kształt i pomaga w transporcie ładunku. Kluczowe białka motoryczne i szkieletowe były zredukowane, podczas gdy niektóre składniki neurofilamentów gromadziły się, sugerując korki w transporcie i możliwe agregacje. Nagrania elektryczne z plastrów hipokampa potwierdziły, że myszy wyrażające PKN207 miały osłabione długotrwałe wzmocnienie — proces, w którym synapsy wzmacniają się po powtarzającej się aktywności i uznawany za komórkową podstawę uczenia się i pamięci. Mimo że PKN207 nie zawiera domeny enzymatycznej PKN1, jego obecność wystarczyła, by naśladować, a czasem przewyższyć destrukcyjne efekty pełnego białka, co sugeruje, że wspólny region N‑terminalny może samodzielnie zakłócać homeostazę neuronów.
Dlaczego to odkrycie ma znaczenie dla chorób mózgu
Ta praca dodaje nową warstwę do zrozumienia zaburzeń związanych z TDP-43. Zamiast jedynie powodować utratę niezbędnych RNA, niewydolność TDP-43 może także rodzić stabilne, toksyczne mikro‑białko, które podważa synapsy i funkcje poznawcze. Kryptyczny ekson PKN1‑5a1 i jego peptydowy produkt PKN207 wyróżniają się teraz jako potencjalne biomarkery wczesnej dysfunkcji TDP-43 oraz jako kandydaci na cele terapeutyczne, które korygują składanie RNA lub blokują szkodliwy fragment. Szerzej, badanie sugeruje, że inne ukryte eksony mogą w podobny sposób generować peptydy napędzające chorobę, wskazując badaczom bogate — i wcześniej pominięte — środowisko molekularnych sprawców w neurodegeneracji.
Cytowanie: Yang, M., Wang, Q., Yan, R. et al. A neurotoxic cryptic peptide arising from TDP-43-dependent cryptic splicing of PKN1. Nat Commun 17, 2963 (2026). https://doi.org/10.1038/s41467-026-68916-0
Słowa kluczowe: TDP-43, kryptyczne składanie, PKN1, neurodegeneracja, Alzheimer i SLA