Clear Sky Science · pl
Przeciwdziałające sobie białka FOX epigenetycznie kontrolują równowagę między cyklem litycznym a latencją wirusa opryszczki
Dlaczego ukryte wirusy opryszczki mają znaczenie
Wiele osób nosi wirusy opryszczki pospolitej przez całe życie, często nieświadomie. Wirusy te mogą przez lata tkwić w spoczynku w komórkach nerwowych, a potem nagle się reaktywować, powodując zajady, choroby oczu lub poważniejsze problemy u osób z osłabionym układem odpornościowym. Co sprawia, że wirus przez większość czasu pozostaje uśpiony, a co go ponownie uruchamia — to od dawna nierozwiązana zagadka. To badanie ujawnia kluczowy element tego systemu kontroli: przeciąganie liny między dwiema przeciwnymi grupami ludzkich białek, które przebudowują DNA wirusa i decydują, czy opryszczka pozostanie w stanie ciszy, czy zacznie tworzyć nowe wirusy.
Dwie komórki gospodarza ciągnące w przeciwnych kierunkach
Autorzy skupili się na dużej rodzinie ludzkich białek wiążących DNA zwanych białkami FOX, które normalnie regulują nasze własne geny podczas rozwoju i metabolizmu. Testując wielu przedstawicieli rodziny FOX w komórkach przypominających neurony, odkryli wyraźne dwie frakcje. Jedna grupa (w tym białka takie jak FOXF1) silnie zwiększała replikację wirusa opryszczki pospolitej typu 1 (HSV‑1) i kilku powiązanych wirusów z rodziny „alfa”. Druga grupa (FO XK1 i FOXK2) działała odwrotnie, zdecydowanie hamując wzrost wirusa. Ta równowaga nie była jednak taka sama we wszystkich typach komórek: komórki nie‑neuronalne i zestresowane neurony miały skłonność do wytwarzania większych ilości aktywujących białek FOX, podczas gdy spoczynkowe neurony czuciowe produkowały bardzo mało białek aktywujących, ale dużo represyjnych FOXK.
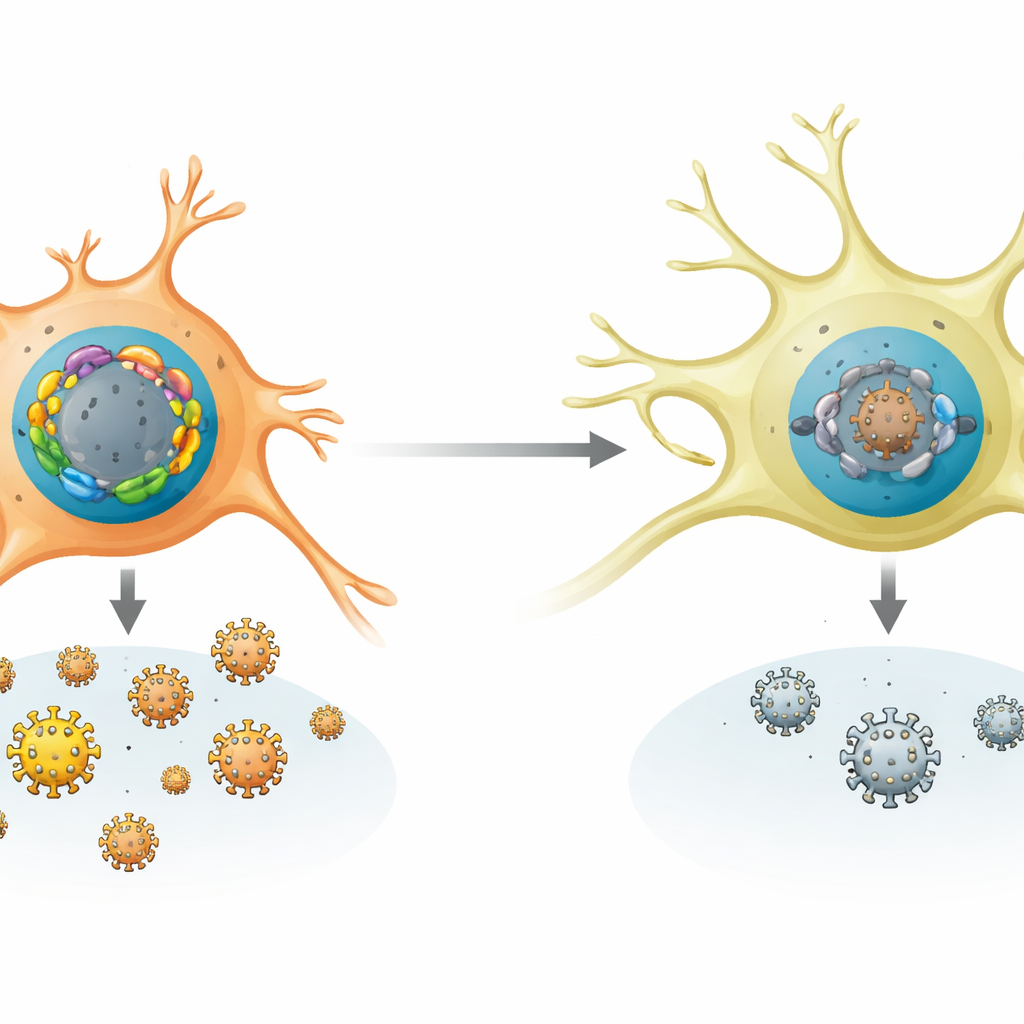
Jak komórki nerwowe sprzyjają stanowi uśpienia
Zespół porównał aktywność genów FOX w wielu typach komórek ludzkich i mysich oraz u zakażonych zwierząt. Neurony czuciowe, naturalne miejsce latencji HSV‑1, wykazywały wzorzec sprzyjający ciszy: silną ekspresję FOXK1 i FOXK2 oraz słabą ekspresję większości aktywujących genów FOX. U myszy wczesne zakażenie i późniejsze sygnały stresowe, takie jak gorączka lub uszkodzenie tkanki, selektywnie podnosiły poziomy kilku aktywujących genów Fox bez obniżania poziomów represyjnych. W hodowlach neuronów mysich i u żywych myszy usunięcie lub wyciszenie białek FOXK ułatwiało replikację HSV‑1 i jego wybudzanie z latencji. Odwrotnie, wymuszenie w neuronach nadprodukcji aktywujących białek FOX wystarczało, by wywołać reaktywację nawet bez chemicznych bodźców, co pokazuje, jak bardzo stan wirusa zależy od tej równowagi FOX.
Chwytanie DNA wirusa i jego otwieranie albo zamykanie
Aby zrozumieć mechanizm leżący u podstaw obserwacji, badacze zmapowali miejsca wiązania białek FOX na genomie wirusa. Stwierdzili, że zarówno aktywator FOXF1, jak i represor FOXK1 wiążą się szeroko wzdłuż DNA HSV‑1, nie tylko przy kilku specyficznych motywach sekwencyjnych. To wiązanie opiera się na konserwowanej części białek FOX, która chwyta szkielet DNA, a nie pojedyncze nukleotydy, co pozwala im przyłączać się niemal w dowolnym miejscu. Gdy są już związane, dwie frakcje białek rekrutują różne partnery molekularne przebudowujące chromatynę — kombinację DNA i białek opakowujących. Aktywujące białka FOX, zwłaszcza FOXF1, łączą się z enzymami CBP i P300, które dodają grupy acetylowe do histonów i rozluźniają chromatynę. To zwiększa dostępność DNA wirusa i wzmacnia aktywność genów wirusowych w fazach wczesnej, środkowej i późnej. Natomiast FOXK1 współdziała z czynnikami takimi jak SIN3A i MAX powiązanymi z deacetylacją histonów i represją genów, uszczelniając chromatynę wirusa i utrzymując geny w stanie wyciszenia.
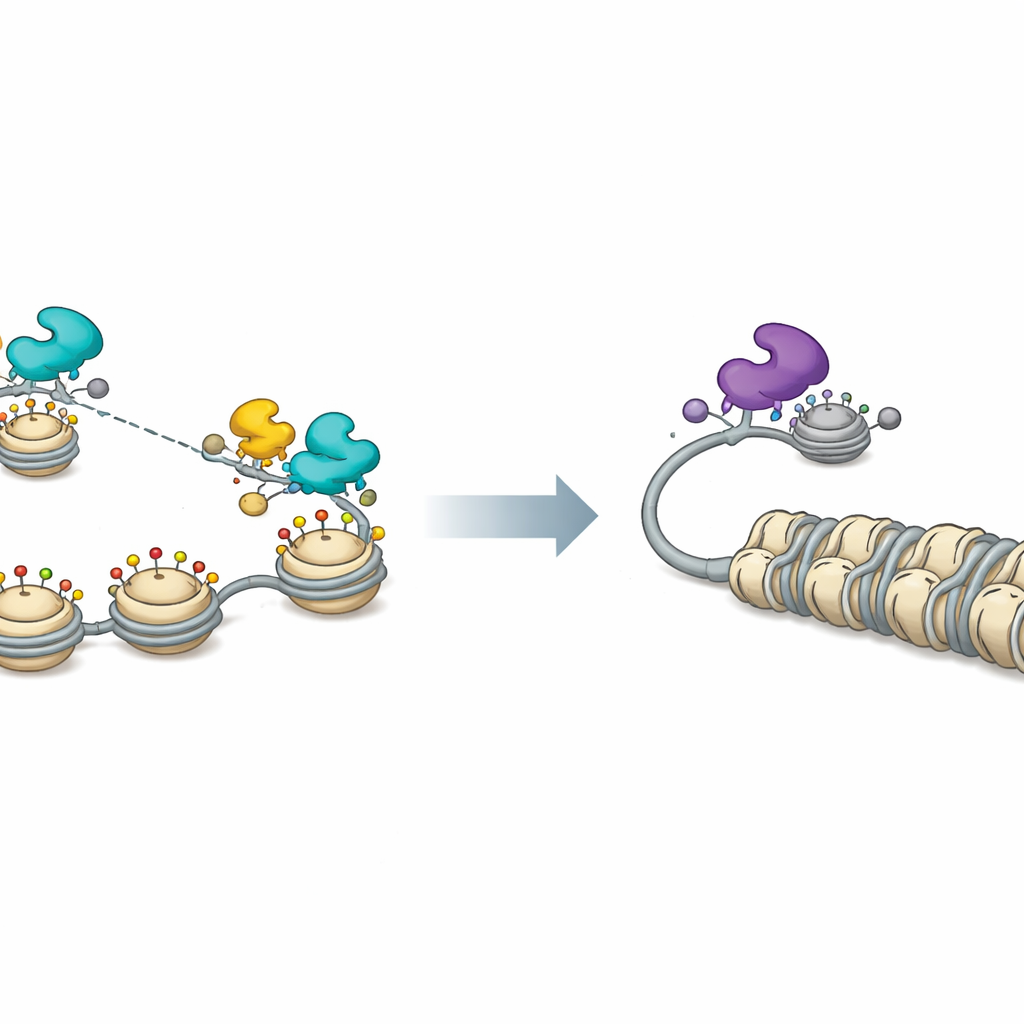
Przełącznik chromatynowy decydujący o śnie i przebudzeniu wirusa
Pomiary chromatyny wirusowej potwierdziły ten obraz. W obecności FOXF1 histony na DNA wirusa były zdezaketylowane lub chemicznie oznaczone w sposób związany z otwartą, aktywną chromatyną, a ogólna dostępność promotorów wirusowych wzrastała w całym genomie. Ekspresja FOXF1 rozpraszała też małe jądrowe struktury zwane ciałkami PML, które normalnie pomagają utrzymać DNA wirusa w stanie represji. Zablokowanie CBP i P300 usuwało wiele z tych efektów aktywujących i ograniczało napędzaną przez FOXF1 ekspresję genów wirusowych. Po stronie represyjnej badacze wykazali, że partnerzy związani z FOXK1 i aktywność deacetylaz histonowych są ważne dla utrzymywania niskiej replikacji HSV‑1; chemiczne zahamowanie deacetylaz zarówno zwiększało produkcję wirusa, jak i osłabiało supresję mediowaną przez FOXK1.
Co to znaczy dla kontroli infekcji trwającej całe życie
Podsumowując, praca sugeruje, że to, czy HSV‑1 jest aktywny, czy uśpiony, w dużej mierze zależy od składu białek FOX w neuronie gospodarza. Spoczynkowe neurony czuciowe naturalnie sprzyjają represyjnemu stanowi zdominowanemu przez FOXK, wciskając wirusa w głęboką ciszę z zwartą chromatyną. Stresy lub inne warunki podnoszące poziomy aktywujących białek FOX mogą przechylić tę równowagę, otwierając chromatynę wirusa i pozwalając wznowić cykl lityczny. Ujawniając tę epigenetyczną walkę o wpływy, badanie podkreśla nowe podejścia, które naukowcy mogliby kiedyś wykorzystać, by trwale wypchnąć wirusy opryszczki w bezpieczną latencję lub, alternatywnie, świadomie je wywoływać, by móc je następnie usunąć.
Cytowanie: Xiang, Y., Yang, X., Zhang, J. et al. Counteracting FOX proteins epigenetically control the herpesvirus lytic-latent balance. Nat Commun 17, 2256 (2026). https://doi.org/10.1038/s41467-026-68915-1
Słowa kluczowe: latencja wirusa opryszczki pospolitej, czynniki transkrypcyjne FOX, chromatyna wirusowa, regulacja epigenetyczna, reaktywacja wirusa