Clear Sky Science · pl
Poszerzanie potencjału uszkadzania DNA przez sztuczne metalo-nukleazy za pomocą chemii klik
Budowanie sprytniejszych molekularnych nożyc
Chemioterapia często działa przez uszkadzanie DNA komórek nowotworowych, ale dzisiejsze leki bywają narzędziami tępego uderzenia, które także ranią tkanki zdrowe. W badaniu przedstawiono nową klasę wysoce programowalnych „molekularnych nożyc” zbudowanych z miedzi i małych fragmentów organicznych łączonych techniką chemii klik. Poprzez dostrajanie kształtu i sposobu, w jaki chwytają DNA, badacze dążą do stworzenia środków, które przecinają materiał genetyczny bardziej precyzyjnie, otwierając drogę do przyszłych terapii przeciwnowotworowych i przeciwbakteryjnych.
Składanie trójramiennego narzędzia tnącego
Zespół wykorzystuje katalizowaną miedzią chemię klik — metodę nagrodzoną Nagrodą Nobla i znaną z niezawodności — do złożenia rodziny cząsteczek nazwanych ligandami Tri-Click (TC). Każda cząsteczka TC to trójramienny trzon, który może jednocześnie utrzymać trzy jony miedzi, tworząc zwartą klaster zdolny do ataku na DNA. Poprzez podmianę różnych chemicznych grup „donorowych” na końcach ramion — opartych na azocie, tlenie lub siarce — naukowcy systematycznie badali, jak subtelne zmiany strukturalne wpływają na wiązanie miedzi, rozpoznawanie DNA i aktywność biologiczną. Wśród kilku nowych projektów szczególnie obiecujące okazały się warianty z płaskimi, pierścieniowymi donorami azotowymi, które dobrze chwytają DNA.
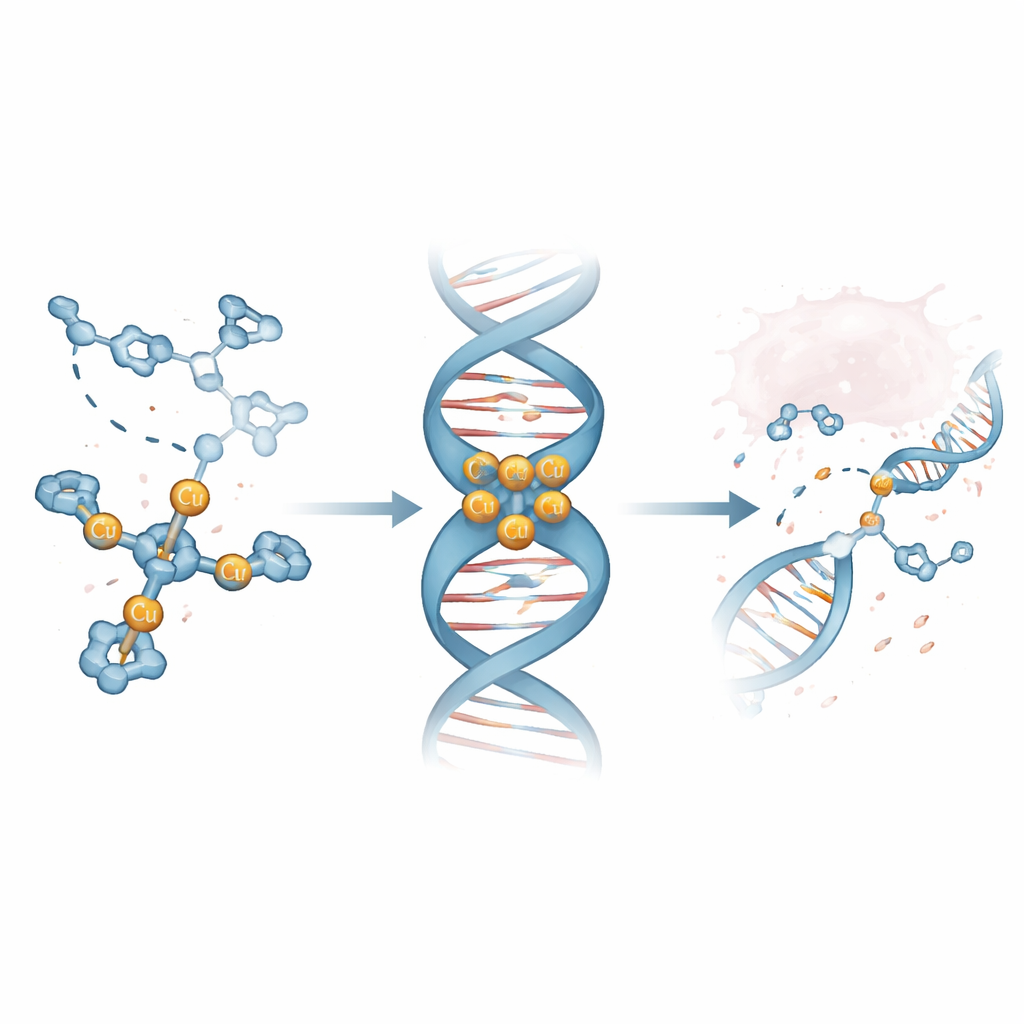
Odkrycie wiodącej cząsteczki preferującej rowki DNA
Za pomocą spektrometrii mas i metod optycznych badacze wykazali, że jeden kompleks o nazwie Cu3-TC-Py wiąże się niezawodnie w trójmiedziowy klaster stabilny w roztworze. Doświadczenia konkurencyjne z fluorescencyjnymi barwnikami związanymi z DNA z grasicy cielęcej pokazały, że Cu3-TC-Py wypiera te barwniki przy bardzo niskich stężeniach, co wskazuje na silne wiązanie z DNA. Badania uzupełniające na krótkich, włosowatych fragmentach DNA wykazały, że kompleks woli zagnieździć się w rowku minor — węższej dolinie owijającej się wokół podwójnej helisy DNA — i szczególnie preferuje odcinki bogate w pary nukleotydów G i C. Symulacje komputerowe o wysokiej rozdzielczości potwierdziły ten obraz, pokazując trójramienny kompleks osadzony w rowku, z ładunkami dodatnimi obejmującymi ujemnie naładowany rdzeń DNA i delikatnie upakowującymi helisę.
Od silnego wiązania do kolapsu i przecięcia DNA
Na poziomie pojedynczych cząsteczek zespół obserwował długie nici DNA ograniczone w nano-kanałach podczas interakcji z Cu3-TC-Py. Przy niskich dawkach kompleks konkurował z barwnikiem rozciągającym nici, wypierając go w miarę wiązania się w rowkach. Przy wyższych dawkach DNA zaczynało kurczyć się, a następnie całkowicie kondensować, co odpowiada silnej atrakcji elektrostatycznej między klastrem miedzi a szkieletowym łańcuchem DNA. Gdy plazmidowe DNA eksponowano na kompleks w obecności środka redukującego, nici przeszły ze swojej natywnej skręconej formy do zrelaksowanej, a potem całkowicie liniowej formy — wzorzec sygnalizujący powstawanie zarówno pojedynczych, jak i podwójnych przerw w nici. Dalsze testy z pochłaniaczami rodników wskazały, że prawdziwymi narzędziami tnącymi wytwarzanymi w pobliżu związanego kompleksu są krótkożyjące gatunki tlenowe — takie jak nadtlenek, tlen singletowy i rodniki hydroksylowe.
Atak na DNA w komórkach nowotworowych i bakteryjnych
Idąc dalej niż oczyszczone DNA, badacze sprawdzili, jak Cu3-TC-Py zachowuje się wewnątrz żywych komórek. W panelach komórek nowotworowych wolne ligandy zawierające aromatyczne, bogate w azot grupy wykazywały znacznie silniejsze hamowanie wzrostu niż wcześniejsze projekty, a w pełni uformowany kompleks miedziowy był jeszcze bardziej silny, zabijając kilka linii komórkowych nowotworowych w stężeniach mikromolowych. Pomiary wewnątrzkomórkowej miedzi wykazały, że Cu3-TC-Py efektywnie transportuje miedź do komórek i wywołuje nagromadzenie uszkodzonego DNA, wykryte metodą obrazowania wspomaganą naprawą, która oznacza uszkodzenia na rozciągniętych niciach genomowych. W bakteriach mikroskopia pokazała, że leczenie szybko zaburza zwarty chromosom bakteryjny, rozpraszając DNA po całej komórce i przypominając silne fragmentowanie obserwowane w przypadku silnego antybiotyku uszkadzającego DNA, co jest zgodne z masowym zniszczeniem materiału genetycznego.
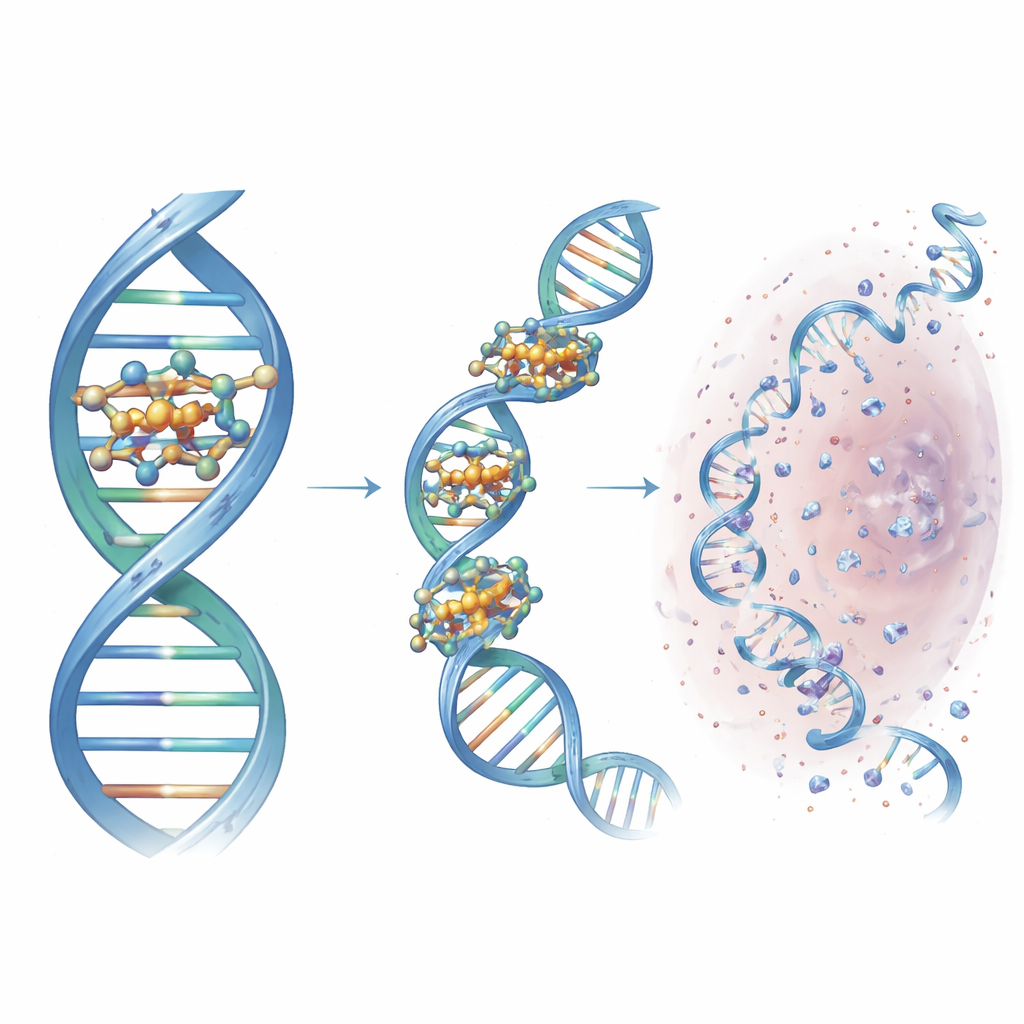
Dlaczego te zaprojektowane nożyce mają znaczenie
Dla niespecjalisty kluczowym wnioskiem jest to, że badacze przekształcili prosty, modułowy szkielet oparty na chemii klik w precyzyjnie dostrojone narzędzie tnące DNA. Wybierając odpowiednie pierścieniowe grupy azotowe, stworzyli zwarty klaster miedzi, który zadokowuje się w konkretnym rowku DNA, ściąga nici razem i lokalnie generuje reaktywne formy tlenu przecinające podwójną helisę. Ta wiodąca cząsteczka, Cu3-TC-Py, uszkadza DNA skutecznie zarówno w komórkach nowotworowych, jak i bakteryjnych i pokazuje, jak racjonalne projektowanie może wysmuklić działanie leków opartych na metalach. Choć przed zastosowaniami klinicznymi pozostaje wiele pracy, badanie wytycza zasady projektowania dla następnej generacji molekularnych nożyc, które pewnego dnia mogłyby zaoferować bardziej ukierunkowane terapie przeciwnowotworowe i nowe strategie przeciwmikrobowe.
Cytowanie: Gibney, A., Sidarta, M., Delahunt, E. et al. Expanding the DNA damaging potential of artificial metallo-nucleases with click chemistry. Nat Commun 17, 2309 (2026). https://doi.org/10.1038/s41467-026-68911-5
Słowa kluczowe: chemia klik, uszkodzenia DNA, kompleksy miedzi, leki przeciwnowotworowe, sztuczne nukleazy