Clear Sky Science · pl
Ewolucyjne przekształcenie kompleksu tiolazy metabolicznej umożliwia biosyntezę antybiotyku
Jak codzienne mikroby reinventują swoją chemię
Wiele antybiotyków i leków, na których polegamy, jest cicho wytwarzanych przez bakterie. Te drobne zakłady chemiczne używają enzymów — molekularnych maszyn — do budowy złożonych związków obronnych. W tym badaniu odkryto, w jaki sposób podstawowy enzymatyczny kompleks metaboliczny, używany kiedyś do rutynowych zadań komórkowych, został ewolucyjnie przeprogramowany w bakteriach jamy ustnej, by wytwarzać silny antybiotyk. Zrozumienie tej przemiany nie tylko ujawnia, jak natura wymyśla nową chemię, lecz także daje wskazówki przy projektowaniu kolejnej generacji leków i biokatalizatorów.
Od podstawowego metabolizmu do chemicznej broni
Wszystkie żywe komórki polegają na zestawie zachowanych enzymów prowadzących centralny metabolizm, takich jak rozkład tłuszczów czy budowa niezbędnych cząsteczek. Jedna z takich grup, nazwana nadrodziną tiolaz, zwykle pomaga w obsłudze małych, wysokoenergetycznych związków jak acetylo-CoA oraz wspiera kluczowe szlaki syntezy lipidów i innych składników komórki. Autorzy odkryli, że w kilku gatunkach Streptococcus z jamy ustnej trzyczęściowy kompleks oparty na tiolazie — złożony z białek spokrewnionych z HMGS, ACAT oraz trzeciego białka pomocniczego — porzucił swoją pierwotną metaboliczną rolę. Zamiast tego kompleks ten kończy biosyntezę antybiotyku nazywanego reutericykliną A, który pomaga tym bakteriom rywalizować w zatłoczonym środowisku jamy ustnej.
Nowy rodzaj reakcji enzymatycznej na szkielecie antybiotyku
Poprzez rekonstrukcję kompleksu Streptococcus w laboratorium i podawanie mu chemicznie zsyntetyzowanego prekursora reutericykliny A, badacze wykazali, że kompleks przeprowadza nietypową reakcję tworzenia wiązania węgiel–węgiel znaną jako akylacja Friedla–Craftsa typu C. Zamiast przyłączać grupę acetylową do tlenu, jak robi to wiele enzymów, instaluje tę grupę bezpośrednio na atomie węgla pierścienia pyrrolidyno-2,4-dionowego — istotnego elementu szkieletu reutericykliny. Kompleks akceptuje zarówno naturalne donorzy acetylu, takie jak acetylo-CoA, jak i kilka sztucznych donorów, a nawet może przeprowadzać reakcję wsteczną, rozbijając utworzone wiązanie. Ta elastyczność poszerza znane spektrum biologicznych acylotransferaz i sugeruje, jak takie enzymy można by zaadaptować do budowy różnorodnych produktów chemicznych.
Przeformowanie zachowanego rusztowania białkowego
Wykorzystując krio-elektronową mikroskopię o wysokiej rozdzielczości, zespół rozwiązał trójwymiarową strukturę kompleksu Streptococcus, nazwanego SmaATase. Pomimo nowej funkcji SmaATase zachowuje uderzające podobieństwo architektoniczne do związanego kompleksu w archeach, który uczestniczy w ścieżce mewalonianowej budowy lipidów izoprenoidowych. Oba są dużymi, multimerycznymi zespołami zbudowanymi z powtarzalnych modułów i mają wspólną jamę, w której kofaktor CoA może wiązać się i przemieszczać między miejscami aktywnymi. Jednak kluczowe reszty katalityczne istotne dla pierwotnej reakcji metabolicznej są w wersji bakteryjnej nieobecne lub zmienione. Testy biochemiczne potwierdzają, że SmaATase nie potrafi już syntetyzować przodkowego produktu HMG-CoA i zamiast tego używa acetylo-CoA wyłącznie jako donoru dla swoich nowych małocząsteczkowych substratów.
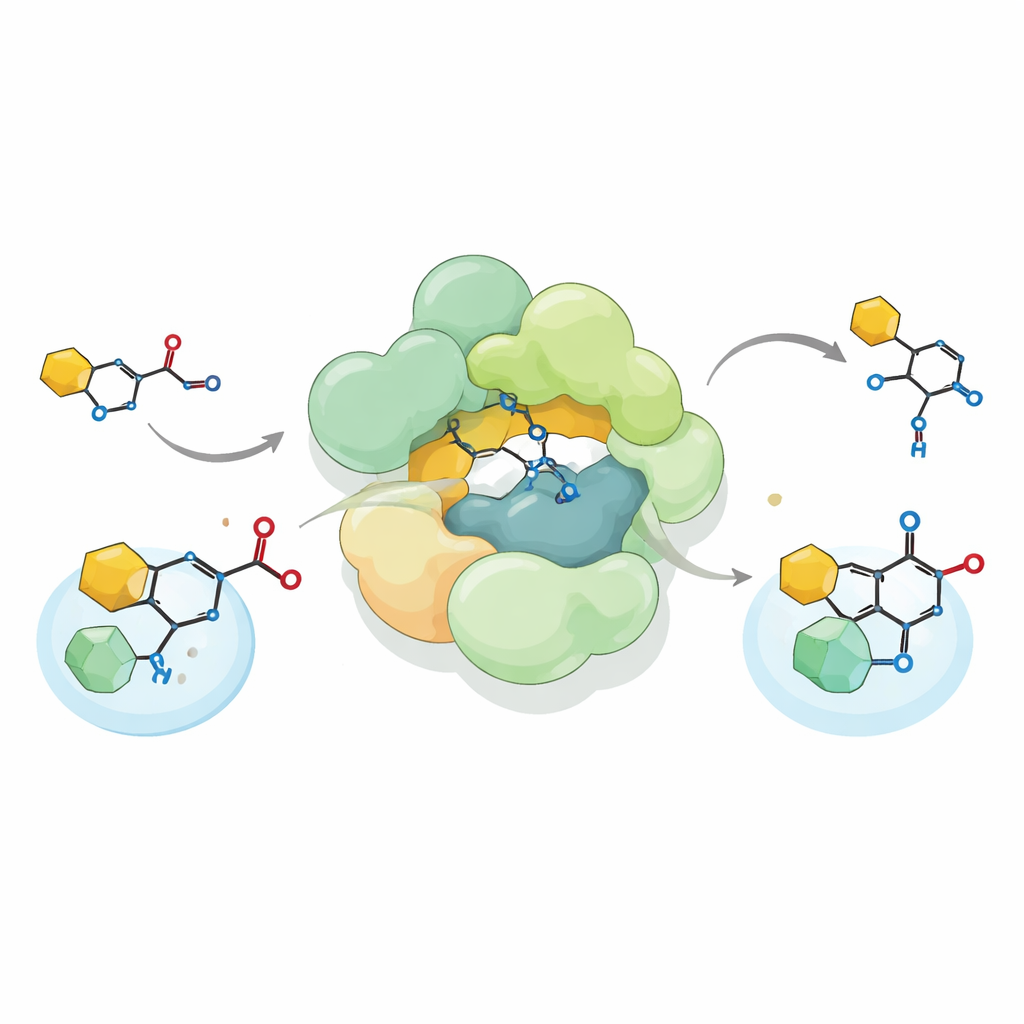
Ewolucyjny szlak od metabolizmu do antybiotyków
Aby zrozumieć, jak mogło dojść do takiego przekształcenia, autorzy porównali sekwencje i aktywności pokrewnych kompleksów w wielu bakteriach i archeach. Zidentyfikowali ponad tysiąc klastrów genowych zawierających ten sam zestaw trzech typów enzymów. Niektóre nadal wspierają klasyczną chemię tiolazową; inne, jak te w Pseudomonas, napędzają produkcję różnych małocząsteczkowych antybiotyków. Reprezentatywny kompleks z Pseudomonas fluorescens wydaje się znajdować pośrednio na tej ścieżce ewolucyjnej: jego domena podobna do HMGS jest nieaktywna, ale jednostka podobna do ACAT wciąż wykonuje bardziej konwencjonalną reakcję na substratach związanych z CoA. W SmaATase i w pseudomonasowym odpowiedniku tworzącym związek chroniący uprawy, DAPG, dalsze zmiany wokół miejsca aktywnego dostosowały enzymy do rozpoznawania niestandardowych akceptorów, takich jak pierścienie aromatyczne czy rdzenie tetraminowe.
Dlaczego maleńka grupa acetylowa robi wielką różnicę
Ostateczny biologiczny zysk tej molekularnej przeróbki jest oczywisty. Gdy zespół przetestował acetylowane antybiotyki reutericyklinę A i DAPG przeciw panelowi bakterii Gram-dodatnich, te cząsteczki wykazały silne działanie zabijające, podczas gdy ich nieacetylowane prekursory były znacznie słabsze lub prawie nieaktywne. Ta mała grupa acetylowa, umieszczona w odpowiednim miejscu przez przeznaczony do tego przeprogramowany kompleks enzymatyczny, zamienia skromny szkielet w potężną broń, pozwalając Streptococcus w jamie ustnej lub Pseudomonas przy korzeniach roślin wyprzeć konkurentów. Praca ta pokazuje, jak ewolucja może recyclować istniejące ramy enzymatyczne przy minimalnych, lecz strategicznych mutacjach, przekształcając rutynowe maszyny metaboliczne w wyspecjalizowane narzędzia obronne — i dostarczając planu dla inżynierów chcących zaprojektować nowe katalizatory tworzące wiązania węgiel–węgiel do odkrywania leków i biologii syntetycznej.
Cytowanie: Liao, G., Sun, R., Shen, Z. et al. Evolutionary repurposing of a metabolic thiolase complex enables antibiotic biosynthesis. Nat Commun 17, 2196 (2026). https://doi.org/10.1038/s41467-026-68910-6
Słowa kluczowe: ewolucja enzymów, biosynteza naturalnych produktów, chemia antybiotyków, metaboliczne przekształcenie, akylacja Friedla–Craftsa