Clear Sky Science · pl
Modelowanie włóknienia płuc na ludzkich komórkach iPSC ujawnia, że hamowanie p300/CBP tłumi przejściowy stan komórek pęcherzykowych
Dlaczego zwłóknienia płuc dotyczą nas wszystkich
Idiopatyczne włóknienie płuc (IPF) to postępująca choroba, w której płuca stopniowo zmieniają się w tkankę bliznowatą, przez co każdy oddech staje się trudniejszy. Dostępne leki jedynie spowalniają ten proces i często powodują niepokojące działania niepożądane. W tym badaniu wykorzystano nowoczesne narzędzia ze świata komórek macierzystych i genomiki, aby odtworzyć w laboratorium zbliznowaciałe płuca i postawić proste, ale istotne pytanie: czy da się znaleźć przełącznik, który skieruje uszkodzone komórki płuc z powrotem z szkodliwego stanu ku regeneracji?
Okno do zbliznowaciałego płuca hodowanego w laboratorium
Aby zbadać IPF, autorzy stworzyli zminiaturyzowane płuca z ludzkich indukowanych pluripotencjalnych komórek macierzystych (iPSC). iPSC prowadzono do różnicowania w komórki pęcherzykowe — komórki wyściełające drobne pęcherzyki powietrzne, gdzie tlen przenika do krwi — i hodowano razem z fibroblastami płucnymi, komórkami tkanki łącznej tworzącymi blizny. Osadzone w miękkim żelu, te „organoidy pęcherzykowe” zachowywały się podobnie do prawdziwej tkanki płucnej. Po ekspozycji na lek chemioterapeutyczny bleomycynę, znany induktor uszkodzeń płuc, żele kurczyły się pod wpływem napięcia wywieranego przez fibroblasty, odzwierciedlając skurcz tkanki obserwowany we włóknieniu.
Wykorzystując ten system, zespół przesiał bibliotekę 264 małych cząsteczek i automatycznie zmierzył, na ile każdy lek zapobiega kurczeniu się żelu, korzystając z narzędzia analizy obrazów opartego na uczeniu głębokim dla obiektywnych odczytów. Wiele związków nie wykazało efektu, ale jedna rodzina wyróżniała się wyraźnie: inhibitory białek p300 i CBP, które regulują pakowanie DNA i aktywność genów. Wszystkie osiem związków ukierunkowanych na p300/CBP w bibliotece zmniejszało kurczenie przy niskich dawkach, wskazując tę ścieżkę jako obiecujący punkt uchwytu we włóknieniu. 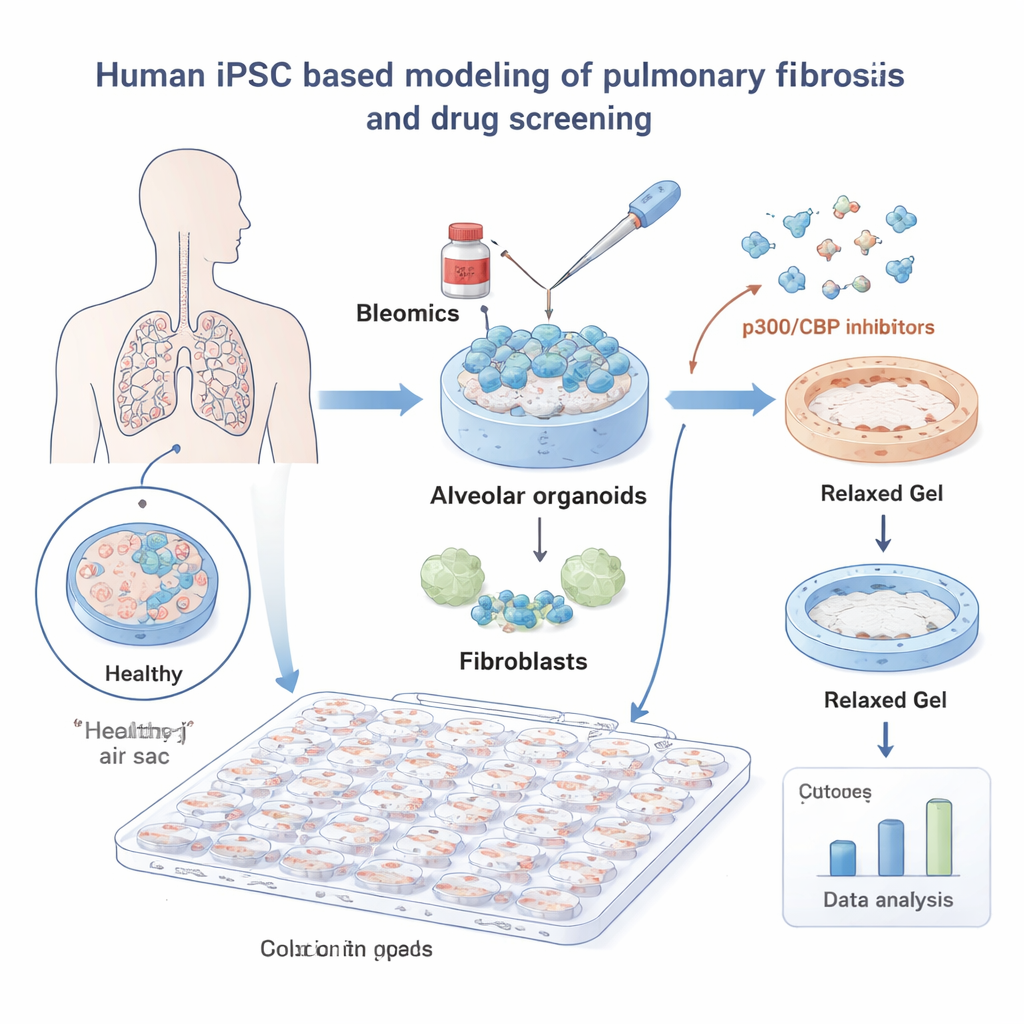
Sprawcy zamieszania: komórki przejściowe płuc
Ostatnie prace ujawniły problematyczny „pośredni” typ komórek w chorych płucach, określany jako przejściowy stan komórek pęcherzykowych. Normalnie komórki podporowe zwane AT2 dojrzewają do ultracienkich komórek AT1, które pokrywają pęcherzyki i umożliwiają wymianę gazową. W IPF jednak komórki AT2 często zatrzymują się w tym stanie przejściowym, wyrażając geny związane ze stresem i naprawą, zamiast zakończyć przejście do w pełni funkcjonalnych komórek AT1. Te komórki przejściowe gromadzą się w obszarach włóknienia i silnie komunikują się z fibroblastami, lecz nie było jasne, czy są jedynie skutkiem uszkodzenia, czy aktywnymi sprawcami bliznowacenia.
Poprzez sekwencjonowanie RNA i profilowanie otwartej chromatyny w swoich organoidach autorzy pokazali, że komórki przejściowe powstające w ich modelu bardzo przypominały te znalezione w płucach pacjentów z IPF. Wywołane komórki przejściowe wykazywały sygnatury genowe stresu, zapalenia i przebudowy macierzy, i silnie aktywowały współhodowane dorosłe fibroblasty płucne. Co istotne, gdy p300/CBP został zablokowany, markery stanu przejściowego spadły, tożsamość AT2 została lepiej zachowana, a aktywacja fibroblastów słabła. Innymi słowy, leki nie ogólnie zatruwały komórek; selektywnie zapobiegały utknięciu komórek AT2 w tym szkodliwym limbo.
Rozplątanie molekularnych przełączników
Aby zrozumieć, jak p300/CBP kształtuje tę decyzję o losie komórki, zespół przeanalizował chemiczne modyfikacje histonów — białek pomagających w pakowaniu DNA. Szczególna modyfikacja, acetylacja H3K27, jest często nakładana przez p300/CBP w aktywnych wzmacniaczach i promotorach. W komórkach przejściowych regiony w pobliżu genów odpowiedzi na stres i pro‑włóknieniowych niosły silną acetylację H3K27 i były wzbogacone w miejsca wiązania czynników transkrypcyjnych, takich jak AP‑1 i HNF1B. Po leczeniu inhibitorami p300/CBP te acetylowe markery zmalały w tych miejscach, a ekspresja wielu genów pro‑włóknieniowych spadła. Bezpośrednie blokowanie AP‑1 lub zmniejszenie poziomów AP‑1 i HNF1B za pomocą małych interferujących RNA również ograniczało program przejściowy i kurczenie organoidów, łącząc to trio — p300/CBP, AP‑1 i HNF1B — z mechanizmem napędzającym przebudowę włóknistą.
Ponad hodowlą in vitro, badanie przetestowało jeden inhibitor, CBP30, na myszach z uszkodzeniem płuc wywołanym bleomycyną. Zwierzęta otrzymujące CBP30 miały mniej komórek przejściowych nabłonka, mniejszą aktywację mioblastów tworzących blizny oraz obniżoną ekspresję markerów włóknienia. To krzyżowe zatwierdzenie między modelami opartymi na ludzkich komórkach macierzystych a modelem zwierzęcym wzmacnia argument, że p300/CBP nie jest jedynie artefaktem laboratoryjnym, lecz rzeczywistym regulatorem bliznowacenia płuc. 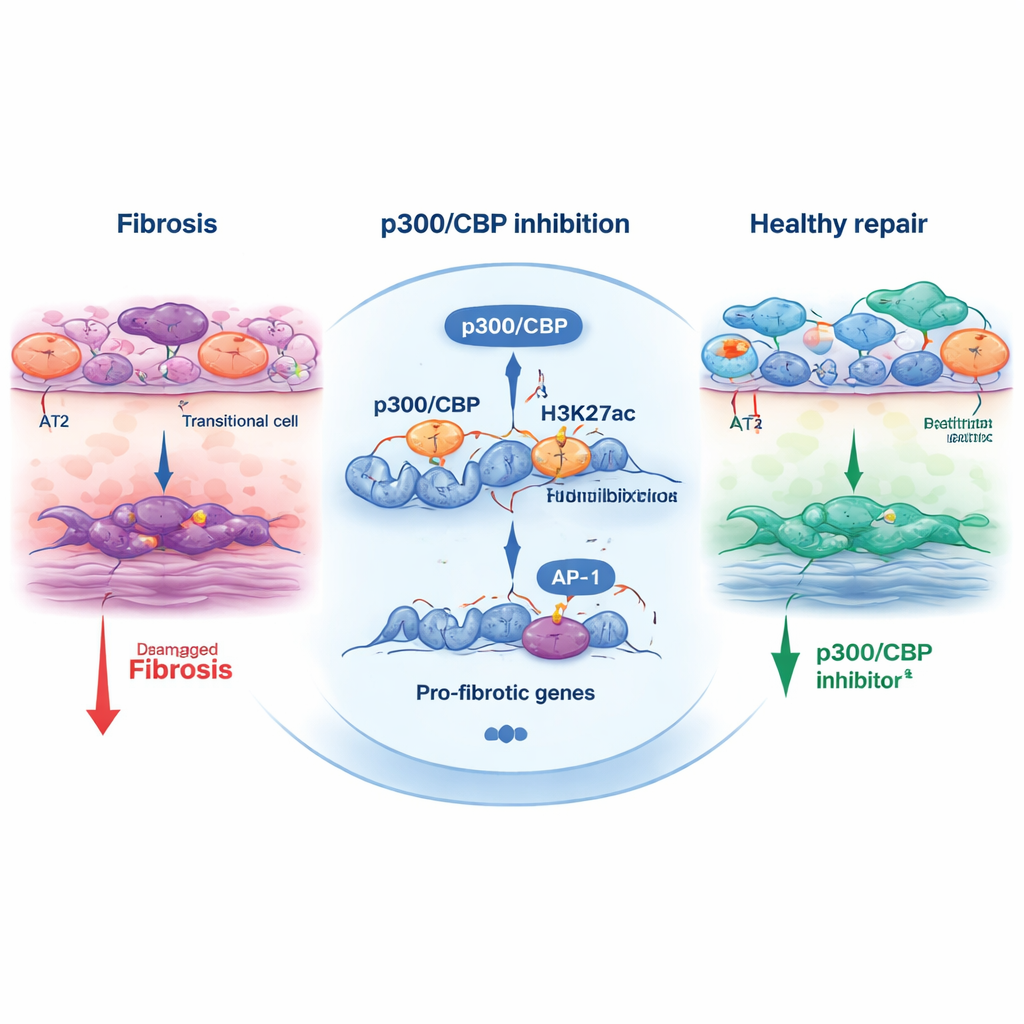
Co to znaczy dla przyszłych terapii
Dla czytelników niebędących specjalistami kluczowe przesłanie jest takie, że autorzy zbudowali realistyczny ludzki model włókniejących płuc i użyli go, aby wyeksponować nowy cel dla leków. Ich praca sugeruje, że bliznowacenie płuc jest częściowo napędzane odwracalnym, indukowanym stresem stanem przejściowym komórek, który wprowadza otaczającą tkankę w błąd. Zmniejszając aktywność p300/CBP, być może da się stłumić ten stan, utrzymać komórki pęcherzykowe na zdrowej ścieżce rozwojowej i zredukować sygnały popychające fibroblasty do nadaktywności. Choć inhibitory p300/CBP nadal muszą być zoptymalizowane pod kątem bezpieczeństwa i przetestowane klinicznie, badanie wskazuje na terapie adresujące podstawową komórkową nieporozumień w IPF, a nie jedynie spowalniające jego skutki.
Cytowanie: Tsutsui, Y., Masui, A., Konishi, S. et al. Human iPSC-based Modeling of Pulmonary Fibrosis Reveals p300/CBP Inhibition Suppresses Alveolar Transitional Cell State. Nat Commun 17, 1214 (2026). https://doi.org/10.1038/s41467-026-68909-z
Słowa kluczowe: idiopatyczne włóknienie płuc, organoidy pęcherzykowe, inhibitory p300/CBP, komórki nabłonkowe w stanie przejściowym, komórki macierzyste płuc