Clear Sky Science · pl
Projektowanie plazmidów z syntetycznymi miejscami rozpoczęcia replikacji
Dlaczego przepisanie DNA mikroorganizmów ma znaczenie
Wiele narzędzi współczesnej biotechnologii — od produkcji insuliny po zaawansowane układy genetyczne — opiera się na małych kółkach DNA zwanych plazmidami. Te genetyczne konwoje wprowadzają zaprojektowane geny do bakterii, jednak ich podstawowa konstrukcja prawie się nie zmieniła od dekad. Badanie to pokazuje, że samo serce plazmidów — sekwencje, które mówią komórkom, kiedy i jak często je kopiować — można kompletnie przeprojektować. Poprzez odbudowanie tego „silnika kopii” od podstaw, autorzy tworzą plazmidy łatwiejsze do regulacji, łączenia i programowania, otwierając drogę do bardziej elastycznych metod diagnostycznych, bioprodukcji i zastosowań biologii syntetycznej.
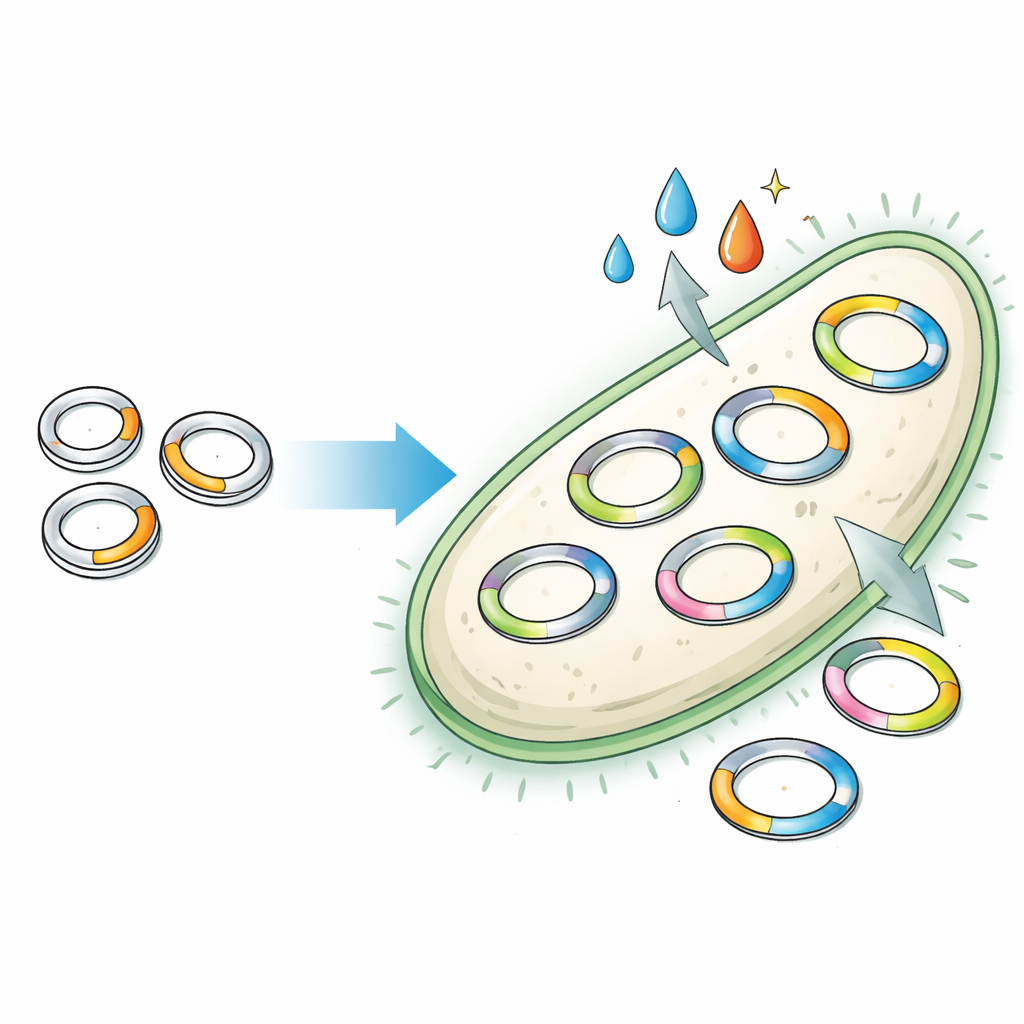
Stare narzędzia z ukrytymi ograniczeniami
Plazmidy ewoluowały naturalnie jako ruchome elementy DNA, pomagając bakteriom wymieniać cechy, takie jak oporność na antybiotyki czy nowe sposoby trawienia źródeł pokarmu. W laboratorium inżynierowie wykorzystują te plazmidy do przenoszenia pożytecznych genów, ale większość opiera się na kilku klasycznych projektach odkrytych w latach 80. XX wieku. Te stare układy skrywają plątaninę nakładających się części genetycznych, które kontrolują, ile kopii plazmidu znajduje się w każdej komórce i czy różne plazmidy mogą współistnieć. Ponieważ te elementy są ze sobą połączone, zmiana jednej cechy może nieprzewidywalnie uszkodzić inną. W efekcie naukowcy mają do dyspozycji ograniczony wybór plazmidów o stałej liczbie kopii i ograniczonej kompatybilności, co hamuje złożoność projektowanych systemów.
Odbudowa silnika kopii od podstaw
Naukowcy skupili się na powszechnie używanym miejscu rozpoczęcia replikacji z rodziny plazmidów pMB1. W swojej naturalnej formie to miejsce wykorzystuje subtelną równowagę między dwoma RNA — jednym inicjującym kopiowanie DNA i drugim je hamującym — aby utrzymać liczbę plazmidów pod kontrolą. Zespół najpierw „refaktoryzował” ten system: rozdzielił nakładające się geny, wyłączył ukryty promotor i umieścił kluczowe elementy na oddzielnych, uporządkowanych kasetach genetycznych. Już samo to pokazało, że podstawowa funkcja miejsca może zostać zachowana przy jednoczesnym uproszczeniu jego układu, przekształcając zagracony, ukształtowany przez ewolucję element w coś bardziej przypominającego modułową maszynę z dostępnymi składnikami.
Wstawianie syntetycznych pokręteł regulacyjnych
Gdy oryginalna logika kontroli została ujawniona, autorzy zastąpili ją w pełni syntetycznymi regulatorami. Połączyli starter replikacji z zaprojektowanymi przełącznikami RNA, które działają jak pokrętła ściemniania: małe RNA kontrolujące mogą odwracać te przełączniki, aby zezwolić lub zablokować produkcję startera, a tym samym kopiowanie plazmidu. Wybierając różne warianty przełączników i łącząc je z promotorami o zróżnicowanej sile, dostroili liczbę kopii plazmidów w zakresie obejmującym ponad dwie rzędy wielkości. Zbadali również różne fizyczne układy kaset kontrolnych na DNA, odkrywając konfiguracje, które poprawiały stabilność i pozwalały zmniejszyć region replikacyjny do zwartego, funkcjonalnego rdzenia, jednocześnie dodając naturalne systemy pomocnicze, które zapobiegają problemom z zaplątywaniem się plazmidów.
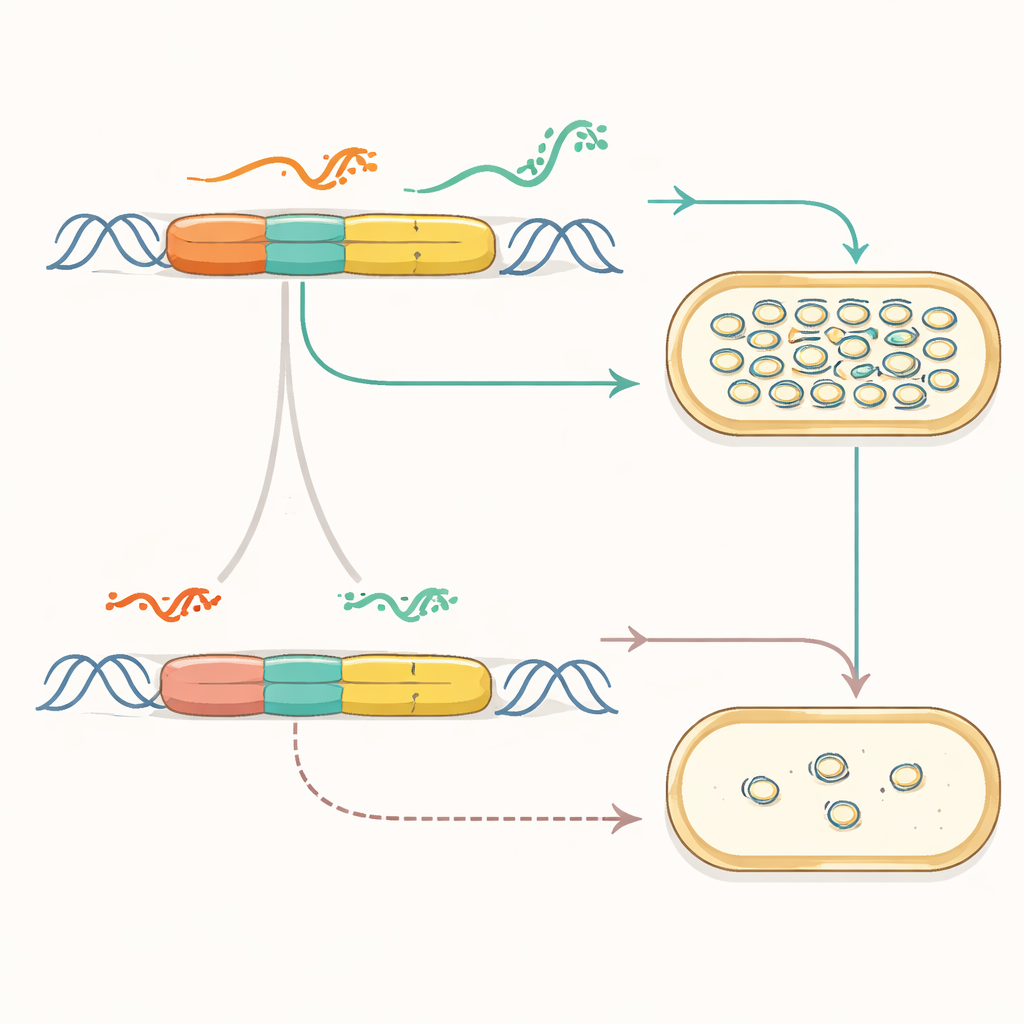
Przekształcanie sygnałów chemicznych w liczbę kopii DNA
Gdy silnik kopii stał się modułowy, zespół pokazał, że można go podłączyć do sygnałów zewnętrznych. Połączyli syntetyczne miejsce rozpoczęcia z indukowalnymi promotorami i strukturami RNA zwanymi riboswitchami, które zmieniają kształt w odpowiedzi na małe cząsteczki. W tych nowych plazmidach dodanie związku chemicznego, takiego jak IPTG czy kumat, powodowało wzrost lub spadek liczby kopii plazmidu — a więc i sygnału raportera. Kilka sygnałów można było łączyć tak, że jedna substancja pobudzała kopiowanie, podczas gdy inna je hamowała. Naukowcy skonstruowali nawet pary plazmidów, z których każdy reagował na inny związek, i śledzili zmiany ich liczby kopii w tej samej komórce za pomocą sekwencjonowania DNA, skutecznie przekształcając liczbę plazmidów w kod kreskowy historii środowiskowej.
Wiele niestandardowych plazmidów w jednej komórce
Kluczowym testem tej strategii było sprawdzenie, czy kilka niezależnie kontrolowanych plazmidów może współistnieć. Dzięki bibliotece ortogonalnych regulatorów RNA zespół zbudował sześć różnych plazmidów, z których każdy miał własne syntetyczne miejsce rozpoczęcia i marker antybiotykowy, i wprowadził wszystkie sześć jednocześnie do E. coli. Sekwencjonowanie całych plazmidów przez kilka dni potwierdziło, że wszystkie sześć pozostało obecnych, choć ich względne obfitości się zmieniały. Próby osiągnięcia tego samego przy użyciu sześciu konwencjonalnych plazmidów nie powiodły się, co podkreśla, że refaktoryzowana konstrukcja i dodane systemy stabilizujące czynią nowe plazmidy bardziej kompatybilnymi i odpornymi, gdy są zgromadzone razem w jednej komórce.
Co to oznacza dla przyszłej biotechnologii
Dla niespecjalisty wniosek jest prosty: autorzy przekształcili plazmidy z sztywnych, uniwersalnych narzędzi w platformę konfigurowalną. Ich syntetyczne miejsca rozpoczęcia replikacji działają jak silniki typu plug-and-play, których prędkość, czułość i wejścia można dobierać według potrzeb. Umożliwia to budowanie bakterii, które zapisują ekspozycje chemiczne jako zmiany w liczbie kopii DNA, testowanie wielu ścieżek genetycznych równolegle poprzez rozdzielenie ich na różne plazmidy lub precyzyjne balansowanie wzrostu i produkcji w szczepach przemysłowych. Choć pewne kompromisy związane ze stabilnością pozostają, praca ta pokazuje, że podstawowe mechanizmy replikacji plazmidów nie są już poza zasięgiem inżynierii, otwierając nowe pole dla innowacji w biologii syntetycznej.
Cytowanie: Liu, B., Seet, Z.R.D., Peng, X. et al. Engineering plasmids with synthetic origins of replication. Nat Commun 17, 2255 (2026). https://doi.org/10.1038/s41467-026-68907-1
Słowa kluczowe: syntetyczne plazmidy, miejsce rozpoczęcia replikacji, regulatory RNA, kontrola liczby kopii, biologia syntetyczna