Clear Sky Science · pl
Receptor sukcynianowy 1 ogranicza hematopoezę i zapobiega progresji ostrej białaczki szpikowej
Gdy paliwo komórkowe idzie na manowce
Nasza krew jest nieustannie odnawiana dzięki niewielkiej populacji komórek macierzystych ukrytych w szpiku kostnym. W tym badaniu zbadano, jak powszechny produkt uboczny metabolizmu — sukcynian — oraz jego czujnik na powierzchni komórki działają jak hamulec tego systemu odnowy. Gdy ten hamulec zawodzi, równowaga między zdrową produkcją krwi a rozrostem nowotworowym może przechylić się w stronę ostrej białaczki szpikowej (AML), agresywnego raka krwi. Zrozumienie tego ukrytego przełącznika kontrolnego może prowadzić do bardziej precyzyjnych terapii, które okiełznają chorobę przez przywrócenie własnych mechanizmów ochronnych organizmu.
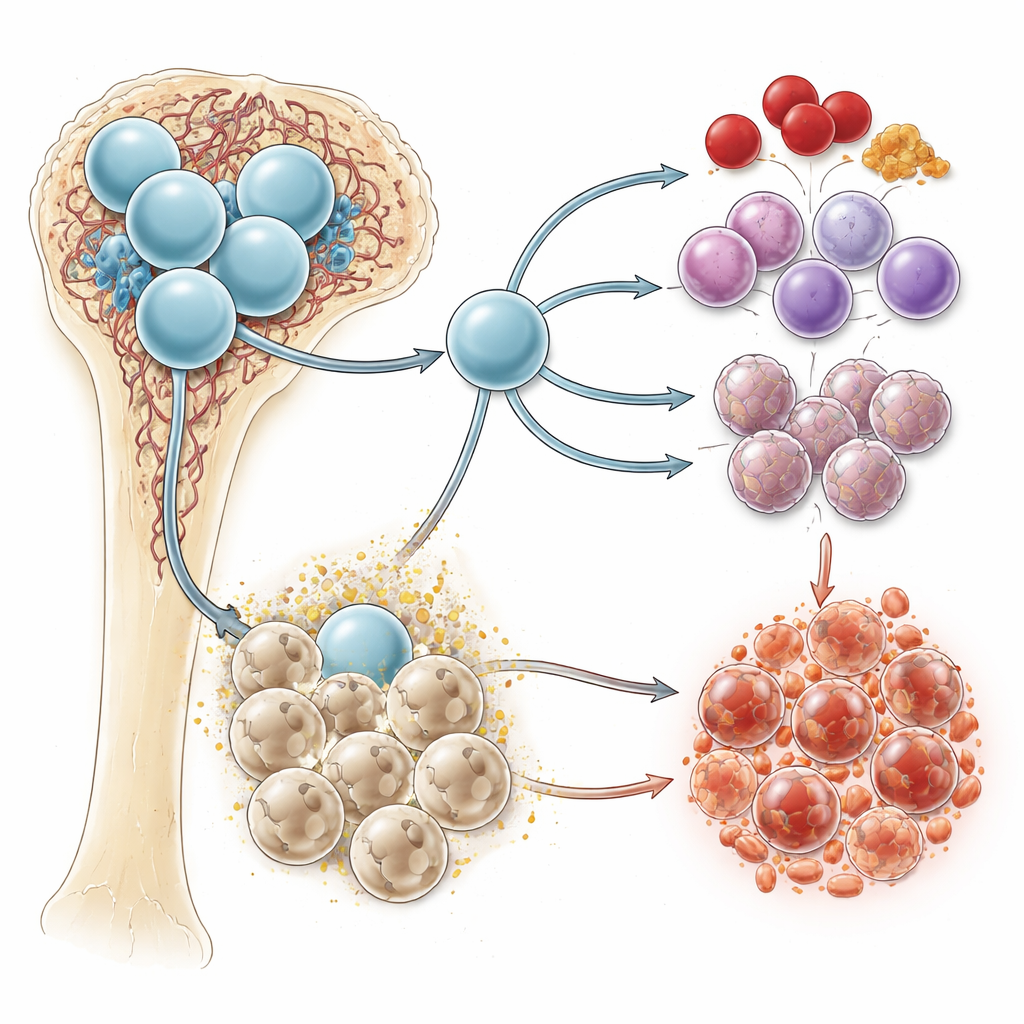
Chemiczny sygnał o podwójnym życiu
Sukcynian jest rutynowym produktem ubocznym spalania paliwa przez komórki, zwłaszcza w mitochondriach, „elektrowniach” komórki. W warunkach niskiego stężenia tlenu — takich, jakie panują w szpiku — sukcynian ma tendencję do kumulowania się. Może działać wewnątrz komórek, zmieniając metabolizm i odpowiedzi zapalne, a także przenikać na zewnątrz, funkcjonując jako sygnał. Na powierzchni komórki receptor zwany SUCNR1 wykrywa sukcynian i przekazuje jego obecność do wnętrza. Wcześniejsze prace łączyły sukcynian i SUCNR1 z zapaleniem i środowiskami sprzyjającymi nowotworom, ale ich bezpośrednia rola w tworzeniu krwi i białaczce pozostawała niejasna.
Oznaka ostrzegawcza u pacjentów z białaczką
Naukowcy przeanalizowali dane ekspresji genów od setek pacjentów z AML i odkryli, że poziomy SUCNR1 znacznie różnią się między osobami. Pacjenci, których komórki białaczkowe wytwarzały niewiele SUCNR1, mieli krótsze przeżycie całkowite i dłuższy okres bez progresji, nawet po uwzględnieniu wieku, płci i standardowych podtypów klinicznych. Pewne podgrupy genetyczne AML wykazywały szczególnie niski poziom SUCNR1. Gdy zespół przeszczepił ludzkie komórki AML pozbawione SUCNR1 do myszy o upośledzonym układzie odpornościowym, a następnie wstrzyknął zwierzętom kwas sukcynowy (który w organizmie przekształca się w sukcynian), obciążenie białaczkowe w szpiku wzrosło. Sugerowało to, że w nowotworach z niskim SUCNR1 dodatkowy sukcynian może faktycznie napędzać postęp choroby zamiast go hamować.
Ukryty hamulec w komórkach macierzystych krwi
Aby zrozumieć, jak SUCNR1 działa w normalnej hematopoezie, naukowcy zwrócili się ku genetycznie zmodyfikowanym myszom. Gdy SUCNR1 został usunięty zarówno w całym organizmie, jak i tylko w komórkach tworzących krew, szpik stał się nadaktywny. Komórki macierzyste i progenitorowe się rozmnożyły, a zarówno komórki mieloidalna (takie jak monocyty i granulocyty), jak i komórki B zwiększyły się we krwi i śledzionie. Te komórkopodobne komórki przeżywały lepiej i tworzyły więcej kolonii w hodowlach in vitro, choć były nieco mniej zdolne do ponownego zainicjowania produkcji krwi po konkurencyjnym przeszczepieniu z normalnymi komórkami. Specjalna linia myszy z reporterem wykazała, że tylko podzbiór komórek macierzystych i progenitorowych faktycznie ekspresjonuje SUCNR1; komórki pozytywne pod kątem SUCNR1 miały szczególnie ograniczony potencjał zasiedlania. Ogólnie receptor działał jak ogranicznik wielkości i aktywności puli komórek macierzystych.
Od wyważonej obrony do zapalnego przeładowania
Szczegółowe profilowanie ekspresji genów w komórkach macierzystych i progenitorowych pozbawionych SUCNR1 ujawniło uderzającą zmianę. Sygnatury cichych, prymitywnych komórek macierzystych zostały stłumione, podczas gdy geny związane z zapaleniem, reaktywnymi formami tlenu i dojrzałymi komórkami krwi zostały wzmocnione. Na wyróżnienie zasługiwały dwie cząsteczki: S100A8 i S100A9, para „alarmin”, które wzmacniają sygnalizację zapalną. Czynniki te były podwyższone zarówno w obrębie kompartmentu komórek macierzystych, jak i w otaczającym płynie szpiku. Gdy zespół leczył myszy pozbawione SUCNR1 tasquinimodem, lekiem blokującym sygnalizację S100A9, nadmierne rozszerzenie komórek macierzystych i progenitorowych oraz nadprodukcja komórek mieloidalnych i B zostały w dużej mierze odwrócone. Innymi słowy, dużą część szkód spowodowanych utratą SUCNR1 można było cofnąć przez przerwanie pętli alarmowej S100A8/S100A9.
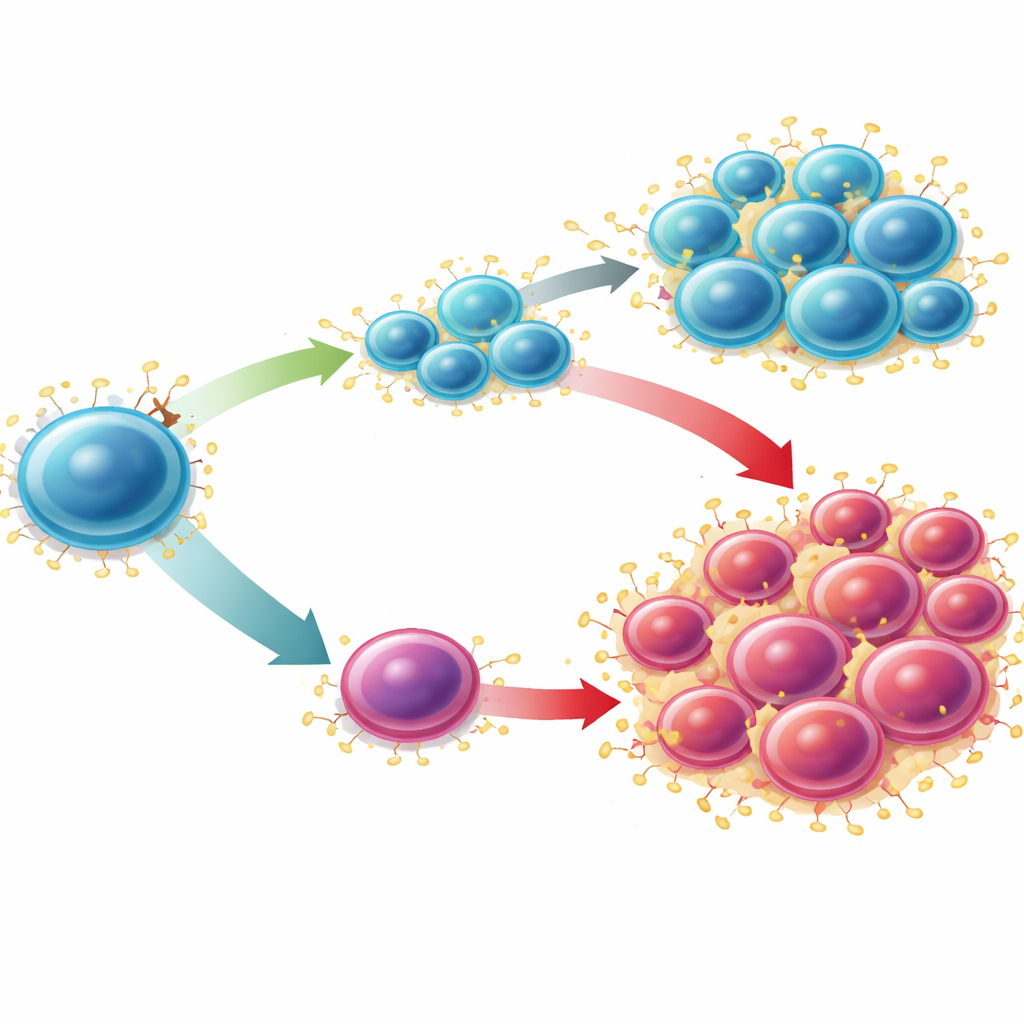
Przekształcenie wrażliwości w strategię leczenia
Naukowcy zapytali następnie, czy tę ścieżkę można wykorzystać terapeutycznie w AML. W agresywnej mysiej białaczce wywołanej mutacją MLL-AF9 — gdzie poziomy Sucnr1 są bardzo niskie — blokowanie S100A9 za pomocą tasquinimodu, szczególnie w połączeniu z silnym związkiem aktywującym SUCNR1, zmniejszało liczbę komórek przypominających komórki macierzyste białaczki i obniżało obciążenie chorobą w szpiku i śledzionie. Analizy danych z pojedynczych komórek RNA z modeli ludzkiego AML leczonych lekiem cytarabina wykazały, że klastry komórek opornych były bogate w S100A8 i S100A9, podczas gdy SUCNR1 był rzadki i powiązany z innym, metabolicznie aktywnym podzbiorem, który kurczył się po leczeniu. W ludzkich liniach komórkowych białaczki aktywacja SUCNR1 zwiększała śmierć komórek wywołaną chemioterapią i mogła sama wywołać apoptozę, gdy SUCNR1 był nadprodukowany. Razem te ustalenia lokują niski SUCNR1 nie tylko jako marker złego rokowania, ale także jako słabość: komórki białaczkowe, które utraciły ten hamulec, mogą silnie polegać na osi S100A8/S100A9 i być szczególnie wrażliwe na strategie, które reaktywują sygnalizację SUCNR1 lub blokują jej następcze alarmy.
Nowy dźwignia do ujarzmienia białaczki
Dla czytelnika niebędącego specjalistą zasadniczy przekaz jest taki, że pozornie prozaiczny produkt uboczny metabolizmu — sukcynian — i jego receptor SUCNR1 tworzą nieoczekiwany system bezpieczeństwa w tworzeniu krwi. Gdy SUCNR1 jest obecny i aktywny, utrzymuje komórki macierzyste w ryzach i zapobiega niekontrolowanemu wzrostowi. Gdy SUCNR1 zostaje utracony lub jest niski — co bywa u niektórych pacjentów z AML — sukcynian i zapalne alarminy takie jak S100A8 i S100A9 mogą popchnąć komórki macierzyste i progenitorowe w kierunku nadmiernego rozrostu i białaczki. Poprzez łączenie leków tłumiących ten zapalny alarm z czynnikami przywracającymi lub naśladującymi sygnalizację SUCNR1 może być możliwe przywrócenie równowagi w produkcji krwi i poprawa skuteczności istniejącej chemioterapii.
Cytowanie: Cuminetti, V., Boet, E., Heugel, M. et al. Succinate receptor 1 restricts hematopoiesis and prevents acute myeloid leukemia progression. Nat Commun 17, 2403 (2026). https://doi.org/10.1038/s41467-026-68906-2
Słowa kluczowe: ostra białaczka szpikowa, receptor sukcynianu, hematopoetyczne komórki macierzyste, metabolizm i rak, sygnalizacja zapalna